Aplicação de diferentes intensidades de campo magnético no cultivo da microalga Spirulina sp. LEB 18
ISBN 978-85-85905-21-7
Área
Bioquímica e Biotecnologia
Autores
Copello Veiga, M. (UNIVERSIDADE FEDERAL DO RIO GRANDE) ; Martins Fontoura, M. (UNIVERSIDADE FEDERAL DO RIO GRANDE) ; Gonçalves de Oliveira, M. (UNIVERSIDADE FEDERAL DO RIO GRANDE) ; Oliveira dos Santos, L. (UNIVERSIDADE FEDERAL DO RIO GRANDE)
Resumo
Diferentes formas de cultivo vêm sendo estudadas para obter melhoria no crescimento de microalgas, como a aplicação de campos magnéticos (CM). Neste estudo utilizou-se Spirulina sp. LEB 18 em meio Zarrouk e cultivada em fotobiorreatores tubulares de 2 L (volume útil de 1,8 L), a 35ºC durante 16 d. Cultivos controles (CC) foram realizados sem aplicação de CM e cultivos com aplicação de 30 e 60 mT. Durante os cultivos determinou-se concentração de biomassa, produtividade máxima (Pmáx), concentração celular máxima (Xmáx), velocidade específica máxima de crescimento (µmáx) e pH. Os cultivos controle e com aplicação de CM de 60 mT apresentaram maiores valores de µmáx 0,17 ± 0,01 d-1 e 0,19 ± 0,02 d-1, respectivamente, resultando em menor tempo de divisão celular.
Palavras chaves
Biomassa; Campos Magnéticos; Cianobactéria
Introdução
As microalgas são micro-organismos fotossintéticos capazes de transformar energia luminosa em compostos orgânicos, algumas espécies em condições adequadas de cultivo podem duplicar sua biomassa diariamente (VONSHAK, 1997). As microalgas podem produzir ampla gama de produtos devido sua composição (SALLA et al., 2016). O teor de carboidratos da biomassa microalgal pode ser utilizado na produção de bioetanol e como fonte de nutrientes em meios de cultivo para crescimento microbiano. Além disso, o teor de lipídios é promissor para a produção de biodiesel (YEN et al., 2013). Por apresentar elevada concentração de proteínas e conteúdo nutricional, a biomassa de Spirulina se destaca como matéria-prima na formulação de suplementos alimentares para humanos e ração para animais (PATIL et al., 2015). A cianobactéria Spirulina sp. é utilizada mundialmente para extração de biocompostos encontrados em sua biomassa, principalmente aqueles com propriedades antioxidantes. A Spirulina sp. é reconhecida como GRAS (Generally Recognized as Safe) pelo FDA (Food and Drug Administration) o que garante sua utilização em formulações de alimentos sem apresentar riscos à saúde (FOX, 1996). A modificação de alguns parâmetros de cultivo vem sendo realizada com o objetivo de causar situações de estresse a microalga, estimulando o crescimento celular e a indução metabólica de produtos de interesse. Neste contexto, alguns parâmetros nos cultivos vêm sendo modificados com o objetivo de estimular o crescimento e induzir a produção de biomoléculas de interesse. A utilização de tratamentos magnéticos no cultivo microalgal apresenta certas vantagens, como não apresentar toxicidade e não ser poluente, além disso, é uma tecnologia segura e com menor custo (TU et al., 2015). Desta forma, o objeto do estudo foi avaliar a influência de campos magnéticos de 30 mT e 60 mT na concentração celular da microalga Spirulina sp. LEB 18.
Material e métodos
A cianobactéria Spirulina sp. LEB 18 foi utilizada sendo mantida em meio Zarrouk padrão (ZARROUK, 1966). Os cultivos foram realizados em fotobiorreatores tubulares verticais de 2 L, com volume útil de 1,8 L e com concentração de biomassa inicial de 0,2 g/L. Esses foram mantidos em estufa termostatizada a 35ºC, com iluminância de 30 µmol/m2s e fotoperíodo de 12 h claro/escuro, durante 16 d. A aeração dos cultivos foi 0,3 vvm (volume de ar volume de meio-1 min-1). A evaporação de água dos cultivos foi compensada com a reposição diária de água destilada estéril. Cultivos controle (CC) foram realizados sem a aplicação de CM e cultivos com aplicação de CM com intensidades de 30 mT e 60 mT. Os CM foram gerados através da aplicação de ímãs de ferrite dispostos ao redor dos fotobiorreatores a 180º um do outro, foram realizadas triplicatas de cada condição de cultivo. O período de exposição dos ensaios ao CM foi de 24 h/d. Diariamente foram retiradas amostras de 5 mL de cada fotobiorreator para determinação de concentração celular e pH. A concentração de biomassa foi avaliada diariamente mediante a leitura da densidade ótica dos cultivos em espectrofotômetro (670 nm) (MORAIS et al., 2008) e o pH dos cultivos foi avaliado através de pHmetro digital. Os parâmetros cinéticos avaliados dos cultivos foram: a concentração de biomassa máxima (Xmáx), produtividade máxima (Pmáx) (Pmáx = (X-X0)/(t- t0)), velocidade específica máxima de crescimento (µmáx) (µmáx = (1/x). (dx/dt)) e tempo de geração (Tg) (Tg = ln(2)/µmáx). As respostas obtidas nos cultivos foram avaliadas por análise de variância (ANOVA) e por teste de Tukey para comparação entre médias, com intervalo de significância de 95% de confiança.
Resultado e discussão
A concentração de biomassa máxima (Xmáx) para todos os ensaios foi
encontrada no 16º d. No cultivo controle (CC), Xmáx foi 0,98 ± 0,02 g/L, já
para os cultivos com aplicação de CM de 30 mT e 60 mT, Xmáx foi 1,02 ± 0,10
g/L e 1,10 ± 0,05 g/L, respectivamente. No cultivo de Spirulina sp. LEB 18,
Deamici, Costa e Santos (2016) obtiveram valores de Xmáx de 2,37 g/L-1 ao
utilizar 30 mT e 2,38 g/L utilizando 60 mT, sendo que o período de exposição
do cultivo ao CM foi 1 h d-1. No presente estudo não houve diferença
significativa no valor de Xmáx para os ensaios, porém o tempo de exposição
utilizado foi 24 h/d.
Entretanto, a velocidade específica máxima de crescimento (µmáx) apresentou
menor valor utilizando 30 mT (0,12 ± 0,03 d-1), em relação ao cultivo
controle (0,19 ± 0,02 d-1) e com 60 mT (0,17 ≤ 0,01 d-1). A velocidade
específica máxima é um parâmetro importante no cultivo, pois a partir dela é
possível determinar o tempo necessário para uma célula duplicar-se, portanto
quanto maior µmáx, menor tempo de cultivo é necessário para obtenção de
biomassa. A partir da Tabela 1, pode-se observar que houve diferença
significativa no Tg, sendo que os ensaios controle e com aplicação de 60 mT
apresentaram valores menores quando comparados ao ensaio de 30 mT, sendo
mais promissores para produção de biomassa de Spirulina sp. LEB 18 em menor
tempo de cultivo.
Segundo Li et al. (2007) a aplicação de até 40 mT estimulou o crescimento de
Spirulina, porém intensidades superiores apresentaram efeito inibitório
sobre o crescimento da microalga. No presente estudo observou-se o
crescimento de Spirulina sp. em ambas intensidades testadas, sendo uma delas
superior a 40 mT (60 mT), mostrando que a aplicação de CM estimula o
crescimento da microalga.
Ao analisar a Figura 1, é possível observar que o pH dos cultivos de
Spirulina ficou na faixa de 9,5 e 10,6. Segundo Costa et al. (2002), o
cultivo da cianobactéria deve ser realizado em pH entre 8,3 e 11,0, pois é
nesta faixa que ela apresenta maior taxa fotossintética, além disso, fora
deste intervalo os cultivos estão sujeitos à contaminação. Segundo Shiraiwa
et al. (1993), o aumento gradual do pH reflete o mecanismo de assimilação do
bicarbonato por cianobactérias. Pois, quando as células incorporam dois íons
de bicarbonato, um é consumido e internalizado como dióxido de carbono
(CO2), enquanto o outro é liberado como carbonato (CO3-2), levando ao
aumento progressivo do pH no meio.
A aplicação de 30 mT não alterou o pH do cultivo quando comparado ao ensaio
controle, porém houve oscilação no início do ensaio de 60 mT. Dependendo da
intensidade aplicada o CM pode alterar os níveis de energia e orientação do
spin dos elétrons. Segundo UNEP (United Nations Environment Programa), WHO
(World Health Organizations) e IRPA (International Radiation Protection
Association) (1987), CM estáticos podem alterar níveis de energia e
orientação da rotação de elétrons, o que pode ter ocasionado a oscilação do
pH no início do cultivo.
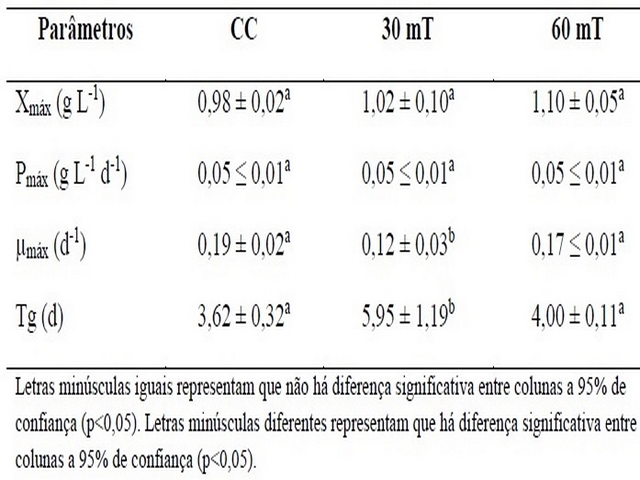
Parâmetros de crescimento obtidos nos cultivos de Spirulina sp. LEB 18 com aplicação de CM de 30 mT e 60 mT e do cultivo controle (CC).

Valores de pH dos cultivos de Spirulina sp. LEB 18 com aplicação de CM de 30 mT (□), 60 mT (◊) e do cultivo controle (○).
Conclusões
A utilização de diferentes intensidades de CM (30 mT e 60 mT) não influenciou no crescimento da microalga Spirulina sp. LEB 18 quando comparado ao cultivo controle. Porém devido aos maiores valores encontrados de µmáx e Tg para o cultivo com aplicação de 60 mT (0,17 ≤ 0,01 d-1; 4,00 ± 0,11 d) e cultivo controle (0,19 ± 0,02 d-1; 3,62 ± 0,32 d) são as condições de cultivo mais promissoras para obtenção de biomassa em tempo menor de cultivo. Embora os demais parâmetros cinéticos não tenham diferido estatisticamente, as diferentes intensidades do CM podem ter ocasionado modificações na composição bioquímica das microalgas.
Agradecimentos
CAPES, CNPq e Universidade Federal do Rio Grande.
Referências
COSTA, J. A. V.; COLLA, L. M.; DUARTE FILHO, P.; KABKE, K.; WEBER, A.
Modeling of Spirulina platensis growth in fresh water using response surface
methodology. World Journal Microbiology and Biotechnology, v. 18, p. 603-607, 2002.
DEAMICI, K. M.; COSTA, J. A. V.; SANTOS, L. O. Magnetic fields as triggers of microalga growth: evaluation of its effect on Spirulina sp. Bioresource Technology, v. 220, p. 62–67, 2016.
FOX, R. D. Spirulina Production e Potencial. France: Edsud, 1996.
HUNT, R. W.; ZAVALIN, A.; BHATNAGAR, A.; CHINNASAMY, S.; DAS, K. C. Electromagnetic biostimulation of living cultures for biotechnology, biofuel and bioenergy applications. International Journal of Molecular Sciences, v. 10, n. 10, p. 4515–4558, 2009.
LI, Z; GUO, S; LI, L; CAI, M. Effects of electromagnetic field on the batch cultivation and nutritional composition of Spirulina platensis in an air-lift photobioreactor. Bioresource Technology. v. 98, p. 700-705, 2007.
LOURENÇO, S. O. Cultivo de Microalgas Marinhas: Princípios e Aplicações. São Carlos: RiMa, 2006.
MORAIS, M. G.; COSTA, J. A. V. Isolation and selection of microalgae from coal fired thermoelectric power plant for biofixation of carbono dioxide. Energy Conversion and Management, v. 48, p. 2169-2173, 2007.
PATIL, S., AL-ZAREA, B.K., MAHESHWARI, S., SAHU, R. Comparative evaluation of natural antioxidants Spirulina and aloe vera for the treatment of oral submucous fibrosis. Journal of Oral Biology Craniofacial Research., v. 1, p. 1–5, 2015.
SALLA, A. C. V.; MARGARITES, A. C.; SEIBEL, F. I.; HOLZ, L. C.; BRIÃO, V. B.; BERTOLIN, T. E.; COLLA, L. M.; COSTA, J. A. V. Increase in the carbohydrate content of the microalgae Spirulina in culture by nutrient starvation and the addition of residues of whey protein concentrate. Bioresource Technology, v. 209, p. 133-141, 2016.
SHIRAIWA, Y., GOYAL, A., TOLBERT, N.E. Alkalization of the medium by unicellular green algae during uptake of dissolved inorganic carbon. Plant Cell Physiol. p. 649-657, 1993.
TU, R., JIN, W., XI, T., YANG, Q., HAN, S-F., ABOMOHRA, A.E-F. Effect of static magnetic field on the oxygen production of Scenedesmus obliquus cultivates in municipal wastewater. Water Research p. 1-7, 2015.
UNEP/WHO/IRPA. United Nations Environment Programme/International Radiation Protection Association/World Health Organization. Environmental Health Criteria 69: Magnetic Fields, Geneva, 1987.
VONSHAK, A. Spirulina platensis (Arthrospira): physiology, cell-biology and biotechnology. London: Taylor & Francis, 1997.
YEN, H.W., HU, C., CHEN, C.Y., HO, S.H., LEE, D.J., CHANG, J.S. Microalgae-based biorefinery – from biofuels to natural products. Bioresource Technology, v. 135, p. 166- 174, 2013.
ZARROUK, C. Contribuition à I étude d une Cyanophycée: influence de divers facteurs physiques ET chimiques sur la croissance et la photosynthèse de Spirulina maxima. Paris: Université Des Paris, 1966.
































