Otimização da produção de carotenoides por Rhodotorula mucilaginosa em meio agroindustrial com melaço e água de maceração de milho
ISBN 978-85-85905-21-7
Área
Bioquímica e Biotecnologia
Autores
Rodrigues, T. (FURG) ; D´amore, T. (FURG) ; Burkert, J. (FURG)
Resumo
A composição do meio de cultivo é um dos fatores importantes para a bioprodução de carotenoides microbianos. Portanto, o objetivo deste trabalho foi a otimização do meio para produção de carotenoides por Rhodotorula mucilaginosa aproveitando coprodutos agroindustriais como substratos alternativos. Os cultivos foram realizados em frascos agitados com 225 mL de meio, 10% de inóculo, incubados a 25°C, 150 rpm por 168 h e a composição do meio (melaço e água de maceração de milho) segundo o delineamento experimental 2². A maximização da produção de carotenoides obteve que a concentração de melaço deve ser 50 g/L e a água de maceração de milho de 3,5 g/L, e nestas condições é possível alcançar aproximadamente 1000 µg/L de carotenoides volumétricos e 8 g/L de biomassa.
Palavras chaves
Biocorante; Coproduto agroindustrial; Levedura
Introdução
Dentre os pigmentos naturais os carotenoides constituem um grupo com ampla distribuição na natureza responsáveis pela coloração (amarelo ao vermelho) de frutas, hortaliças, flores, algas, bactérias e fungos (DAMODARAN; PARKIN; FENNEMA, 2010). Possuem efeitos benéficos a saúde como a capacidade antioxidante (WANG et al., 2006), atividade pró-vitamina A e ação na redução do risco de desenvolvimento de doenças degenerativas (KIM; AHN; LEE-KIM, 2001) e cardiovasculares (RICCIONE, et al., 2009). O crescimento do mercado por alimentos mais saudáveis e benéficos a saúde, além da preocupação com a utilização de aditivos químicos nos alimentos fez com que houvesse um crescimento na produção de carotenoides obtidos naturalmente (SENSIENT, 2011). Apesar de vários micro-organismos possuírem a capacidade de biossíntese de carotenoides nem todos são industrialmente interessantes. No entanto, as leveduras se destacam pela necessidade básica de uma fonte de carbono e de nitrogênio para a biossíntese, o que é relativamente simples quando comparada a outros micro-organismos (VALDUGA et al, 2009). O gênero Rhodotorula têm sido estudado empregando-se substratos de baixo custo como fonte de nutrientes (BRANCO, 2010; SCHNEIDER et al. 2013; CHENG; YANG, 2016). Para a indústria oferece vantagens sobre os outros gêneros em termos da taxa de crescimento (MALISORN; SUNTORNSUK, 2008). O desenvolvimento de processos biotecnológicos para a produção de carotenoides visa o aumento do rendimento. No entanto um fator limitante é o custo relativamente alto destes processos. O emprego de substratos de baixo valor agregado, como os coprodutos agroindustriais se torna uma alternativa para que se minimize o custo desta produção (DAS et al., 2007). Dentre estes coprodutos o melaço de cana de açúcar tem sido utilizado como substrato para processos fermentativos. Resultante da cristalização final do açúcar, é composto por: água, açúcares em média 62%, compostos de origem orgânica e uma fração mineral composta principalmente por cálcio, magnésio, sódio e potássio (RAMBLA et al., 1999). Outro coproduto agroindustrial é a água de maceração de milho, obtida do processamento do milho, resultante da água de lavagem dos grãos (DE SOUZA, 2007). Esse coproduto é rico em carboidratos, aminoácidos, peptídeos, minerais, metais, vitaminas e fosfato. Assim, é um meio favorável aos processos fermentativos. Devido a sua composição esses coprodutos tem sido estudados como fonte de nutrientes para micro-organismos (RIVAS et al., 2004). Sendo assim, o objetivo deste trabalho foi definir as concentrações dos componentes do meio de cultivo agroindustrial (água de maceração de milho e melaço) para a maximização da produção de carotenoides por Rhodotorula mucilaginosa, através da técnica de planejamento experimental.
Material e métodos
A levedura Rhodotorula mucilaginosa isolada e identificada por Otero (2011) e depositada na Coleção de Cultura André Toselo (CCT 7668) foi utilizada. Para a reativação foi realizado repiques e incubados por 48 h a 25ºC em meio ágar extrato de malte e levedura YM (3 g/L de extrato de levedura, 3 g/L de extrato de malte, 5 g/L de peptona e 10 g/L de glicose). Após foi realizada ressuspensão celular (pré inóculo) em 1 mL de água peptonada (0,1%) e adicionada em 9 mL no meio YM por 48 h a 25ºC. O inóculo foi preparado em frascos agitados de 250 mL com 90 mL do meio de cultivo YM modificado (PARAJÓ; VÁZQUEZ, 1998), e adicionado 10 mL do pré inóculo, sendo incubado a 25°C, 150 rpm por 48 h ou tempo necessário para atingir no mínimo 1x108 células.mL-1, contadas em câmara de Neubauer (MICHELON et al., 2012). Os cultivos foram realizados em frascos agitados de 500 mL com 225 mL do meio de produção agroindustrial, o pH inicial de 6,0, acrescidos de 10% de inóculo, iniciando com 1x107 células.mL-1, a 25ºC, 150 rpm por 168 h (SILVA, 2009), sendo realizado o acompanhamento de biomassa e carotenoides a cada 24 h. A bioprodução de carotenoides foi estudada analisando os efeitos da composição do meio de cultivo agroindustrial água de maceração de milho (3,5 a 9,5 g/L ) e melaço de cana de açúcar (10 a 50 g/L ) através de um delineamento composto central 2², tendo como repostas a máxima concentração de carotenoides volumétricos em cada ensaio e neste mesmo tempo de processo a concentração de biomassa e carotenoides específicos alcançada.A concentração de biomassa ao longo do processo foi estimada pela absorbância a 620 nm, através de curva padrão previamente construída (CHOI; PARK, 2003).Para a determinação da concentração de carotenoides, a biomassa foi seca por 48 h a 35°C, posteriormente macerada com gral e pistilo e padronizada em peneira com mesh 115 (CIPOLATTI, 2012) e congeladas por 48 h a -18°C (FONSECA et al., 2011). O processo de rompimento celular com dimetilsulfóxido foi utilizado (MICHELON et al., 2012), sendo a extração feita com acetona, e o procedimento de ruptura repetido até o branqueamento total das células. Aos sobrenadantes adicionou-se 10 mL de solução de NaCl 20% (m.v-1) e 10 mL de éter de petróleo. Após a fase apolar foi filtrada com NaSO, originando os extratos carotenogênicos (MICHELON et al., 2012). A determinação da concentração de carotenoides totais nos extratos foi realizada em espectrofotômetro a 448 nm, sendo expresso em termos de seu carotenoide majoritário (CIPOLATTI, 2012), β-caroteno em éter de petróleo com absortividade específica de 2592, de acordo com Davies (1976).Os dados foram tratados com auxílio de Statistica 5.0, a 95% de nível de confiança (p < 0,05). A análise de variância foi utilizada para estimar os parâmetros estatísticos significativos para a construção de modelos empíricos codificados e as superfícies de resposta (RODRIGUES;IEMMA, 2012)
Resultado e discussão
As variáveis independentes codificadas e com os seus respectivos valores reais, concentração de melaço e concentração de água de maceração de milho, bem como as respostas avaliadas (variáveis dependentes) concentração de biomassa, carotenoides específicos e volumétricos variaram de 2,69 g/L (ensaio 1) a 8,73g/L (ensaio2), 110,8 µg/g (ensaio 9) a 177,9 µg/g (ensaio 1) e 407 µg/L (ensaio 3) a 1077 µg/L (ensaio 4), respectivamente (Figura 1).Com a finalidade da construção de modelos empíricos codificados (Equação 1 e Equação 2) para prever as respostas em função da concentração de melaço e água de maceração de milho foram realizadas análise de variância para biomassa, concentração específica e volumétrica de carotenoides (Figura 1). A Equação 1 foi descrita como Carotenoides volumétricos (µg/L) = 746,3 + 307,7xMelaço (Equação 1) e para a Biomassa (g/L)=5,72 + 2,52xMelaço (Equação 2). Em ambos os modelos os coeficientes de regressão não significativos (p>0,05) água de maceração de milho e a interação entre a água de maceração e o melaço foram adicionados ao resíduo da análise de variância. Os coeficientes de correlação da análise de variância (R) de 0,98 e 0,92, respectivamente, para carotenoides volumétricos e biomassa, foram obtidos demonstrando que os modelos propostos se ajustaram bem aos dados experimentais. Outro parâmetro avaliado foi a razão Fcalculado/Ftabelado de 22,9 para produção de carotenoides e 4,4 para biomassa, sendo assim considerados modelos preditivos, foi possível construir as superfícies de respostas (Figura 2). A concentração de carotenoides específicos não possibilitou a construção de modelos preditivos e significativos. Os desvios relativos entre os resultados experimentais e os preditos pelos modelos foram inferiores a 20% (Figura 1), demonstrando que as equações do modelo preveem bem o comportamento da produção volumétrica de carotenoides e da biomassa. O aumento da concentração da água de maceração de milho independente da concentração de melaço de cana de açúcar não influenciou na produção de carotenoides volumétricos (Figura 2a) e na concentração de biomassa (Figura 2b), conforme descrito pelas Equações 1 e 2, respectivamente. No entanto, o incremento na concentração do melaço em toda a faixa de concentração de água de maceração de milho estudada aumentou significativamente a produção carotenogênica e a biomassa microbiana.
Estes resultados estão de acordo com os ensaios 2 e 4, da Figura 1 que alcançaram as maiores produções de biomassa e carotenoides volumétricos deste estudo. Dessa forma para a maximização da produção de carotenoides a concentração de melaço deve ser 50 g/L e a água de maceração de milho de 3,5g/L, e nestas condições é possível alcançar aproximadamente 1000 µg/L de carotenoides volumétricos e 8 g/L de biomassa.
A maximização da produção de carotenoides no meio de cultivo agroindustrial proposto neste trabalho foi similar ao alcançado em meio YM (3 g/L de extrato de levedura, 3 g/L de extrato de malte, 5 g/L de peptona, 10 g/L de glicose) por Cipolatti (2012), utilizando o mesmo micro-organismo e as mesmas condições de processo, que obteve uma máxima produção de carotenoides de 1068 μg/L. Portanto, demonstrando que a utilização do meio agroindustrial, com substratos alternativos de menor valor agregado, pode viabilizar esta produção e minimizar os custos do processo.
Machado e Burkert (2015) utilizando o meio agroindustrial com 40 g/L de melaço e 6,5 g/L água de maceração de milho, nas mesmas condições de processo deste trabalho, porém, com a levedura Sporidiobolus pararoseus alcançaram 520,94 μg/L (73,19 μg/ g), resultados inferiores comparados a este trabalho com a R. mucilaginosa.
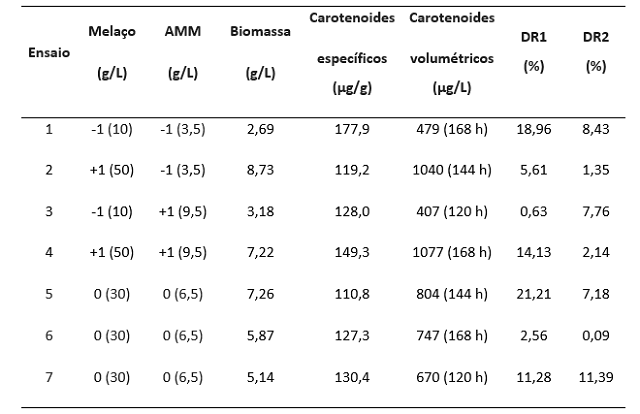
AMM= água de maceração de milho DR1= desvio relativo (%) para resposta biomassa DR2= desvio relativo (%) para resposta carotenoides volumétricos
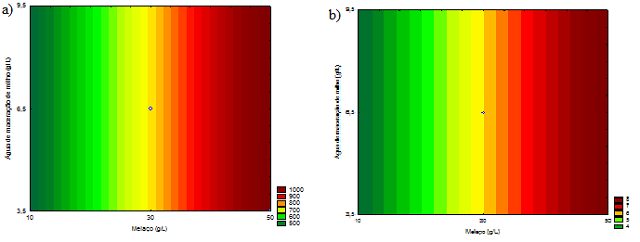
Carotenoides em µg/L (a) e biomassa em g/L (b) em função da concentração de melaço e água de maceração de milho
Conclusões
A levedura Rhodotorula mucilaginosa foi capaz de produzir carotenoides com a utilização de um meio de cultivo agroindustrial formulado com melaço e água de maceração de milho. A concentração de melaço possuiu efeito significativo na produção carotenogênica e na biomassa, no entanto a concentração de água de maceração de milho não obteve efeito significativo. A maximização da produção obteve aproximadamente 1000 µg/L em carotenoides e 8 g/L de biomassa, no meio contendo 50g/L melaço e 3,5 g/L água de maceração de milho.
Agradecimentos
Os autores agradecem aos órgãos de fomento: FURG, CNPq, CAPES, FAPERGS.
Referências
BRANCO, L. S. C. Estudo da ampliação de escala na produção de biomassa de Rhotorula sp. CNPAT02 em processo batelada para obtenção de carotenoides.2010.76f. Dissertação (Mestrado em Engenharia Química)-Universidade Federal do Ceará, Fortaleza 2010.
CHENG, Y.; YANG, C. Using strain Rhodotorula mucilaginosa to produce carotenoids using food wastes. Journal of the Taiwan Institute of Chemical Engineers, v.61, p.270-275, 2016.
CHOI, M.H.; PARK, Y.H. Production of yeast biomass using waste Chinese cabbage. Biomass & Bioenergy, v. 25, p. 221-226, 2003.
CIPOLATTI, E. P. Obtenção de carotenoides microbianos com atividade antioxidante a partir de coprodutos agroindustriais. 2012. 120f. Dissertação (Mestrado em Engenharia e Ciência de Alimentos) – Universidade Federal do Rio Grande, Rio Grande, 2012.
DAMODARAM, S.; PARKIN, K. L.; FENNEMA, O. R. Química de Alimentos de Fennema. 4.ed. Porto Alegre: Artmed, 2010.
DAS, A., YOON, S., LEE, S., KIM, J., OH, D., KIM, S. An update on microbial carotenoid production: application of recent metabolic engineering tools. Applied Microbiology and Biotechnology, v.77, p.505–512, 2007.
DAVIES, B. H. Chemical Biochemistry Plant Pigments. GOODWIN, T. W., Academic Press: New York, 1976.
DE SOUZA SOBRINHO, H. B. Utilização de resíduos industriais como substratos de baixo custo para a produção de biossurfactante por Candida sphaerica. 2007. 98f. Dissertação (Mestrado em Desenvolvimento de Processos Ambientais). Universidade Federal do Recife. Recife, 2007.
FONSECA, R. A. S.; RAFAEL, R. S.; KALIL, S. J.; BURKERT, A.V.; BURKERT, J. F. M. Different cell disruption methods for astaxanthin recovery by Phaffia rhodozyma. African Journal of Biotechnology, v.10, p.1165-1171, 2011.
MACHADO, W. R. C.; BURKERT, J. F. M. Optimization of agroindustrial medium for the production of carotenoids by wild yeast Sporidiobolus pararoseus. African Journal of Microbiology Research, v. 9, p. 209-219, 2015.
MALISORN, C.; SUNTORNSUK, W. Improved β-carotene production of Rhodotorulaglutinis in fermented radish brine by continuous cultivation. Biochemical Engineering Journal, v.43, p. 27-32, 2008.
MICHELON, M.; BORBA, T. M.; RAFAEL, R. S.; BURKERT, C. A. V.; BURKERT, J. F. de M. Extration of carotenoids from Phaffia rhodozyma: A comparison between different techniques of cell disruption. Food Science and Biotechnology, v. 21, n. 1, p. 1-8; 2012.
OTERO, D. M. Bioprospecão de leveduras silvestres produtoras de carotenoides. 2011. 76 f. Dissertação (Mestrado em Engenharia e Ciência de Alimentos) – Universidade Federal do Rio Grande, Rio Grande, 2011.
PARAJÓ, J. C. V. S., VÁZQUEZ, M. Optimization of carotenoid production by Phaffia rhodozyma cell grown on xylose. Process Biochemestry, v. 33, n. 2, p. 181-187, 1998.
RAMBLA, M. A. O.; PRADA, A. R.; COOPAT, T. S.; CARRACEDO, G. B. Méis. Manual dos derivados da cana-de-açúcar. Instituto Cubano de Pesquisas dos Derivados da Cana-de-açúcar. Cap. 2.4, p. 49-55. 1999.
RIVAS, B.; MOLDES, A. B.; DOMÍNGUEZ, J. M.; PARAJÓ, J. C. Development of culture media contining spent yeast cells of Debaryomyces hansenii and corn steep liquor for lactic acid production with Lactobacillus rhamnosus. International Jounal of Food Microbiology, v. 97, p. 93-98, 2004.
RODRIGUES, M. I.; IEMMA, A. F. Planejamento de Experimentos e Otimização de processos: uma estratégia seqüencial de planejamentos. Campinas: Casa do Pão Editora, 2012.
SCHNEIDER, T.; GRAEFF-HONNINGER, S.; FRENCH, W.T.; HERNANDEZ, R.; MERKT, N. Lipid and carotenoid production by oleaginous red yeast Rhodotorula glutinis cultivated on brewery effluents. Energy, v. 61, p.34-43, 2013.
SENSIENT. A nova tendencia no mercado de corantes . Food Ingredients Brasil, v.18, 2011.
SILVA, D. A. Maximização da produção de astaxantina por Phaffia rhodozyma utilizando água de parboilização do arroz. 2009. 93f. Dissertação (Mestrado em Engenharia e Ciência de Alimentos) – Universidade Federal do Rio Grande, Rio Grande, 2009.
VALDUGA, E.; TATSCH, P. O.; TIGGEMANN, L.; TREICHEL, H.; TONIAZZO, G.; ZENI, J.; LUCCIO, M. Produção de carotenoides: microrganismos como fonte de pigmentos naturais. Química Nova, v. 32, p. 2429-2436, 2009.
WANG, M.; TSAO, R.; ZHANG, S.; DONG, Z.; YANG, R.; GONG, J.; PEI, Y. Antioxidant activity, mutagenicity/anti-mutagenicity, and clastogenicity/anti-clastogenicity of lutein from marigold flowers. Food Chemistry Toxicology, v. 44, p.1522-1559, 2006.
KIM, M.; AHN, S.; LEE-KIM, Y. Relationship of serum α-tocopherol, carotenoids and retinol with the risk of breast cancer. Nutrition Research, V. 21, P.797-809, 2001.
RICCIONE, G.; ORAZIO, N.; PALUMBO N.; BUCCIARELLI, V. ILIO, E., BAZZANO, L. Relationship between plasma antioxidant concentrations and carotid intima-media thickness: the: Asymptomatic Carotid Atherosclerotic Disease in Manfredonia Study . European Journal of Preventive Cardiology, v.16, p. 351–357, 2009.
































