CARACTERIZAÇÃO QUÍMICA DE UM EXOPOLISSACARÍDEO PRODUZIDO POR BACTÉRIA DO GÊNERO Mesorhizobium A PARTIR DE GLICEROL RESIDUAL
ISBN 978-85-85905-21-7
Área
Bioquímica e Biotecnologia
Autores
Oliveira, J.M. (FURG) ; Amaral, S.A. (FURG) ; Burkert, C.A.V. (FURG)
Resumo
Estudos recentes têm mostrado que as bactérias diazotróficas são capazes de utilizar resíduos industriais como fonte de carbono e produzir exopolissacarídeos (EPS). Este trabalho teve como objetivo caracterizar quimicamente o EPS produzido pela bactéria Mesorhizobium loti Semia 816, a partir de glicerol residual como fonte de carbono. O EPS em estudo apresentou teores de proteínas superiores aos encontrados na gelana e xantana, enquanto que o teor de ácidos urônicos e açúcares totais foram similares ao encontrado para xantana. Na determinação de cinzas, os biopolímeros não apresentaram diferença significativa entre si.
Palavras chaves
bactérias diazotróficas; polissacarídeos; biopolímeros
Introdução
Os polissacarídeos atualmente mais estudados são os de origem microbiana, devido algumas vantagens de obtenção em relação às outras gomas, visto que são independentes das condições climáticas, são produzidos em condições controladas, há possibilidade de utilização de matérias-primas regionais, há maior rapidez na obtenção do produto acabado e necessidade de espaço relativamente pequeno (FREITAS; ALVES; REIS, 2011). Devido à grande diversidade de suas propriedades, os exopolissacarídeos (EPS) de origem microbiana podem ser aplicados em diversos segmentos industriais. Nessas pesquisas, uma grande diversidade de estruturas de EPS microbianos foi relatada, mas a produção industrial foi consolidada apenas para alguns, nomeadamente goma xantana, levana, dextrana e pululana (FREITAS et al., 2011; MOSCOVICI, 2015). Esses polissacarídeos apresentam uma maior variedade de estruturas e propriedades físico-químicas, sendo aplicados em diversas áreas, como alimentos, farmacêutica, petrolífera, cosmética, têxtil, de tintas, produtos agrícolas, entre outras. Dependendo de sua estrutura química, algumas aplicações podem incluir seu uso como emulsificantes, estabilizantes, ligantes, agentes gelificantes, coagulantes, lubrificantes, formadores de filmes, espessantes e agentes suspensores (DONOT et al., 2012; FARIA et al., 2011; SILVA et al., 2009). Outros micro-organismos são capazes de sintetizar e secretar polissacarídeos, destacando-se as bactérias diazotróficas da família Rhizobiaceae, constituída pelo gênero Rhizobium, Sinorhizobium, Mesorhizobium, Bradyrhizobium e Azorhizobium (CASTELLANE, 2011; FRIZZO, 2007; MONTEIRO et al., 2012). Os rizóbios são bactérias do solo que são capazes de estabelecer uma simbiose fixadora de nitrogênio com plantas da família das leguminosas (PROMÉ et al., 2002), e que nos últimos anos são o tema de muitas pesquisa cientificas (FRIZZO, 2007; KUMAR; MODY; JHA, 2007; CASTELLANE, 2011; CASTELLANE; LEMOS, 2016; MONTEIRO et al., 2012; RIBEIRO, 2015). A estrutura, composição, biossíntese e propriedades funcionais dos polissacarídeos extracelulares podem variar dependendo da cepa utilizada, do substrato e das condições de produção (FREITAS; ALVES; REIS, 2011; SILVA et al., 2009). A maioria dos processos de produção emprega preferencialmente glicose e sacarose como fontes de carbono na elaboração dos meios de produção. Porém, o emprego de matérias-primas como subprodutos ou rejeitos agroindustriais, pode não só reduzir custos do processo, como minimizar os problemas ambientais. Conforme pesquisas desenvolvidas nos últimos anos, o glicerol possui como componente principal carbono de fácil assimilação (ROSA et al., 2015; MACHADO JR. et al., 2015; SPIER; BUFFON; BURKERT, 2015; RIOS et al., 2015; SILVA et al., 2016; RIBEIRO, 2015; TRINDADE; MUNHOZ; BURKERT, 2015). A caracterização dos EPS microbianos é importante na definição da aplicação desses biopolímeros, diante disto o objetivo deste trabalho foi caracterizar quimicamente o exopolissacarídeo produzido pela bactéria Mesorhizobium loti Semia 816 a partir glicerol residual.
Material e métodos
Os experimentos foram realizados no Laboratório de Engenharia de Bioprocessos da Universidade Federal do Rio Grande (FURG). Foi utilizada a bactéria Mesorhizobium loti Semia 816. Como fonte de carbono foi utilizado o glicerol residual proveniente de uma indústria de biodiesel localizada no Rio Grande do Sul. Para fins de comparação, foram utilizadas as gomas gelana e xantana. Inóculo, cultivo e recuperação do EPS: O inóculo foi preparado partindo de um tubo contendo a cultura microbiana, sendo raspada com 10 mL de água peptonada 0,1%, transferindo para o meio YMA contendo (g/L): 10 manitol; 0,1 K2HPO4; 0,4 KH2PO4; 0,2 MgSO47H20; 0,1 NaCl; 0,4 extrato de levedura (STAUDT; WOLFE; SHROUT, 2012). Incubou-se a 30°C e 200 rpm até atingir a densidade ótica (DO) de 0,8 a 600 nm. O cultivo foi realizado com o meio com a seguinte a composição (g/L): 12,2 glicerol residual; 0,4 fosfato de potássio monobásico; 0,1 fosfato de potássio dibásico; 0,2 sulfato de magnésio hepta-hidratado; 0,1 cloreto de sódio; 0,4 extrato de levedura; 0,12 cloreto de manganês tetra-hidratado; 0,15 cloreto de cálcio di-hidratado; pH ajustado em 7,0. O cultivo foi conduzido em frascos agitados a 30°C e 200 rpm (RIBEIRO, 2015). A recuperação do EPS foi realizada através da centrifugação a 13.000 x g por 30 min a 4ºC para remoção de células, seguida de precipitação do EPS pela adição de álcool etílico 96% (1:3 v/v). Após 24 h a ± 4ºC, centrifugou-se novamente a 13.000 x g por 15 min. O EPS foi dialisado (limite de exclusão de 12.000 Da) por 72 h a 4°C e liofilizado (RIBEIRO, 2015). Caracterização química: Foi realizada a caracterização química do EPS produzido, como também das gomas gelana e xantana. O conteúdo de açúcares totais foi determinado através do método fenol-ácido sulfúrico (DUBOIS; GILLES; HAMILTON, 1956). A concentração do teor de açúcares foi determinada através de uma curva padrão de glicose. O conteúdo de proteínas totais foi determinado através do método de Kjeldahl (Método 920.87), segundo AOAC (2003), utilizando o fator 6,25. A dosagem de ácidos urônicos foi realizada pelo método colorimétrico descrito por Filisetti-Cozzi e Carpita (1991). A quantificação foi realizada com o auxílio de uma curva padrão de ácido glicurônico dentro da faixa de linearidade do método (0,97 a 38,8 μg/400μL de ácido urônico). O conteúdo de umidade foi determinado usando a metodologia da AOAC (2003), Método 925.10. Os teores de cinzas do EPS e das gomas comerciais foram determinados por incineração em mufla (AOAC, 2000). As determinações utilizando o EPS rizobiano e as gomas xantana e gelana foram realizadas em triplicata, sendo os dados tratados por análise de variância e teste de Tukey (MONTGOMERY, 2004), a fim de verificar a existência de diferenças significativas entre os polissacarídeos, a 95% de confiança (p ≤ 0,05). O tratamento estatístico dos dados foi feito com o software Statistica 5.0.
Resultado e discussão
A quantificação dos açúcares totais, proteínas solúveis e cinzas do EPS
recuperado é apresentada na Tabela 1, bem como das gomas comerciais xantana
e gelana, para fins de comparação.
Os teores de açúcares totais do EPS produzido neste trabalho com o processo
de diálise apresentou valor de 82,54% em base seca, conforme apresentado na
Tabela 1, não havendo diferença significativa (p>0,05) em relação à goma
xantana (87,78%), mas diferindo significativamente (p<0,05) em relação à
goma gelana (91,03%). Entretanto, a goma gelana não apresentou diferença
significativa (p>0,05) em relação à xantana comercial.
Monteiro et al. (2012) encontraram teores de açúcares totais de 85% e 80%
para EPSs produzidos por Rhizobium e Mesorhizobium,
respetivamente. Já Aranda-Selverio et al. (2010) encontraram um teor de
carboidratos em torno de 94,6% e 87% para Rhizobium tropici e
Mesorhizobium, respectivamente. Zhou et al. (2014) estudaram a
produção de EPSs pela bactéria Rhizobium radiobacter S10 e
encontraram um teor de açúcares de 84,5%.
Em relação ao teor de proteínas totais (Tabela 1), o EPS em estudo
apresentou 11,31% em base seca, diferindo significativamente (p<0,05) das
gomas xantana (5,04%) e gelana (3,23%). O mesmo foi verificado por Ribeiro
(2015), ao encontrar 11,31% de proteínas totais no EPS produzido pela
bactéria Mesorhizobium loti Semia 816.
Na determinação de cinzas, os biopolímeros não apresentaram diferença
significativa entre si (p>0,05). O EPS sintetizado pela bactéria em estudo
apresentou teor de cinzas de 5,99%, não diferindo (p>0,05) do encontrado
para goma gelana comercial (5,44%) bem como do apresentado pela xantana
comercial, que apresentou um valor de 6,85% de cinzas. Zhou et al. (2014)
determinaram um teor de cinzas de 0,32% no EPS de Rhizobium
radiobacter S10.
Assim como a maioria dos EPSs produzidos por rizóbios, descritos na
literatura (CASTELLANE et al., 2015; MONTEIRO et al., 2012; MORETTO et al.,
2015), foi possível observar um valor considerável de ácidos urônicos.
Diferença significativa (p<0,05) foi observada entre o EPS produzido e a
goma gelana, sendo encontrado teor de ácidos urônicos de 3,90±0,19% e
1,80±0,75%, respectivamente. Já quando comparado com a goma xantana
(3,50±0,12%), não houve diferença significativa entre si (p>0,05).
Castellane et al. (2015) encontraram, avaliando a composição de
monossacarídeos de Rhizobium tropici 4077 e mutante 4077, valores de
4,58% e 0,08%, e 7,18% e 0,06%, respectivamente, para ácido glicurônico e
galacturônico. Monteiro (2011), ao caracterizar estruturalmente
polissacarídeos produzidos por bactérias dos gêneros Rhizobium e
Mesorhizobium, encontrou teores de ácido urônico entre 0,8 e 12,7%.
Moretto et al. (2015), na determinação da composição em monossacarídeos do
EPS produzido por Rhizobium EPSLBMP-C04, encontraram quantidade de
ácido glicurônico de 3,57%, e para Rhizobium EPSLBMP-C02 foi
encontrado 10% de ácido galacturônico e traços de ácido glicurônico.
A presença de ácidos urônicos foi, desta forma, constatada para o EPS
produzido pela bactéria Mesorhizobium lotti Semia 816. A presença de
ácidos urônicos determina o caráter polianiônico da maioria dos EPSs
microbianos, promovendo assim alterações na sua conformação molecular e
aumentando a sua solubilidade (DIAZ; VENDRUSCOLO; VENDRUSCOLO, 2004;
RADCHENKOVA et al., 2013).
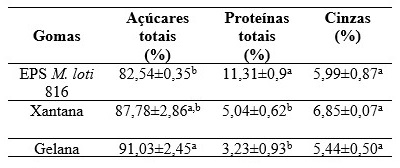
*Valores (médias ± desvio padrão) com letras minúsculas diferentes na mesma coluna apresentam diferença significativa (p<0,05).
Conclusões
O EPS sintetizado pela bactéria Mesorhizobium loti Semia 816, recuperado por precipitação, dialisado e liofilizado, é constituído principalmente por carboidratos (82,54%), apresentando um teor considerável de ácidos urônicos (3,90%), similar ao encontrado na goma xantana, o qual deve influenciar diretamente em suas propriedades, pois torna o EPS altamente aniônico. Além disso, apresentou 11,31% de proteínas, superior aos valores encontrados para as gomas xantana e gelana, a qual pode contribuir para algumas propriedades, como a capacidade emulsificante. Quanto ao teor de cinzas, não diferiram entre si.
Agradecimentos
Os autores agradecem à FURG, CAPES, CNPq e FAPERGS.
Referências
AOAC, Official Methods of Analysis.17th ed. Gaithersburg, MD: Association of Official Analytical Chemists, 2003. CD-ROM.
AOAC, Official Methods of Analysis, 17th ed. Washington, DC: Association of Official Analytical Chemists, 2000. CD-ROM.
ARANDA- SELVERIO, G.; PENNA, A. L. B.; CAMPOS-SÀ, L. F.; JUNIOR, O. S.;
VASCONCELOS, A. F. D.; SILVA, M. L. C.; LEMOS, E. G. M.; CAMPANHARO, J. C.; SILVEIRA, J. L. M. Propriedades reológicas e efeito da adição de sal na viscosidade de exopolissacarídeos produzidos por bactérias do gênero Rhizobium. Química Nova, v. 33, p. 895-899, 2010.
CASTELLANE, T. C. L. Obtenção e avaliação de mutantes exoz- e phbab- envolvidos no metabolismo de polímeros de carbono em Rhizobium tropici Semia 4080 com potencial biotecnológico. 2011. 115 f. Tese (Doutorado em Agronomia) - Universidade Estadual Paulista “Julio de Mesquita Filho”, Faculdade de Ciências Agrarias e Veterinárias, Campus de Jaboticabal, Jaboticabal, São Paulo - SP.
CASTELLANE, T. C. L.; LEMOS, E. G. M. Determinação da massa molecular de exopolissacarídeos produzidos por estirpe mutante de Rhizobium tropici. Ciencia & Tecnologia: FATEC-JB, v. 8, Edição Especial, 2016.
CASTELLANE, T. C. L.; PERSONA, M.R.; CAMPANHARO, J. C.; LEMOS, E. G. M. Production of exopolysaccharide from rhizobia with potential biotechnological and bioremediation applications. International Journal of Biological Macromolecules, v. 74, p. 515-522, 2015.
DIAZ, P. S.; VENDRUSCOLO, C. T.; VENDRUSCOLO, J. L. S. Reologia de xantana: Uma revisão sobre a influência de eletrólitos na viscosidade de soluções aquosas de gomas xantana. Semina: Ciências Exatas e Tecnológicas, v. 25, n.1, p. 15-28, 2004.
DONOT, F.; FONTANA, A.; BACCOU, J.C.; SCHORR-GALINDO, S. Microbial exopolysaccharides: Main examples of synthesis, excretion, genetics and extraction. Carbohydrate Polymers, v. 87, p. 951–962, 2012.
DUBOIS, N.; GILLES, K. A.; HAMILTON, J. K.; REBERS, P. A.; SMITH, F. Colorimetric method for determination of sugar and related substances. Analytical Chemistry, v. 28, p. 350-356, 1956.
FILISETTI-COZZI, T. M. C. C.; CARPITA, N. C. Measurement of uronic acids without interference from neutral sugars. Analytical Biochemistry, v. 197, p.157-162, 1991.
FREITAS, F.; ALVES, V. D.; REIS, M. A. M. Advances in bacterial exopolysaccharides: From production to biotechnological applications. Trends in Biotechnology, v. 29, p. 388-398, 2011.
FREITAS, F.; ALVES, V. D.; TORRES, C. A. V.; CRUZ, M.; SOUSA, I.; MELO, M. J.; RAMOS, A. M.; REIS, M. AM.. Fucose-containing exopolysaccharide produced by the newly isolated Enterobacter strain A47 DSM 23139. Carbohydrate Polymers, v. 83, p. 159-165, 2011.
FRIZZO, M. L. S. Seleção e caracterização de rizóbios nativos, de solos do Rio Grande do Sul, para Lotus corniculatus l. e Lotus uliginosus schkuhr. 2007. 81 f. Dissertação (Mestrado em Ciência do Solo)- Universidade Federal do Rio Grande do Sul (UFRGS), Porto Alegre- RS.
KUMAR, A. S.; MODY, K.; JHA B. Bacterial exopolysaccharide – A perception. Journal of Basic Microbiology, v. 47, p. 103-117, 2007.
MACHADO JR, F. R. S.; MICHELON, M.; DALCANTON, F.; FURLONG, E. B.; BURKERT, J. F. M.; BURKERT, C. A. V. Biomass production by Yarrowia lipolytica as a source of lipids: Bench scale cultivation on raw glycerol-based medium. International Food Research Journal, v. 22, n. 3, p. 1253-1260, 2015.
MONTEIRO, N. K. Caracterização estrutural de polissacarídeos produzidos por bactérias dos gêneros Rhizobium e Mesorhizobium. 2011. 98 f. Dissertação (Mestrado em Engenharia e Ciência de Alimentos) - Universidade Estadual Paulista “Júlio de Mesquita”, Campus São José do Rio Preto, São José do Rio Preto - SP.
MONTEIRO, N. K.; EXPOSTI, D. T. D.; SILVA, M. L. C.; LEMOS, E. G. M.; CAMPANHARO, J. C.; SILVEIRA, J. L. M. Caracterização química dos géis produzidos pelas bactérias diazotróficas Rhizobium tropici e Mesorhizobium sp. Química Nova, v. 35, n. 4, p.705-708, 2012.
MONTGOMERY, D. C. Introdução ao controle estatístico de qualidade. 4.ed. Rio de Janeiro: Ed LTC, 2004. 512 p.
MORETTO, C.; CASTELLANE, T.C.L.; LOPES, E.M.; OMORI, W.P.; SACCO, L.P.; LEMOS, E.G.M. Chemical and rheological properties of exopolysaccharides produced by 178 four isolates of rhizobia. International Journal of Biological Macromolecules, v. 81, p. 291– 298, 2015.
MOSCOVICI, M. Present and future medical applications of microbial exopolysaccharides. Frontiers in Microbiology, v. 6, 2015.
PROMÉ, J. C.; FERRO, M.; DEBELLÉ, F.; PROMÉ, D.; KRISNAN, H. B. The pivotal role of tandem mass spectrometry in structural determinations of nod factors produced by Rhizobia. Nod factors produced by wild-type strains of Mesorhizobium huakii and Rhizobium sp. mus10. International Journal of Mass Spectrometry, v. 219, p. 703-716, 2002.
RADCHENKOVA, N.; VASSILEV, S.; PANCHEV, I.; ANZELMO, G.; TOMOVA, I.; NICOLAUS, B.; KUNCHEVA, M.; PETROV, K.; KAMBOUROVA, M. Production and properties of two novel exopolysaccharides synthesized by a thermophilic bacterium Aeribacillus pallidus 418. Applied Biochemistry and Biotechnology, v. 171, p. 31-43, 2013.
RIBEIRO, V. A. Produção e caracterização de exopolissacarídeos a partir de bactérias diazotróficas cultivadas em meios à base de glicerol residual. 2015. 192 f. Tese (Doutorado em Engenharia e Ciência de Alimentos) – Escola de Química de Alimentos, Universidade Federal de Rio Grande (FURG), Campus de Rio Grande, Rio Grande – RS.
RIOS, D. A. S.; BORBA, T. M.; KALIL, S. J.; BURKERT, J. F. M. Rice parboiling wastewater in maximization of carotenoids bioproduction by Phaffia rhodozyma. Ciência e Agrotecnologia, v. 39, p. 401-410, 2015.
ROSA, C. F. C.; MICHELON, M.; BURKERT, J. F. M.; KALIL, S. J.; BURKERT, C. A. V. Effect of medium composition on changes of surface tension during cultivation of Pseudomonas aeruginosa LBM10 growing on glycerol. International Journal of Engineering Research and Applications, v. 5, n. 4, p. 41-46, 2015.
SILVA, M. F.; FORNARI, R. C. G.; MAZUTTI, M. A.; OLIVEIRA, D.; PADILHA, F. F.; CICHOSKI, A. J.; CANSIAN, R. L.; DI LUCCIO, M.; TREICHEL, H. Production and characterization of xantham gum by Xanthomonas campestris using cheese whey as sole carbon source. Journal of Food Engineering, v. 90, p. 119-123, 2009.
SILVA, C. M.; BORBA, T. M.; KALIL, S. J.; BURKERT, J. F. M. Raw glycerol and parboiled rice effluent for carotenoid production: Effect of the composition of culture medium and initial pH. Food Technology and Biotechnology, v. 54, p. 489-496, 2016.
SPIER, F.; BUFFON, J. G.; BURKERT, C. A. V. Bioconversion of raw glycerol generated from the synthesis of biodiesel by different oleaginous yeasts: Lipid content and fatty acid profile of biomass. Indian Journal of Microbiology, v. 55, p. 415-422, 2015.
STAUDT , A.K.; WOLFE, L.G., SHROUT, J.D. Variations in exopolysaccharide production by Rhizobium tropici. Archives of Microbiology, v. 194, p. 197–206, 2012.
TRINDADE, A. R.; MUNHOZ, P. A.; BURKERT, V. A. C. Raw glycerol as an alternative carbon source for cultivation of exopolysaccharide-producing bacteria. Journal of Applied Biotechnology, v. 3. n. 2. p. 61-73, 2015.
ZHOU, F.; WU, Z.; CHEN, C.; HAN, J.; AI, L.; GUO, B. Exopolysaccharides produced by Rhizobium radiobacter S10 in whey and their rheological properties. Food Hydrocolloids, v. 36, p. 362-368, 2014.
































