Biocatálise de caseína de leite bovino por protease tratada em líquido iônico e acetona
ISBN 978-85-85905-21-7
Área
Bioquímica e Biotecnologia
Autores
Blumberg Machado, T. (UNIVERSIDADE FEDERAL DO RIO GRANDE) ; Furtado Prestes, C. (UNIVERSIDADE FEDERAL DO RIO GRANDE) ; de Matos de Borba, T. (UNIVERSIDADE FEDERAL DO RIO GRANDE) ; Brandelli, A. (UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL) ; Juliano Kalil, S. (UNIVERSIDADE FEDERAL DO RIO GRANDE)
Resumo
A caseína pode ser hidrolisada por ação catalítica de proteases, gerando peptídeos bioativos. Este estudo visou empregar uma protease oriunda de Bacillus sp. P45 tratada no líquido iônico (LI) [Emim][Tf2N] e acetona (1:1, v/v) na hidrólise da caseína em meio aquoso. A reação foi monitorada, através do método pH-stat, quantificando o grau de hidrólise (GH) das ligações peptídicas. O GH na reação catalisada pela protease tratada em LI e acetona não foi favorável na hidrólise de caseína, pois apresentou um GH 1,8 vezes menor que a enzima padrão solubilizada em tampão. Em vista dos resultados, futuros estudos devem ser conduzidos, reduzindo a concentração de LI e/ou aplicando a enzima nesta condição para outros tipos de processos biocatalíticos com uso de solventes orgânicos.
Palavras chaves
Hidrólise; Processo enzimático; pH stat
Introdução
Caseínas são frações proteicas do leite (WALSTA; JENNESS, 1984), usadas na indústria de alimentos como agente emulsificante, ligante com água e gelificante (ALVAREZ et al, 2007). Em vista do baixo valor destas proteínas, seu uso para obtenção de peptídeos bioativos é atrativo (CERVATO; CAZZOLA; CESTARO, 1999), sendo que o processo é usualmente por hidrólise enzimática (DAROIT et al, 2012, HIDALGO et al, 2015). As proteases catalisam a clivagem das ligações peptídicas de proteínas e estão disponível na natureza e/ou podem ser obtidas por fonte microbiana. Proteases possuem diversas aplicações na indústria química, farmaceutica e de alimentos (GUPTA; RAMNANI, 2006), adicionalmente estão sendo empregadas na hidrólise de alimentos proteicos para liberar peptídeos bioativos presos na estrutura da proteína (SARMADI; ISMAIL, 2010). Líquidos iônicos (LI) são sais fundidos que vem sendo estudados como estabilizantes de enzimas (DANG et al, 2007) e meios reacionais (HERNÁNDEZ- FERNANDEZ et al, 2009, YANG et al, 2010). Como meio reacionais, geralmente os LIs são empregados como substitutos dos solventes orgânicos (SO), porém recentemente a mistura de LI e SO foi empregada (NASCIMENTO et al, 2015). A protease oriunda do Bacillus sp. P45 foi estabilizada no LI [Emim] [Tf2N], mantendo 80% da atividade após incubada a 55ºC por 144 h. Além disso, a adição de acetona à protease em LI 1:1 (v/v) proporcionou aumento de 91% da atividade enzimática em relação a protease somente no LI (BORBA, 2015). Em vista da capacidade estabilizante dos líquidos iônicos e seu emprego em reações, o objetivo do trabalho foi quantificar a hidrólise de caseína de leite bovino (CLB) através do parâmetro GH em meio aquoso catalisado por protease tratada no LI [Emim][Tf2N] e acetona.
Material e métodos
A protease foi sintetizada pela bactéria Bacillus sp. P45 em cultivo submerso e parcialmente purificada por sistema aquoso bifásico integrado a diafiltração (SALA et al, 2014). A atividade proteolítica foi determinada com o substrato azocaseína a 40ºC conforme Daroit, Côrrea e Brandelli (2009). As hidrólises foram conduzidas em reatores encamisados de 100 mL utilizando a protease P45 (2 mL, 600 U/g de proteína), como biocatalisador, na hidrólise da caseína de leite bovino 3,5% (m/v). O potencial de catálise foi estudado no meio aquoso em duas condições de uso da protease: solubilizada em tampão Tris- HCl 100 mmol/L pH 7,5 (condição 1; padrão) e tratada no líquido iônico [Emim] [Tf2N] e adicionada de acetona 1:1 v/v (condição 2). O tratamento da protease na condição 2 consistiu em uma homogeneização com o LI sob agitação magnética a 4ºC por 30 min. A reação foi monitorada utilizando-se o método pH-stat (ADLER-NISSEN, 1986), titulando-se continuamente com hidróxido de sódio 0,2 mol/L de modo a manter o pH constante. Os parâmetros de reação foram pH 7,5, 40ºC, reator com 73 mL de meio por 8 h (condição 1) e 5,5 h (condição 2). A ruptura das ligações peptídicas foram quantificadas através do percentual do grau de hidrólise, que é dependente do volume de hidróxido de sódio consumido durante a hidrólise, da normalidade da base, do grau de grupamento amino liberados pela hidrólise, da massa de proteína do substrato CLB e do número total de ligações peptídicas por unidade de massa (ADLER-NISSEN, 1986).
Resultado e discussão
A Figura 1 apresenta o grau de hidrólise do substrato caseína ao longo do
tempo. No meio aquoso contendo a enzima em LI e acetona o GH foi de 3,89% após
5,5 h de reação. Porém, o ensaio padrão foi superior ao ensaio testado com
valor de GH igual 6,93% em 8 h, o maior percentual indicou maior número de
ligações peptídicas rompidas, que provavelmente originam peptídeos de menor
tamanho.
A diferença nos valores de GH foi causado pelo tratamento da protease. O
contato do LI pode ter proporcionado a formação de um recobrimento na
superfície da protease (LEE; KIM, 2002), tornando-a estável, mas provavelmente
gerou uma mudança na estrutura impossibilitando o substrato ter acesso ao
sítio ativo da molécula. A atividade catalítica em LIs não segue uma regra
(FISCHER; MUTSCHLER; ZUFFERREY, 2011), enquanto algumas enzimas são ativadas
(DANG et al, 2007), outras são desestabilizadas (ATTRI; VENKATESU; KUMAR,
2011).
Outra causa pode ter sido a troca de íons do LI com a solução alcalina,
utilizada para o controle de pH e na manutenção das funções catalíticas da
protease (FISCHER; MUTSCHLER; ZUFFERREY, 2011), o que pode ter ocasionado
mudanças das propriedades do LI e menor eficiência catalítica.
Daroit et al (2012) e Hidalgo et al (2015) hidrolisaram caseinato ovino e
caseinato de sódio bovino, respectivamente, catalisados por proteases
tamponadas, quantificando o GH pela metodologia do ácido 2,4,6-trinitrobenzeno
sulfônico (TNBS). No primeiro estudo foi obtido um GH de 5,5% e no segundo, GH
de 8,2% após 7 horas de reação. Assim, foi verificado que o resultado do
estudo está na mesma ordem de grandeza, porém novas investigações fazem-se
necessárias para avaliar a aplicação da protease tratada em outros processos
como para a síntese de peptídeos.
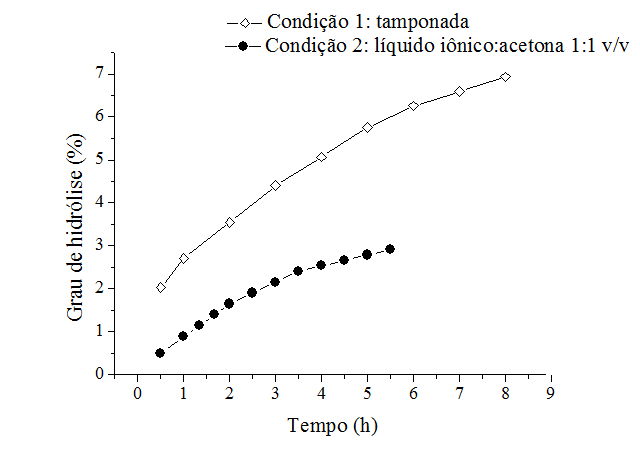
Grau de hidrólise nos ensaios de caseína de leite bovino para as duas condições de uso da protease.
Conclusões
A partir dos resultados apresentados neste estudo pode-se concluir que a protease homogeneizada em líquido iônico e acetona não foi eficaz em catalisar a hidrólise de CLB, pois apresentou o GH de 3,89% após 5,5 horas de reação, enquanto que o ensaio padrão obteve 6,93% em 8 horas. Futuras investigações são necessárias para avaliar o uso da protease nesta condição que possibilitem o desenvolvimento de novos processos biocatalíticos em LI.
Agradecimentos
A Capes, CNPq e FAPERGS-PROBIC.
Referências
ADLER-NISSEN, J. Enzymic hydrolysis of food proteins. Elsevier Applied Science Publishers, 1986. ISBN 0853343861.
ALVAREZ, E. M.; RISSO, P. H.; GATTI, C. A.; BURGOS, M.; SALA, V. S. Calcium-induced aggregation of bovine caseins: effect of phosphate and citrate. Colloid and Polymer Science, v. 285, n. 5, p. 507-514, 2007.
ATTRI, P.; VENKATESU, P.; KUMAR, A. Activity and stability of α-chymotrypsin in biocompatible ionic liquids: enzyme refolding by triethyl ammonium acetate. Physical Chemistry Chemical Physics, v. 13, n. 7, p. 2788-2796, 2011.
BORBA, T. D. M. D. Aplicação de líquidos iônicos: estabilidade e propriedades catalíticas de protease queratinolítica. 2015. 62 (Dissertação). Universidade Federal do Rio Grande, Rio Grande.
CERVATO, R. C., BENVENUTO CESTARO, GIOVANNA. Studies on the antioxidant activity of milk caseins. International Journal of Food Sciences and Nutrition, v. 50, n. 4, p. 291-296, 1999.
DANG, D. T.; HA, S. H.; LEE, S.-M.; CHANG, W.-J.; KOO, Y.-M. Enhanced activity and stability of ionic liquid-pretreated lipase. Journal of Molecular Catalysis B: Enzymatic, v. 45, n. 3, p. 118-121, 2007.
DAROIT, D. J.; CORRÊA, A. P. F.; BRANDELLI, A. Keratinolytic potential of a novel Bacillus sp. P45 isolated from the Amazon basin fish Piaractus mesopotamicus. International Biodeterioration & Biodegradation, v. 63, n. 3, p. 358-363, 2009.
DAROIT, D. J.; CORRÊA, A. P. F.; CANALES, M. M.; COELHO, J. G.; HIDALGO, M. E.; TICHOTA, D. M.; RISSO, P. H.; BRANDELLI, A. Physicochemical properties and biological activities of ovine caseinate hydrolysates. Dairy Science & Technology, v. 92, n. 4, p. 335-351, 2012.
FISCHER, F.; MUTSCHLER, J.; ZUFFEREY, D. Enzyme catalysis with small ionic liquid quantities. Journal of Industrial Microbiology & Biotechnology, v. 38, n. 4, p. 477-487, 2011.
GUPTA, R.; RAMNANI, P. Microbial keratinases and their prospective applications: an overview. Applied Microbiology and Biotechnology, v. 70, n. 1, p. 21-33, 2006.
HERNÁNDEZ‐FERNÁNDEZ, F.; DE LOS RIOS, A.; TOMÁS‐ALONSO, F.; GOMEZ, D.; VÍLLORA, G. Stability of hydrolase enzymes in ionic liquids. The Canadian Journal of Chemical Engineering, v. 87, n. 6, p. 910-914, 2009.
HIDALGO, M. E.; CÔRREA, A. P. F.; CANALES, M. M.; DAROIT, D. J.; BRANDELLI, A.; RISSO, P. Biological and physicochemical properties of bovine sodium caseinate hydrolysates obtained by a bacterial protease preparation. Food Hydrocolloids, v. 43, p. 510-520, 2015.
LEE, J. K.; KIM, M.-J. Ionic liquid-coated enzyme for biocatalysis in organic solvent. The Journal of Organic Chemistry, v. 67, n. 19, p. 6845-6847, 2002.
NASCIMENTO, M. G.; DA SILVA, J. M. R.; DA SILVA, J. C.; ALVES, M. M. The use of organic solvents/ionic liquids mixtures in reactions catalyzed by lipase from Burkholderia cepacia immobilized in different supports. Journal of Molecular Catalysis B: Enzymatic, v. 112, p. 1-8, 2015.
SALA, L.; GAUTÉRIO, G. V.; YOUNAN, F. F.; BRANDELLI, A.; MORAES, C. C.; KALIL, S. J. Integration of ultrafiltration into an aqueous two-phase system in the keratinase purification. Process Biochemistry, v. 49, n. 11, p. 2016-2024, 2014.
SARMADI, B. H.; ISMAIL, A. Antioxidative peptides from food proteins: a review. Peptides, v. 31, n. 10, p. 1949-1956, 2010.
WALSTRA, P.; JENNESS, R. Dairy Chemistry & Physics. John Wiley & Sons, 1984. ISBN 0471097799.
YANG, Z.; ZHANG, K.-P.; HUANG, Y.; WANG, Z. Both hydrolytic and transesterification activities of Penicillium expansum lipase are significantly enhanced in ionic liquid [BMIm][PF6]. Journal of Molecular Catalysis B: Enzymatic, v. 63, n. 1, p. 23-30, 2010.
































