ISBN 978-85-85905-15-6
Área
Iniciação Científica
Autores
de Almeida, P.H.G. (CCET/UEG) ; de Rezende, C.H.A. (CCET/UEG) ; Ferreira, A.A. (CCET/UEG) ; Batista, M.P. (CCET/UEG) ; Signini, R. (CCET/UEG) ; Costa, M.B. (CCET/UEG)
Resumo
A quitosana, polímero derivado da quitina, possui larga aplicação e destaca- se por ser estável, atóxico, filmogênico, apresentar potencial elétrico natural, além de ação antioxidante e antimicrobiana. Entretanto, quitosanas e seus derivados demonstram sua atividade biológica somente em meio ácido devido ao seu baixo pH 6,5 e baixa solubilidade em meio aquoso. Vislumbrando melhorar as condições para a solubilidade destes compostos, em meio aquoso e/ou solventes orgânicos, este trabalho vislumbrou a síntese de quitosanas guaniladas, a partir do emprego de tiouréias substituídas. Os rendimentos iniciais evidenciaram uma necessidade na melhora da metodologia proposta, bem como, no grau de purificação da quitosana, uma vez que os mesmos foram superiores a 100%.
Palavras chaves
Quitosana; Guanilação; Solubilidade
Introdução
Moléculas bioativas, oriundas de produtos naturais ou sintéticas, são promissoras por possuírem uma diversidade estrutural, com amplo espectro de atividades biológicas (DIAS, 2001; GUIDO, 2010), dentre as quais se destacam as atividades antimicrobiana, antifúngica, anticâncer, dentre outras (SILVA, 2013). A quitosana é um polímero estável, atóxico, filmogênico e além de possuir potencial elétrico, apresenta ação antioxidante e antimicrobiana (CORTEZ, 2013). Entretanto, esse potencial biológico ocorre somente em meio ácido devido ao seu baixo pH 6,5. Assim, os derivados de quitosana com solubilidade em água, são solúveis em meio fisiológico básico e são ácidos (CAI, 2013). Na tentativa de melhorar esta barreira (solubilidade), muitos pesquisadores direcionam estas reações de síntese, com quitosanas, para gerar derivados solúveis (CAI, 2013). Reações de guanilação em quitosanas são descritas na literatura, mas a maioria envolve o emprego de bisguanidinas como reagente guanilante. Poucos são os estudos que envolvem o emprego com guandinas N,N-dissubstituídas e tiouréias. Associadas a todas estas observações, este trabalho vislumbrou a síntese de quitosanas guaniladas, a partir da aplicação de tiouréias substituídas, com variação de grupos doadores ou retiradores de elétrons, para inicialmente, avaliar a metodologia proposta e, posteriormente, submeter estes derivados quitosânicos a ensaios biológicos.
Material e métodos
A parte experimental foi executada na Universidade Estadual de Goiás – Campus de Ciências Exatas e Tecnológicas Henrique Santillo. A quitosana, os reagentes e solventes P. A. foram utilizados sem purificação prévia. A Cromatografia em Camada Delgada (CCD) foi realizada utilizando-se placa de alumínio com 0,20 mm de sílica gel 60 com indicador de fluorescência UV254 (Macherey-Nagel). Os espectros de infravermelho (IV) foram registrados no espectrômetro Spectrum Frontier (Perkin Elmer). *Procedimento geral para a síntese de quitosanas guaniladas: As tiouréias (A-E) utilizadas neste estudo foram preparadas de acordo com a metodologia adaptada de Cunha e Colaboradores (2001) e O’Donovan e Colaboradores (2013). Inicialmente, solubilizou-se (3 mmol) de quitosana em 20 mL de ácido acético 1%, com agitação constante por aproximadamente 10 minutos até formar um gel. Em seguida, adicionou-se uma solução de carbonato de sódio 1% até que o pH estivesse na faixa de 7-8. Posteriormente, adicionou-se a tioureia (2 mmol) na solução, e em seguida, 4 mL de uma solução de trietilamina, e 30 mL de água destilada. A reação foi mantida sob refluxo, em banho de óleo, com a temperatura entre 50 - 70°C. A reação foi acompanhada por CCD. Após 2 dias, a reação foi finalizada e purificada por extração descontínua com acetato de etila (2X25mL), seca em Na2SO4 e concentrada em evaporador rotativo.
Resultado e discussão
A busca por novas substâncias biologicamente ativas tem sido um dos grandes
desafios enfrentados pela ciência, principalmente devido ao aumento da
resistência de enfermidades a antibióticos e antifúngicos.
Como alvo sintético, desde grupo de pesquisa, as tiouréias substituídas vêm
sendo estudadas e sintetizadas para posterior aplicação em metodologias de
síntese de derivados quitosânicos guanilados, por reações de guanilação de
quitosanas, com o intuito de melhorar a solubilidades destes compostos que
são descritos como possuidores de grandes atividades biológicas em meio
fisiológico.
Tiouréias são importantes “blocos construtores” devidos às suas aplicações
químicas e farmacêuticas, e neste trabalho foram empregadas em uma
metodologia de guanilação para converter o grupo amino da quitosana em uma
guanidina substituída e funcionalizada.
Em nossos estudos iniciais, os espectros de absorção no infravermelho
mostraram bandas características de quitosanas ( 3450 -3350 cm-1 OH da
quitosana) e quitosanas funcionalizadas com o grupo guanidínico ( 3550 cm-1
NH e 1615 cm-1 CN) em um mesmo espectro. Os rendimentos elevados (>100%)
corroboram para esta mistura. Logo foi possível notar a necessidade de uma
melhora nesta metodologia para que toda a matéria-prima seja convertida em
produto com rendimentos aceitáveis, uma vez que este foi calculado a partir
de uma unidade do monômero funcionalizado.
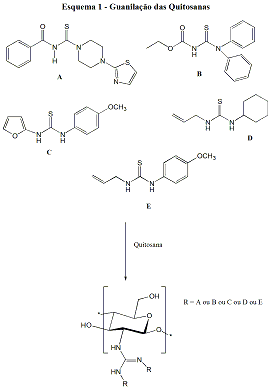
Reação de guanilação da quitosana
Conclusões
Neste trabalho foi possível concluir que a metodologia empregada é viável, apesar dos espectros de absorção no IV evidenciarem a presença de matéria- prima e produtos guanilados. A simplicidade da metodologia para a guanilação da quitosana favorece o aprofundamento deste estudo, com a finalidade gerar melhores rendimentos e posteriormente testarmos a solubilidade dos derivados quitosânicos em meio aquoso e orgânico.
Agradecimentos
Ao CNPQ, CAPES, FAPEG e UEG pelas bolsas fornecidas e ao grupo de pesquisa LabSIMCO.
Referências
CAI, Z. S.; SUN, Y. M.; ZHU, X. M.; ZHAO, L. L.; YUE, G. Y., Polymers Bulletin, V. 70, p.1085-1096, 2013.
CORTEZ, Douglas Henrique Cardoso. Obtenção e Comparação de Quitosanas Fúngicas. Dissertação de Mestrado, UFSC, Florianópolis, SC, 2013.
CUNHA, S. D.; COSTA, M. B.; NAPOLITANO, H. B.; LARIUCCI, C.; VENCATO, I., Tetrahedron, V. 57, p. 1671-1675, 2001.
DIAS, A.; CORRÊA, A. G.; Química Nova, V.24, p. 236-242, 2001.
GUIDO, R. V. C. - ANDRICOPULO D. A.; OLIVA, G., Química Nova, São Paulo, v. 24, 2010.
O’DONOVAN, D.H.; ROZAS, I, Tetrahedron Letters, v. 52, p. 4117-4119, 2011
SILVA, P.B.G.; VICALVI, M.C.V.; EGITO, M.S., SOLIDÔNIO, E.G.; SENA, K.X.F.R.; ALBUQUERQUE, J.F.C., 53º Congresso Brasileiro de Química. Realizado no Rio de Janeiro/RJ, 2013.


















