ISBN 978-85-85905-15-6
Área
Iniciação Científica
Autores
Silva, R.R. (UNIVERSIDADE FEDERAL DE PERNAMBUCO) ; Silva, D.G. (UNIVERSIDADE FEDERAL DE PERNAMBUCO) ; Silva, A.I.S. (UNIVERSIDADE FEDERAL DE PERNAMBUCO) ; Lima, N.B. (UNIVERSIDADE FEDERAL DE PERNAMBUCO)
Resumo
Este trabalho tem como objetivo avaliar a espontaneidade da síntese de complexos de európio com ligantes TPPO, [EuCl2(TPPO)n(H2O)(6-n)]+, a partir da troca de ligantes H2O do complexo reagente [EuCl2(H2O)6]+ por n ligantes TPPO. Todos os cálculos das propriedades termodinâmicas foram obtidos através da utilização do modelo RM1 Orbitais para lantanídeos usando o programa MOPAC. Os nossos resultados mostram que a espontaneidade da reação de troca de ligantes H2O do complexo reagente [EuCl2(H2O)6]+ por ligantes TPPO parece estar relacionada com a quantidade de ligantes TPPO envolvidos. Verificamos, por exemplo, que a reação mais espontânea envolve 4 ligantes TPPO.
Palavras chaves
Európio; RM1; reação de substituição
Introdução
Complexos de európio (III) são alvo de muito interesse pela comunidade científica devido a sua propriedade de converter luz com comprimento de onda na região do ultravioleta em uma luz com o comprimento de onda na região do visível vermelho-alaranjado (Lima et al, 2013). A eficiência deste processo de conversão de luz depende dos ligantes que estão coordenados ao metal. Podemos citar como exemplo de ligantes eficientes, os ligantes iônicos ß-dicetonatos. Comumente, também são utilizados ligantes não iônicos, podemos citar como exemplo, o ligante óxido de trifenilfosfina, TPPO, figura 1. Uma vez preparados estes complexos, é possível utiliza-los em várias aplicações, dentre elas: em LED’s (SHAO et al, 2012); em dispositivos óptico eletrônicos (WANG et al, 2011), etc. A síntese de complexos de európio(III) com ligantes ß-dicetonatos normalmente é realizada a partir da reação envolvendo o complexo reagente [EuCl2(H2O)6]Cl, onde tanto os ligantes H2O quanto os ligantes cloretos podem ser facilmente substituídos por outros ligantes (Lima et al, 2013). Neste contexto, temos como objetivo a análise da espontaneidade das reações de troca dos ligantes H2O do complexo reagente [EuCl2(H2O)6]Cl por n ligantes TPPO, sendo n=1, 2, 3 ou 4.
Material e métodos
No sentido de calcular as propriedades termodinâmicas escolhemos o modelo RM1 orbitais para lantanídeos e o programa de química quântica computacional MOPAC. Inicialmente, realizamos cálculos de otimização completa de geometria, onde em seguida calculamos as frequências de todas as espécies consideradas neste trabalho. Finalmente, obtivemos os dados das propriedades termodinâmicas (entalpias de formação, entropia e energia livre de Gibbs de formação).
Resultado e discussão
A tabela 1 apresenta os valores de energia livre de Gibbs de reação, ∆rG, de
todas as reações consideradas neste trabalho. Os nossos resultados indicam que
a reação envolvendo o complexo reagente [EuCl2(H2O)6]+ e quatro ligantes TPPO,
formando o complexo [EuCl2(TPPO)4(H2O)2]+ parece ser a mais espontânea porque
o valor de ∆rG (-117kcal/mol) é o mais negativo comparando com as demais
reações. Em seguida, passamos a avaliar a possibilidade do complexo
[EuCl2(TPPO)4(H2O)2]+ realmente ter ligantes H2O no poliedro de coordenação.
Assim, também estudamos outras duas reações em que além das quatro moléculas de
água serem trocadas por quatro ligantes TPPO, as demais também seriam
dissociadas, formando assim os complexos [EuCl2(TPPO)4(H2O)]+ e
[EuCl2(TPPO)4]+. Os nossos resultados mostram que provavelmente a espécie
prevista para ser mais espontânea de ser formada é a [EuCl2(TPPO)4]+, ou seja,
sem nenhum ligante H2O coordenado ao metal. Isso deve ocorrer devido ao
aumento de impedimento estérico no complexo, pois as moléculas de TPPO são
consideravelmente mais volumosas quando comparadas com as moléculas de água.
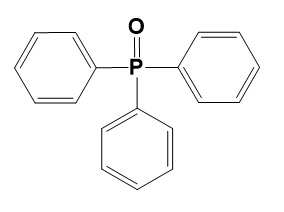
Estrutura química do óxido de trifenilfosfina (TPPO).

Conclusões
Neste trabalho foram analisadas a espontaneidade das reações de troca de ligantes H2O do complexo [EuCl2(H2O)6]+ por ligantes TPPO. Os nossos resultados mostram que a reação com maior espontaneidade forma o complexo [EuCl2(TPPO)4]+, onde quatro ligantes TPPO deslocaram todos os ligantes H2O que estavam coordenados ao metal.
Agradecimentos
Os autores agradecem ao PIBID-Química/UFPE, ao PET-Química/UFPE, à PROAES/UFPE, ao CNPq, ao PRONEX/FACEPE.
Referências
Lima, Nathália B. D., Gonçalves, Simone M. C., Júnior, Severino A., Simas, Alfredo M., Sci Rep-Uk, v. 3, p. 2395, 2013.
Shao, G., Li, Y., Feng, K., Gan, F., Gong, M., Sensors Actuators B Chem. 173, 692–697, 2012.
Wang, G., Peng, Q., LI, Y., Acc. Chem. Res. 44, 322–332, 2011.


















