ISBN 978-85-85905-15-6
Área
Química Orgânica
Autores
Mendonça, M.A.G. (UNIVERSIDADE ESTADUAL DE GOIÁS) ; Andrade, C.C. (UNIVERSIDADE ESTADUAL DE GOIÁS) ; Mendonça, T.L.F. (UNIVERSIDADE ESTADUAL DE GOIÁS) ; Lázaro Faleiro Naves, P. (UNIVERSIDADE ESTADUAL DE GOIÁS) ; Borges Costa, M. (UNIVERSIDADE ESTADUAL DE GOIÁS)
Resumo
Diversas moléculas de cunho medicamentoso possuem o núcleo guanidínico inserido em um sistema heterocíclico condensado. Reações tri-componentes com guanidinas tem sido reportadas com bom rendimento em uma única etapa. O objetivo deste trabalho foi avaliar a toxicidade do N-[3,4,5,6,7,8- hexaidro-1,3-bis-(4-metoxifenil)-5-oxo-4-fenilquinazolin-2-(1H)-ilideno]- benzamida, um composto obtido através da reação entre um núcleo guanidínico, dimedona e benzaldeído, frente a "Artemia salina" Leach em ensaios independentes. Os resultados obtidos indicam um teste validado já que o controle com dicromato de potássio matou os naúplios de A. salina nas concentrações do teste. Indicam, ainda, que o composto em questão possui certa toxicidade frente aos microcrustáceos, entretanto essa toxicidade é baixa.
Palavras chaves
guanidina; tricomponente; Artemia salina
Introdução
Todos os ambientes não controlados são povoados por micro-organismos que exercem suas atividades metabólicas de maneira independente, ou não, contribuindo beneficamente ou causando algum tipo de malefício, por exemplo, doenças ao seu hospedeiro[1]. No caso da microbiota normal, ou flora como antigamente denominada, quando instalada em seu território normal é capaz de proteger contra agentes infecciosos, sintetizar vitaminas (como as do complexo B e a própria vitamina K) e outros compostos interessantes para o metabolismo do hospedeiro. Entretanto, caso ocorra alguma situação de perda da integridade de algum tecido, órgão ou sistema, as bactérias podem migrar do seu habitat e causar doenças em outras regiões do organismo[1]. Em suas mais diversas formas e apresentações, os antibióticos transformaram a terapêutica contra bactérias causadoras destas doenças de forma a permitir que o tratamento de algo que antes era causa de altos índices de morbi- mortalidade tornasse corriqueiro e, mais além, solidificando terapias que, em tempos passados, seriam bastante remotas. Contudo, todos os esforços passados em tornar este tipo de droga disponível ao mundo serão em vão se os mecanismos de resistências desenvolvidos pelos patógenos a estes medicamentos continuarem a crescer mais rapidamente que a taxa de desenvolvimento de novas moléculas ativas e formas farmacêuticas viáveis de tratamento[2]. Na tentativa de reverter esta situação, o grupo funcional “guanidina” – encontrado em várias substâncias naturais isoladas de algas, esponjas, micro-organismos e responsável pela atividade biológica de muitos compostos farmacêuticos – tem sido estudado como possível agente antimicrobiano[3]. Guanidinas são classificadas como bases orgânicas. Trata-se de um grupo funcional centrado em um esqueleto protonado denominado “Aromaticidade Y”, ou seja, possui uma ressonância através de três formas canônicas. Por isso, as guanidinas apresentam boa estabilidade e natureza altamente básica (corroborada pelo pH do ácido conjugado de aproximadamente 13)[4]. Dentre as substâncias naturais dotadas deste grupo funcional, pode-se citar a estreptomicina, um antibiótico aminoglicosídico que revolucionou a terapia de tuberculose e tem-se mostrado com certa atividade oncogênica através da inibição do microARN oncogênico miR-21. Este oncogene é bastante expresso em vários tipos de câncer e sua depleção é capaz de diminuir consideravelmente os tumores. Derivados guanilados de aminoglicosídeos tem mostrado também excelente capacidade antimicrobiana contra bactérias resistentes importantes na clínica médica como Staphylococcus aureus e S. epidermidis[5]. Entretanto, o principal empecilho do uso terapêutico de moléculas guaniladas diz respeito à baixa absorção oral. Desta forma, a otimização molecular de tais compostos para tornar o processo de absorção intestinal mais viável de moléculas contendo este grupo funcional é uma necessidade iminente[6]. Uma das formas de otimizar a funcionalidade do grupo guanidínico é a formação de sistemas heterocíclicos condensados ou lineares, que têm mostrado um vasto potencial de atividades biológicas, rendimentos de reações relativamente altos apesar de sua complexidade e sínteses resumidas em apenas uma etapa utilizando-se o componente guanidínico, composto β – dicarbonil (dimedona) e aldeído aromático[7]. Uma das maneiras de se testar a atividade biológica é através de "Artemia salina" (Leach), um microcrustáceo comumente usado em ensaios de toxicidade, uma vez que é considerado como indicador de letalidade quando em um bioensaio que utiliza a CL50 (concentração letal média) como diretriz de teste da atividade biológica[8]. Ensaios com "Artemia salina" são aplicados para detecção de compostos bioativos cuja toxicidade contra este microcrustáceo é um indício de potencial atividade biológica em outros organismos. Desta forma, é de grande valia usar este ensaio como norte pra estudos mais específicos de substâncias bioativas[9]. Sendo assim, este trabalho objetivou avaliar a citotoxicidade preliminar de um composto obtido através da condensação tri-componente de um reagente contendo o núcleo guanidínico utilizando-se "Artemia salina".
Material e métodos
A parte experimental foi executada na Unidade Universitária de Ciências Exatas e Tecnológicas (UnUCET) da Universidade Estadual de Goiás (UEG). Os reagentes e solventes P. A. (E. Merck, Aldrich Chemical Co., Fluka, Grupo Química, Vetec, Ecibra e Quimex) foram utilizados sem purificação prévia. Os ensaios foram realizados conforme método de Meyer e colaboradores (1982), com adaptações de Molina-Salinas & Said-Fernández (2006), que veio a padronizar este tipo de ensaio. Utilizou-se meio de água marinha sintética preparado com dissolução de sal marinho (40 g L-1) em água destilada com a devida suplementação com extrato de leveduras (6 mg L-1) e posterior esterilização em autoclave. Ajustou-se o pH para 8,5 com solução de bicarbonato de sódio 0,1 mol L-1. Foram incubados 100 mg dos cistos por 36 horas em 1 L de meio com fonte de iluminação artificial, temperatura ambiente e oxigenação constantes. Após a eclosão, os náuplios, atraídos por fonte de luz, foram pipetados e transferidos para uma placa de Petri com 5 mL de meio fresco. O bioensaio foi realizado em microplaca de poliestireno estéril de 96 poços na qual foram adicionadas diferentes concentrações (500, 250, 125, 62,5 e 31,25 μg mL-1) do composto. Os náuplios foram distribuídos nas placas, padronizando um total de 10±1 indivíduos em cada poço. Controles negativos, de viabilidade e de letalidade foram incluídos no ensaio utilizando diluições de 100 μg mL-1 de dicromato de potássio. Com os resultados, foi possível o cálculo da DL50 pelo método gráfico dose-resposta – Próbito, no programa computacional Statistic 2010. Todos os ensaios realizados foram feitos em triplicata e de maneira independente.
Resultado e discussão
Um desafio para a execução do teste de toxicidade frente à "A. salina" foi à
solubilização da amostra do composto heterocíclico guanidínico.
Ela foi feita em Dimetilsulfóxido (DMSO), mostrando-se bastante solúvel,
para posterior adição à água marinha até completar-se o volume do balão
volumétrico. Contudo, ao adicionar-se a água salina, foi possível perceber
uma pequena turvação. Para averiguar se a turvação era decorrente da
precipitação do composto, o teste foi repetido apenas com DMSO em água
salina e a turvação foi novamente perceptível. Sendo assim, o teste de
toxicidade foi realizado com a amostra solubilizada inicialmente em DMSO 10%
e água marinha já que a turvação não se relacionou diretamente com a
precipitação do composto guanidínico em teste.
Procedeu-se, então, com a execução do teste frente a um controle com
dicromato de potássio, que é um composto comprovadamente letal para "A.
salina". E, de fato, pode-se perceber que, nas concentrações utilizadas da
amostra de teste, os controles morreram. Desta forma, o teste foi validado.
Para avaliação da toxicidade ou inércia do DMSO procedeu-se com o teste do
branco, ou seja, os naúplios foram submetidos à análise no meio de água
marinha somente e no meio de água marinha com 10% de DMSO. Em ambos os
casos, notou-se que os naúplios não morreram significativamente. Conclui-se,
pois, que o meio com DMSO não favoreceu a morte dos microcrustáceos e,
quaisquer efeitos de morte ou não eram devidos única e exclusivamente ao
composto teste.
O teste total foi executado em triplicata em dois dias diferentes, com a
mesma solução estoque, porém com diluições diferentes. Assim, manteve-se a
independência do teste, ou seja, desta forma é possível reduzir ao máximo os
possíveis erros interferentes nos resultados como: erro do analista,
diluição, pesagem, preparação de soluções etc.
Com aproximação de uma casa decimal, o valor encontrado previsto para DL50
do composto N-[3,4,5,6,7,8-hexaidro-1,3-bis-(4-metoxifenil)-5-oxo-4-
fenilquinazolin-2-(1H)-ilideno]-benzamida (Figura 1) é 328,5 μg mL-1, de
acordo com o
software Statistica.
A literatura mostra que a determinação da toxicidade dos compostos leva em
consideração que valores de CL50<1000ppm apresentam certa toxicidade frente
à "Artemia salina" (MEYER et al., 1982). Desta forma, são considerados com
baixa toxidade os que apresentam CL50 entre 250 e 1000ppm, já os com CL50
entre 250 e 80ppm são considerados moderadamente tóxicos, e com CL50 abaixo
de 80pmm altamente tóxicos (DOLABELA, 1997).
Sendo assim, é possível afirmar que o composto possui toxicidade contra
"Artemia salina". Embora a toxicidade seja baixa, deve-se proceder com
testes de atividade biológica frente a bactérias, fungos e tumores de forma
a se ter uma ideia global do quão pronunciada é esta atividade em outros
testes e outros organismos com a perspectiva de se descobrir uma molécula
com potencial uso terapêutico.
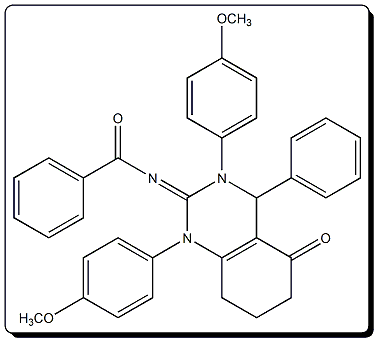
Estrutura química do composto N-[3,4,5,6,7,8- hexaidro-1,3-bis-(4-metoxifenil)-5-oxo-4- fenilquinazolin-2-(1H)-ilideno]-benzamida.
Conclusões
O desenvolvimento de fármacos eficazes para o tratamento de infecções bacterianas é uma realidade iminente em um contexto marcado pelo crescimento acelerado de mecanismos de resistência microbiana aos medicamentos disponíveis no mercado. O composto sintetizado e alvo do teste de toxicidade frente à "Artemia salina" é um heterociclo contendo um grupo guanidínico obtido pela condensação de uma guanidina com dimedona e benzaldeído. A avaliação estatística foi feita de modo independente para evitar erros humanos e de maquinário. Obteve-se como resultado de CL50 o valor de 328,5 ppm, indicativo de um composto com baixa toxicidade frente aos microcrustáceos e passível de submissão a outros testes biológicos para averiguação de atividade frente a outros microorganismos.
Agradecimentos
À UEG pelo Programa de Pós-Graduação, ao corpo docente e de técnicos de laboratórios pela orientação na execução dos experimentos. À CAPES pelo apoio financeiro.
Referências
1 TORTORA, G.J.; FUNKE, B.R.; CASE, C.L. Microbiologia, 10 ed., p. 18, 69, 70, 77, 555, 574, 575; Porto Alegre, Artmed, 2012.
2 LIVERMORE, D.M. The need for new antibiotics. Clinical microbiology and infection, v. 10, p. 1-9, 2004.
3 CHEN, C. Y.; LIN, H. C.; HUANG, Y. Y.; CHEN, K. L.; HUANG, J. J.; YEH, M. Y.; WONG, F. F. ‘One-flask’ transformation of isocyanates to guanidines hydrochloride by using sodium bis(trimethylsilyl)amide. Tetrahedron, v. 66, p. 1892-1897, 2010.
4 SACZEWSKI, F.; BALEWSKI, L. Biological activities of guanidine compounds. Expert Opinion Therapeutics Patents, v.19, p. 1417-1448, 2009.
5 BERLICK, R.G.S.; TRINDADE-SILVA, A. E.; SANTOS, M.F.C., The chemistry and biology of organic guanidine derivatives. Natural Product Reports, v. 29, p.1382-1406, 2012.
6 RAULF, M.K.; DIN, I.; BADSHAH, A. Novel approaches to screening guanidine derivatives. Expert opinion drug discovery, v.8, p. 1-15, 2013.
7 POTAPOV, A.Y,; SHIKHALIEV, H. S.; KRYLSKY, D.V.; KRISIN, M.Y., Three-component condensation of hetarylguanidines with aldehydes (ketones) and dicarbonyl compounds. Chemistry of Heterocyclic Compounds, v. 42, p. 1338-1342, 2006.
8 NUNES, P. X.; MESQUITA, R. F.; SILVA, D. A.; LIRA, D. P.; COSTA, V. C. O.; SILVA, M. V. B.; XAVIER, A. L.; DINIZ, M. F. F. M.; AGRA, M. F. Constituintes químicos, avaliação das atividades citotóxica e antioxidante de Mimosa paraibana Barneby (Mimosaceae). Revista Brasileira de Farmacognosia, v.18 (supl), p.718-723, 2008.
9 AMARANTE, C. B.; MÜLLER, A. H.; PÓVOA, M. M.; DOLABELA, M. F. Estudo fitoquímico biomonitorado pelos ensaios de toxicidade frente à Artemia salina e de atividade antiplasmódica do caule de aninga (Montrichardia linifera). Acta Amazonica, v.41, n.3, p.431-434, 2011.


















