Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Química Tecnológica
TÍTULO: SÍNTESE, CARACTERIZAÇÃO E ATIVIDADE BIOLÓGICA DE ACETATOS DE COBRE (II) E FERRO (III) PARA CONTROLE DE Aedes aegypti (DIPTERA: CULICIDAE).
AUTORES: Verger Nardeli, J. (UFGD) ; Haiashi Kato, M.F. (UFGD) ; Teodoro Carvalho, C. (UFGD) ; Jose de Arruda, E. (UFGD)
RESUMO: Objetivou se a síntese de acetatos básicos de Cu2+ e Fe3+ para análise da
toxicidade com larvas de 3º estádio de Aedes aegypti e avaliação da atividade
biológica com bactérias Gram-negativas e Gram-positivas. Os íons metálicos de
transição Cu2+ e Fe+3 possuem atividade bactericida e fungicida e são tóxicos para
larvas de Aedes aegypti nos estágios de ovo e larvais, inviabilizam a eclosão dos
ovos, retardam o ciclo reprodutivo do inseto e controlando microrganismos de forma
persistente. Também se investiga a importância dos grupos carboxilas na formação
dos complexos metálicos, toxicidade, transporte e internalização celular dos íons
tóxicos. A atividade inseticida e/ou bactericida é devido, principalmente, aos
íons metálicos Cu2+ e/ou Fe3+ por indução celular in situ de estresse.
PALAVRAS CHAVES: Aedes aegypti ; acetatos, larvicida; estresse oxidativo.
INTRODUÇÃO: A dengue é uma doença virótica e, atualmente, a infecção de maior ocorrência nos
humanos1. Os mosquitos são insetos vetores eficientes na transmissão do
patógeno, a partir da sucção de sangue do indivíduo contaminado pelo vírus,
incubação e propagação para outro indivíduo. Sabe-se que não se pode erradicar o
inseto vetor, pois a ausência de uma espécie e seu nicho biológico e competência
vetorial poderia até ser substituída por outra espécie, talvez, até mais
competente vetorialmente para a propagação do vírus e da doença2. Neste trabalho
buscou-se investigar a atividade inseticida e/ou biológica dos acetatos,
principalmente, como inseticidas não convencionais com vista ao controle do
inseto a partir das suas formas imaturas e alteração/retardação do ciclo
reprodutivo e sua dinâmica para o controle de doenças negligenciadas. A síntese,
caracterização e toxicidade dos acetatos de Cu2+ e Fe3+ foram realizadas para
larvas de 3o estádio de A. aegypti, inibição da eclosão de ovos e atividade
biológica para as bactérias Staphylococcus aureus ATCC-25923(+), Escherichia
coli ATCC-25922(-), Listeria monocytogenes ATCC-7644(+) e Salmonella typhimurium
ATCC-14028(-). Estas bactérias foram escolhidas como bactérias modelos para o
controle de microrganismos dos criadouros e cadeia alimentar do inseto.
MATERIAL E MÉTODOS: O acetato de ferro foi preparado por via sódica utilizando uma metodologia
clássica3 com modificações, para obtenção de acetato de Fe3+ com poucos íons
interferentes para os bioensaios de toxicidade. As sínteses dos acetatos mais
puros foram realizadas por via carbonato4. A reação do acetato de Fe3+ é
mostrada na equação 1, esta mesma metodologia via carbonato foi utilizada para a
síntese do acetato de Cu2+.
FeCO3 (s) + 3 CH3COOH(aq.) → Fe(CH3COO)3 (aq.)
(1)
Os antibiogramas foram realizados com acetatos de Cu2+ e Fe3+ no intervalo de
concentração de 10-1 a 10-4 mol L-1 contra bactérias Gram(-) e Gram(+) por
metodologias previamente estabelecidas5. Os bioensaios de toxicidade foram
realizados por metodologia descrita na literatura e estabelecida pela OMS com
modificações para larvas de 3o estádio de A. aegypti (linhagem Rockfeller) e os
resultados experimentais da mortalidade foram tratados estatisticamente por
probit6.
RESULTADOS E DISCUSSÃO: Resultados mostraram que o acetato de Cu2+ inviabiliza e/ou impede a eclosão dos
ovos a partir da disponibilidade do íon Cu2+ em solução, afetando a viabilidade
dos ovos. A mortalidade das larvas ocorreu pela destruição da matriz peritrófica
(MP), e, possivelmente, por facilitação do transporte e internalização dos íons
metálicos para indução in situ de danos celulares por reações redox (estresse
oxidativo) nas células do intestino médio (mesêntero) do sistema digestório das
larvas de A. aegypti. Estes resultados são importantes para avaliar a extensão
do controle populacional do vetor considerando a redução populacional dos
insetos, alteração da microbiota e de microrganismos da cadeia alimentar do
inseto por imposição de condições desfavoráveis e/ou restrições ou atraso ao
processo reprodutivo do inseto. A imposição dessas condições desfavoráveis pode
alterar o ciclo reprodutivo e, permitir um controle abrangente e aditividade no
controle como parte importante do manejo do inseto. Os resultados dos
antibiogramas mostraram a susceptibilidade de bactérias Gram-positivas e Gram-
negativas Staphylococcus aureus ATCC-25923(+), Escherichia coli ATCC-25922(-),
Listeria monocytogenes ATCC-7644(+) e Salmonella typhimurium ATCC-14028(-) em
soluções diluídas com concentrações de acetato de Cu2+ e Fe3+ no intervalo de
10-1 a 10-4 mol L-1. Na Figura 1 e 2 são mostrados os tamanhos dos halos de
inibição para os microrganismos indicando os diâmetros de inibição (mm) versus
concentração dos compostos (mol L-1).
Os bioensaios de toxicidade com larvas de 3º estagio de A. aegypti mostraram que
o acetato de Cu2+, possui CL10 de 0,910±0,038 mg L-1, CL50 de 10,989±5,39 mg L-1
e CL90 de 901,892±109,85 mg L-1 (onde mg L-1 = ppm). O acetato de Fe3+ não
mostrou atividade bactericida.
Fig 1.
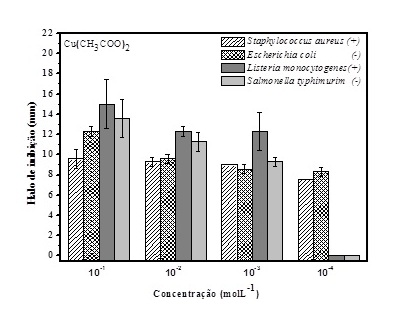
Antibiograma para bactérias Gram-positivas e Gram-
negativas com Cu(CH3COO)2 no intervalo de
concentração de 10-1 a 10-4 mol L-1
Fig 2.

Antibiogramas para bactérias Gram-positivas e Gram-
negativas com Fe(CH3COO)3 no intervalo de
concentração de 10-1 a 10-4 mol L-1
CONCLUSÕES: O acetato de Cu2+ possui atividade biológica/larvicida para o A. aegypti e
bactérias Gram-positivas e Gram-negativas. Nas concentrações de controle
utilizadas para larvas de 3o estádio de A. aegypti e microrganismos que pertencem
a cadeia alimentar do inseto e pode apresentar baixo impacto ambiental. Observa se
que a atividade do acetato de Cu2+ é abrangente e resultou em halos de inibição
maiores em relação ao acetato de Fe3+, apresentando maior atividade biológica para
o inseto e microrganismo. O acetato de Fe3+ não possui atividade larvicida até
1000 ppm, mas possui atividade bactericida.
AGRADECIMENTOS: UFGD, UNESP, CAPES, CNPq e FUNDECT.
REFERÊNCIAS BIBLIOGRÁFICA: 1. WHO. Dengue guidelines for diagnosis, treatment, prevention and control. (2009). World Health Organization. WHO/HTM/NTD/DEN/2009.
2. FANG, J. A world without mosquitoes. Nature. Washington-DC, p.433-434, 2010.
3. SKOOG, D.A.; WEST, D.M.; HOLLER, F.J.; CROUCH, S.R. Fundamentals of Analytical Chemistry. 8º ed. Ed. Thomson/Brooks/Cole, CA, USA. p. 449-485, 2004.
4. CARVALHO, C. T et al. Synthesis, characterization and thermal behaviour of solid-state compounds of 2-methoxybenzoate with some bivalent transition metal ions. Eclética, v. 30, p. 19-26, 2005.
5. NATIONAL COMMITTEE FOR CLINICAL LABORATORY STANDARDS - NCCLS. 1993. Methods for dilution antimicrobial susceptibility tests for bacteria that grow aerobically. Approved standard M7-A3, 2nd ed. National Committee for Clinical Laboratory Standards, Villanova, Pa.
6. WHO - World Health Organization. Instructions for determining the susceptibility or resistance of mosquito larvae to insecticides: WHO-VBC 81.807. p. 1-6, 1981.
