Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Ambiental
TÍTULO: ESTUDO DA OXIDAÇÃO TERMOQUÍMICA USANDO A TÉCNICA DiCTT PARA A DEGRADAÇÃO/MINERALIZAÇÃO DE EFLUENTES LÍQUIDOS FENÓLICOS
AUTORES: Brandão, Y.B. (UFPE/UNICAP) ; Teodosio, J.R. (UFPE) ; Oliveira, J.G.C. (UFPE) ; Silva-júnior, A.A. (UFPE) ; Vasconcelos, W.E. (UNICAP) ; Benachour, M. (UFPE)
RESUMO: Essa pesquisa tem como objetivo avaliar a técnica de Tratamento Térmico por Contato Direto (DiCTT) de efluentes líquidos para oxidação termoquímica do composto orgânico fenol. Os estudos experimentais foram realizados em uma estação semi-industrial operando com um excesso de ar (E) de 40%, vazão de gás natural (QGN) de 4 m3.h-1, vazão líquida (QL) de 170 L.h-1, taxa de reciclagem dos gases de combustão (QRG) de 50% e razão molar estequiométrica fenol/peróxido de hidrogênio (R) de 50%, quantificando-se a degradação do fenol por Cromatografia Líquida de Alta Eficiência-CLAE e a conversão do Carbono Orgânico Total-COT com um analisador de COT. A formação de ácidos foi analisada por um pH-metro. Foram alcançadas taxas de degradação do fenol de quase 99% e conversão de COT de até 35%.
PALAVRAS CHAVES: DiCTT; Fenol; Radicais Hidroxila
INTRODUÇÃO: Os compostos fenólicos são prejudiciais à saúde humana, podendo provocar necrose, problemas digestivos, danos ao fígado e aos rins (CHEN et al.,2004; TOR et al., 2006). Quando presentes em água potável, os fenóis podem causar sérios problemas de saúde pública, podendo também provocar a morte de peixes, mesmo em concentrações na faixa de 1 mg.L-1. Em concentrações inferiores a 1 mg.L-1, são também tóxicos a outras espécies biológicas e destroem o ambiente aquático (MISHRA et al., 1995). Devido a esses fatores, o Conselho Nacional do Meio Ambiente-CONAMA estabelece o valor máximo de 0,5 mg.L-1 para a presença de substâncias orgânicas em efluentes, tais como fenóis (CONAMA,2011).
Uma das alternativas viáveis no tratamento dos efluentes orgânicos fenólicos está no uso de um novo Processo Oxidativo Avançado (POA) não convencional, aplicando a técnica DiCTT (Direct Contact Thermal Treatment), que visa oxidar os compostos fenólicos a baixas temperaturas e à pressão atmosférica, através da geração dos radicais livres, principalmente •OH, decorrentes da chama de combustão do gás natural (metano), podendo favorecer a aplicação desta tecnologia em plataformas de prospecção de petróleo do tipo “off-shore”, onde o gás natural é disponível e o espaço físico é reduzido (BENALI; GUY,2007; BRANDÃO et al., 2010). Este trabalho tem como objetivo o tratamento de efluentes líquidos fenólicos em diferentes concentrações iniciais de fenol (CF0) variando entre 500 e 3000 mg.L-1 através do processo DiCTT. Os estudos experimentais no tratamento desses efluentes foram realizados em uma estação semi-industrial, quantificando-se a degradação termoquímica do fenol e a conversão do Carbono Orgânico Total (COT), com formação de ácidos e a mineralização da carga orgânica em dióxido de carbono e água.
MATERIAL E MÉTODOS: Nesta técnica DiCTT o efluente líquido contaminado com fenol é injetado tangencialmente no reator para produzir um fluxo helicoidal nas suas paredes internas. Esse fluxo permite um contato mais íntimo entre o efluente líquido e os radicais livres da chama, principalmente •OH, propiciando a oxidação dos compostos fenólicos à baixas temperaturas e à pressão atmosférica, evitando ao mesmo tempo a incineração da fase líquida. A temperatura elevada da chama contribui para o aumento do desempenho da oxidação em presença de radicais livres, bem como favorece que o processo de oxidação se realize completamente na fase líquida, através da transferência de uma parte do excesso de oxigênio presente na chama. Uma representação esquemática da estação semi-industrial utilizada na condução dos ensaios experimentais está representada conforme a Figura 1.
Considerando a temperatura da fase líquida (cerca de 77 0C) foi avaliado a oxidação termoquímica para diferentes concentrações iniciais de fenol (CF0) variando entre 500 e 300 mg.L-1, sendo o excesso de ar (E) de 40%, a vazão de gás natural (QGN) de 4 m3.h-1, a razões molar estequiométrica fenol/peróxido de hidrogênio (R) de 50%, a vazão de recirculação da fase líquida (QL) de 170 L.h-1 e a taxa de reciclagem dos gases de combustão (QRG) de 50%.
A razão molar (R) de 100% corresponde à completa mineralização de fenol de acordo com a estequiometria da reação descrita na Equação (1):
C6H5OH + 14 H2O2 → 6 CO2 + 17 H2O (1)
Razões molares de R (diferentes de 100%) são calculadas proporcionalmente conforme previsto pela estequiometria da reação na Eq. (1).
A oxidação do fenol foi quantificada por análises de Cromatografia Líquida de Alta Eficiência (CLAE) e Carbono Orgânico Total (COT) e a acidez monitorada por um pH-metro.
RESULTADOS E DISCUSSÃO: A evolução da temperatura e do pH do efluente líquido durante o processo está apresentada na Figura 2a. Fica evidenciado que a concentração de fenol não influencia a curva de aquecimento da fase líquida, alcançando uma temperatura final de aproximadamente 350K (77°C). As curvas da evolução do pH (Fig. 2.a) mostram que para as concentrações de 2000 e 3000 mg.L-1 de fenol, o pH inicial já apresenta valores baixos, 4 e 3, respectivamente, enquanto para uma CF0=500 mg.L-1, o pH envolve um valor inicial de 8. Uma provável explicação para este fenômeno pode estar diretamente ligado à quantidade de peróxido de hidrogênio adicionado diminuindo o pH inicial devido à uma possível oxidação prematura do fenol, formando ácidos orgânicos (DELVIN; HARRIS, 1984).
As Figuras 2.b e 2.c mostram os perfis de degradação do fenol de quase 99% e conversão do COT de aproximadamente 35%, respectivamente. Na Fig. 2.b evidencia-se claramente que o aumento da concentração inicial de fenol de 500 a 3000 mg.L-1 não interfere na duração da primeira etapa da reação, chamada de período de indução, e não apresenta um efeito significativo sobre a degradação do fenol após um tempo de aproximadamente 130 min. Após o período de indução, ao redor de 110 min, a velocidade da reação se torna mais pronunciada, como era esperado, alcançando valores de XF praticamente iguais após um tempo operacional ao redor de 130 min, independentemente da concentração inicial do fenol. Uma degradação do fenol em torno de 99% é obtida após um tempo de operação de 180 min. A Fig. 2.c permite identificar um tempo de período de indução também de aproximadamente de 110 min, e mostrar um leve aumento da conversão do COT com aumento da concentração inicial do fenol atingindo valores de XT de 27,5; 31,5 e 35% para os valores de CF0.
FIGURA 1

Esquema da estação semi-industrial de tratamento de efluentes líquidos fenólicos por oxidação termoquímica usando a técnica DiCTT.
FIGURA 2
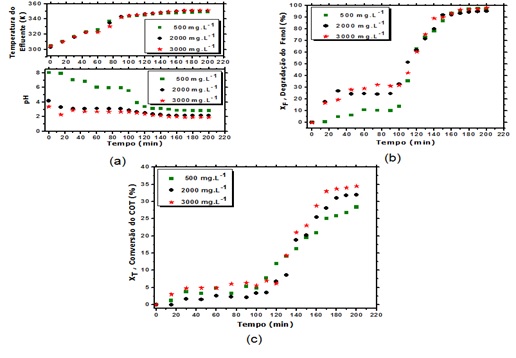
Evolução da temperatura e do pH (a) em função do tempo de operação; Evolução da degradação do fenol (b) e da conversão do COT (c) em função do tempo.
CONCLUSÕES: Independentemente do valor da concentração inicial de fenol (500, 2000 e 3000 mg.L-1), o processo apresenta taxas máximas de degradação de fenol próximas de 99% após 170 min de operação, além de proporcionar uma conversão de carbono orgânico total, após uma duração de 210 min, entre um intervalo de variação reduzido, de 27,5 a 35%, dentro da faixa da concentração inicial de fenol estudada.
AGRADECIMENTOS: Os autores desejam expressar seus agradecimentos para FINEP/MCT-Brasil, a PETROBRÁS e CNPq.
REFERÊNCIAS BIBLIOGRÁFICA: CHEN, Q. M.; YANG, C.; GOH, N. K.; TEO, K. C.; CHEN, B. Photochemical degradation of 1,3-dinitrobenzene in aqueous solution in the presence of hydrogen peroxide. Chemosphere, v. 55, p. 339-344, 2004.
TOR, A.; CENGELOGLU, Y.; AYDIN, M. E.; ERSOZ, M. 2006. Removal of phenol from aqueous phase by using neutralized red mud. Journal of Colloid and Interface Science, v. 300, Issue 2, p. 498-503, 2006.
MISHRA, V. S.; MAHAJANI, V. V.; JOSHI, J. B. Wet air oxidation. Industrial and Engineering Chemistry Research, v. 34, p. 2-48, 1995.
BRASIL. Ministério do Meio Ambiente. Resolução n0 430, de 13 de maio de 2011. Conselho Nacional de Meio Ambiente (CONAMA), Brasília, DF, 2011.
BENALI, M.; GUY, C. Thermochemical oxidation of phenolic-laden liquid effluent models. Journal of Environmental Engineering Science, v. 6, p. 543-552, 2007.
BRANDÃO, Y.; TEODOSIO, J.; BENACHOUR, M.; OLIVEIRA, J.; MARINHO, I.; FIGUEIRÊDO, F.; ANSELMO-FILHO, P. Estudo do efeito do excesso de ar e da potência dissipada do queimador sobre as capacidades do processo DiCTT no tratamento de efluentes líquidos fenólicos. Revista Iberoamericana Sistemática- Cibernética & Informática, v. 7, p. 1 – 9, 2010.
DELVIN, H. R.; HARRIS, I. J. Mechanism of the oxidation of aqueous phenol with dissolved oxygen. Industrial and Engineering Chemistry Research, v. 23, p. 387-392, 1984.
