Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Química Analítica
TÍTULO: OTIMIZAÇÃO DO PROCESSO DE EXTRAÇÃO DE SUBSTÂNCIAS ORGÂNICAS UTILIZANDO A CASCA DO BARBATIMÃO (Stryphnodendron barbatiman Mart. )
AUTORES: Albuquerque, R.T. (ETELDL-PE) ; Silva-junior, A.A. (UFPE/ETELDL-PE) ; Silva, D.D. (ETELDL-PE) ; Silva, S.J. (ETELDL-PE) ; Moraes, C.M. (UFPE/ETELDL-PE) ; Bastos, A.M.R.S. (UFPE) ; Albuquerque, S.S.M.C. (UFPE) ; Andrade, S.A. (UFPE) ; Benachour, M. (UFPE)
RESUMO: O objetivo desta pesquisa foi a otimização do processo de extração de substâncias
orgânicas da casca do Barbatimão (Stryphnodendron barbatiman Mart.). Foi utilizada
um planejamento delinear fracionário 26-2, com 16 ensaios, 4 variáveis
independente: solvente - álcool (-1) e água (+1),concentração – 15 g / 50 mL (-1)
e 30 g / 50 mL (+1),aquecimento - T ambiente (-1) e com T 40ºC (+1), e tempo de
imersão - 30 minutos (-1) e 60 minutos (+1). O melhor processo de extração para o
álcool foi no ensaio 2 (no processamento álcool, 30 g / 50 mL, 40°C e 60 minutos)
e para a água foi no ensaio 9, no processamento água, 30 g / 50 mL, 40°C e 30
minutos. Todos os extratos apresentaram absorções na faixa de comprimento de onda
de 190 a 500 nm, o que os tornam viáveis economicamente.
PALAVRAS CHAVES: Casca do Barbatimão; Extração; Otimização
INTRODUÇÃO: Barbatimão: planta medicinal utilizada há muito tempo pelos indígenas, é
encontrada no cerrado brasileiro. Tem ação anti-sépticacicatrizante,
antibacteriana e antifúngica (Criasude, 2013). Nos planejamentos experimentais
baseados em princípios estatísticos os pesquisadores podem extrair do sistema em
estudo o máximo de informação útil, fazendo um número mínimo de experimentos.
Essas técnicas são ferramentas poderosas, com as quais vários objetivos
específicos podem ser alcançados (SOUZA, 2007). A extração é uma técnica usada
para separação, isolamento e purificação de compostos orgânicos. Este processo
se baseia na maior solubilidade de um ou mais compostos de uma mistura em
determinado solvente. Duas ou mais substâncias podem ser separadas pela extração
somente se suas solubilidades forem muito diferentes (SOLOMONS & FRYHLE, 2002).
A espectrofotometria é o método de análises óptico mais usado nas investigações
biológicas e físico-químicas. A cor das substâncias se deve a absorção
(transmitância) de certos comprimentos de ondas da luz branca que incide sobre
elas, deixando transmitir aos nossos olhos apenas aqueles comprimentos de ondas
não absorvidos(HARRIS, 2005).
MATERIAL E MÉTODOS: A Casca do Barbatimão (Stryphnodendron barbatiman Mart) foi adquirida no centro
da cidade de Escada/PE, em feira livre, selecionada por aspectos livres de
contaminação, seguindo o planejamento fracionário delinear 26-2, com 16 ensaios,
com 4 variáveis independente : solvente - álcool (-1) e água (+1), concentração
– 15 g / 50 mL (-1) e 30 g / 50 mL (+1), aquecimento - T ambiente (-1) e com T
40ºC (+1), e tempo de imersão - 30 minutos (-1) e 60 minutos (+1) e as
correlações de respostas: SC, SA, ST, CA, CT, AT, SCA, SCT e SCAT . Foram
adquiridas no mesmo dia do processamento, as sementes, pesadas 10 g em balança
semi analítica (Marca Quimis – BG2000) para cada ensaio, trituradas em
almofariz. Para os ensaios com temperatura de 40º C foi utilizado o banho-maria
(Marca Quimis) e termômetro para o controle da temperatura. As Células de
extração (FIGURA 1a) foram fabricadas com garrafas PET de 250 mL (FIGURA 1c) e
tela (FSI - BNMO 200 µ 60X50). Foi monitorado o pH de cada ensaio, com fita
indicador Merck e o resíduo seco a temperatura solar e armazenado para
tratamento posterior. Após cada ensaio o extrato foi armazenado em frasco de
vidro de 100 mL (FIGURA 1b) e conservado a 5ºC para analise em Espectrofotômetro
UV-VISISVEL (UV-VIS spectrophotometer) (marca Thermo Scientific e modelo Genesys
10s).
RESULTADOS E DISCUSSÃO: Na otimização do processamento da extração de substâncias orgânicas utilizando a
casca de babartimão. Foi utilizado o planejamento fracionário delinear 26-2, com
16 ensaios, com 4 variáveis independente : solvente - álcool (-1) e água (+1),
concentração – 15 g / 50 mL (-1) e 30 g / 50 mL (+1), aquecimento - T ambiente
(-1) e com T 40ºC (+1), e tempo de imersão - 30 minutos (-1) e 60 minutos (+1),
para as sementes de urucum. O melhor processo de extração para o álcool foi no
ensaio 2 no processamento álcool, 30 g / 50 mL, 40°C e 60 minutos e para a água
foi no ensaio 9, no processamento água, 30 g / 50 mL, 40°C e 30 minutos(FIGURA
2). Todas as extrações ocorreram no comprimento de onda: 190 a 500 nm. A
Extração com temperatura a 40º C e ambiente realizada com álcool promoveu a
extração de substâncias polares, tendo em vista, a polaridade do álcool.
Resultado similar ocorreu na pesquisa de Corantes naturais como indicadores de
pH foi utilizado várias substâncias como solventes: Água, Álcool, Acetona e
Dicloroetano com bons resultados para todos os solventes (DIAS, GUIMARÃES &
MERÇON, 2003). O melhor solvente foi o álcool para todos os processamentos
(FIGURA 2).
FIGURA 1

Figura 1. (a)Célula de Extração; (b) Armazenamento
do Extrato e (c) Ensaios processados.
FIGURA 2
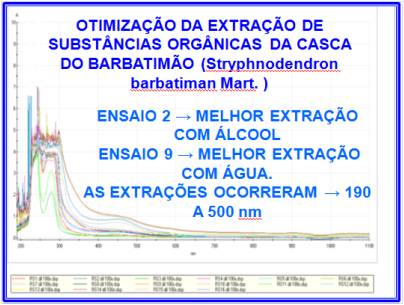
OTIMIZAÇÃO DO PROCESSO DE EXTRAÇÃO DE SUBSTÂNCIAS
ORGÂNICAS UTILIZANDO A CASCA DO BARBATIMÃO PARA O
PLANEJAMENTO FRACIONÁRIO DELINEAR 26-2.
CONCLUSÕES: Nas condições que esta pesquisa foi desenvolvida constatamos que partindo de
materiais de baixo custo, é possível a realização de extrações de substâncias
orgânicas utilizando as casca do Barbatimão de forma bastante satisfatória. O
melhor processo de extração para o álcool foi no ensaio 2 (no processo álcool,
30g/50mL, 40°C e 60 minutos) e para a água foi no ensaio 9, no processo água,
30g/50mL, 40°C e 30 minutos. Todas as extrações ocorreram no comprimento de onda:
190 a 500 nm. A extração nestas condições de processamento apresentou-se viável e
econômico.
AGRADECIMENTOS: Escola Técnica Estadual Luís Dias Lins (ETELDL-PE), Programa de Pós-Graduação em
Engenharia Química - DEQ-UFPE.
REFERÊNCIAS BIBLIOGRÁFICA: DIAS, M. V., GUIMARÃES, P. I. C., MERÇON, F. Corantes naturais como indicadores de pH. Química Nova na Escola, n° 17, maio 2003.
HARRIS, C Daniel. Análise Química Quantitativa. Fundamentos da Espectrofotometria. 6ª ed. Rio de Janeiro: LTC, 2005. P. 398-423.
SOLOMONS, T.W.G.; FRYHLE, C.B. Química Orgânica. 7. ed. Rio de Janeiro: LTC, 2002. 474 p
www.seagri.ba.gov.br.
