Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Química Analítica
TÍTULO: Determinação do Teor de Ácido Ascórbico pelo Método de Tillmans em Polpas de Frutas.
AUTORES: Nascimento, J.M.C. (UFRN) ; Moura, M.F.V. (UFRN) ; Fonseca, P.A.Q. (UFRN) ; Cruz, A.M.F. (UFRN) ; Soares, J.C. (UFRN)
RESUMO: As vitaminas são moléculas que funcionam como catalisadores no organismo. O
ácido ascórbico é uma molécula muito instável, pois reage com o oxigênio do ar e
com a luz. Previne principalmente gripes e resfriados. O trabalho teve como
objetivo determinar o teor de ácido ascórbico através da titulação pelo Método
de Tillmans que se baseia na redução do sal 2,6-diclorofenol por uma solução
ácida de vitamina C, o método mostrou-se bastante satisfatório, pois pode ser
analisado o teor de ácido ascórbico contido em cada amostra titulada que foi
21,98; 30,44; 38,22; 28,75 e 21,31 mg/100g para as polpas de seriguela, umbu,
cajá, morango e cupuaçu, respectivamente, o que leva a concluir que a cada 100 g
de polpa de fruta obtêm-se em média 50% de vitamina para o consumo diário da
população em geral.
PALAVRAS CHAVES: ácido ascórbico; Tillmans; vitamina C
INTRODUÇÃO: A indústria de polpas de frutas congeladas tem se expandido bastante nos últimos
anos. As unidades processadoras se compõem, em sua maioria, de pequenos
produtores, dos quais, grande parte ainda utiliza processos artesanais.
O processamento de frutas para obtenção de polpas é uma atividade agroindustrial
importante, na medida em que agrega valor econômico à fruta, evitando
desperdícios e minimizando perdas que podem ocorrer durante a comercialização do
produto in natura.
O ácido ascórbico é uma substância orgânica simples que tem despertado grande
interesse, devido aos efeitos benéficos como vitamina, além de seu grande uso
como reagente e como aditivo em alimentos. Em vista disso, pesquisas têm sido
realizadas na tentativa de se propor novos métodos de determinação. De ácido
ascórbico. A Indeterminação do conteúdo de ácido ascórbico em vegetais é muito
importante, pois além de seu papel fundamental na nutrição humana, sua
degradação pode favorecer o escurecimento não enzimático, e causar aparecimento
de sabor estranho ao alimento. A vitamina C é solúvel em água e qualquer excesso
é excretado pela urina. Ela é encontrada em frutas e vegetais, especialmente em
frutas cítricas, tomates, espinafre, batatas e brócolis. Ela é facilmente
destruída por calor e luz, portanto esses alimentos devem ser armazenados em
local fresco e escuro e preparados de maneira mais rápida possível.
O presente trabalho tem como objetivo determinar a quantidade de vitamina C
presente nas polpas de frutas de cajá, seriguela, umbu, cupuaçu e morango a fim
de verificar qual fruta é mais rico ou mais pobre em vitamina C e também
discutir os riscos que podem ser causados pela falta dessa vitamina ao organismo
da população em geral.
MATERIAL E MÉTODOS: Neste trabalho de determinação do teor de ácido ascórbico presente em polpas de
frutas, todos os experimentos foram realizados no Instituto de Química da UFRN.
Os materiais e equipamentos utilizados neste trabalho foram: microbureta;
dessecador; papel de filtro; pipetas volumétricas de 1, 4 e 10 mL; pipetas
graduadas de 5 e 10 mL; provetas de 50, 100, 200 e 500 mL; béqueres de 50 e 100
mL; erlenmeyer de 250 mL; balões volumétricos de 100 e 200 mL; funil de vidro;
bastão de vidro; balança analítica (B-TEC-210A) e freezer (FRICON).
Os reagentes utilizados neste trabalho foram: 2,6-diclorofenol indofenol; Ácido
Ascórbico; Bicarbonato de sódio; ácido acético; ácido metafosfórico; sal sódico
do 2,6-diclorofenol indofenol; solução de azul de metileno (0,05%); solução de
vitamina C (padrão); solução de Tillmans; solução de ácido acético e solução
diluída de Vitamina C (10%), iodeto de potássio, solução de tiossulfato de
sódio, solução de iodato de potássio, solução de amido.
A determinação de ácido ascórbico utilizada neste trabalho foi baseada no Método
de Tillmans, conforme descrito nas Normas Analíticas do Instituto Adolfo Lutz.
Este método é indicado para amostras com baixo teor de vitamina C, baseia-se na
redução do sal sódico de 2,6-diclorofenol indofenol por uma solução ácida de
vitamina C.
Para que seja possível determinar o teor de vitamina C é necessário fazer o
cálculo do fator (F) da solução de Tillmans conforme a relação:
F = mg de vitamina C usados na titulação / mL da solução de Tillmans gastos
Após obter o valor do fator (F), calcula-se o teor de ácido ascórbico,
relacionado a seguir:
V x F x 100 / A = ácido ascórbico mg/100 mL
V = volume da solução de Tillmans gasto na titulação.
F = fator da solução
A = mL da amostra utilizada.
RESULTADOS E DISCUSSÃO: Após a padronização da solução de Tillmans, titulou-se as amostras a partir de
uma alíquota de 10 mL da solução contendo polpa de fruta e a solução ácida na
proporção de 1:1 em erlenmeyer de 250,0 mL contendo 4,0 mL da solução de
vitamina C diluída, 6,0 mL da solução ácida e 50,0 mL de água, repetiu-se três
vezes esse mesmo procedimento para cada amostra de seriguela, umbu, cajá,
morango e cupuaçu. Assim, obteve-se os seguintes valores na titulação, conforme
Tabela 1.
A partir dos valores obtidos pode-se calcular o teor de ácido ascórbico,
relacionado a seguir, e obteve-se a Tabela 2 e a Figura 3 com os resultados do
teor de ácido ascórbico em cada tipo de amostra, conforme a relação a seguir:
V x F x 100/ A = ácido ascórbico mg/100 mL.
A amostra de cajá apresentou o maior teor de ácido ascórbico (38,22 mg/100g),
entretanto, seriguela e cupuaçu apresentaram os menores teores de ácido
ascórbico, 21,98 mg/100g e 21,31 mg/100g, respectivamente.
Resultados obtidos na titulação com solução de Tillmans.
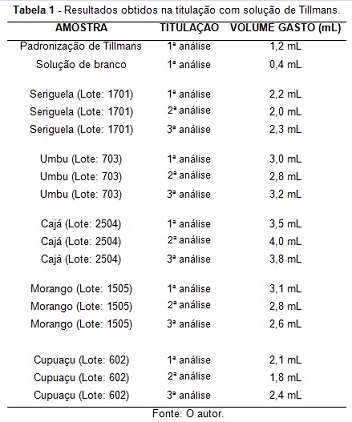
Valores, em triplicata, para cada polpa de
seriguela, umbu, caja, cupuaçu e morango.
Teores de ácido ascórbico nas polpas de frutas.

Tabela e gráfico com os resultados dos teores de
ácido ascórbico nas polpas de frutas.
CONCLUSÕES: O Método de Tillmans mostrou-se bastante eficaz. Os resultados permitiram concluir
que o teor de ácido ascórbico contido nas amostras está em conformidade com a
Regulamentação da ANVISA que específica valores em torno de 25 á 45 mg/diário para
o consumo humano. O teor de ácido ascórbico contido em cada amostra foi 21,98,
30,44; 38,22; 28,75 e 21,31 mg/100 g para as polpas de seriguela, umbu, cajá,
morango e cupuaçu, respectivamente, conclui-se que para cada 100 g de polpa de
fruta obtêm-se em média 50 % de vitamina C considerando o teor ácido ascórbico
diário para um adulto sadio.
AGRADECIMENTOS: Agradeço primeiramente a Deus, a todos os meus familiares, a minha orientadora, a
Fábrica Delícia da Fruta e a todos os meus colegas de laboratório.
REFERÊNCIAS BIBLIOGRÁFICA: PEREIRA, J. M. A. T. K.; OLIVEIRA, K. A. M.; SOARES, N. F. F.; GONÇALVES; M. P. J. C. Avaliação da qualidade físico-química, microbiológica e microscópica de polpas de frutas congeladas comercializadas na cidade de Viçosa-MG. Alimentação Nutricional, Araraquara, v.17, n.4, p.437-442, out./dez. 2006.
ARANHA, F. Q.; BARROS, Z. F.; MOURA, L. S. A., O Papel da Vitamina C Sobre as Alterações Orgânicas no Idoso. Revista Nutricional, Campinas-SP, pg. 89-97, maio, 2000.
INSTITUTO ADOLFO LUTZ. Normas Analíticas do Instituto Adolfo Lutz. V.1 Métodos químicos e físicos para análise de alimentos. 3 ed. São Paulo-SP, 1985.
BRASIL. Resolução RDC n. 12, de 02 de janeiro de 2001, da Agência Nacional de Vigilância Sanitária. Diário Oficial [da] República Federativa do Brasil, Brasília, DF, 10 jan. 2001. Seção 1, p.45-53.
GUILLAND, J.C., LEQUEU, B. As vitaminas do nutriente ao medicamento. São Paulo; Santos, 1995.
STADLER, Z., Determinação do Teor de Vitamina C em Alimentos. Curitiba, Monografia apresentada ao Curso de Especialização em Ensino de Química Experimental, Universidade Federal do Paraná - PR. 1999.
PAULING, L., Como viver mais e melhor: o que os médicos não dizem sobre sua saúde. 4.ed. São Paulo : Best Seller, 1988.
CÂNDIDO, L.M.B., CAMPOS, A.M. Alimentos funcionais: uma revisão. Boletim da Revista Brasileira de Ciência e Tecnologia de Alimentos, São Paulo, v.29, n.2.
MARCUS, R., COULSTON, A.M. Vitaminas hidrossolúveis. In: GILMAN, A.G., ROLL, T.W., NIES, A.S. As bases farmacológicas da terapêutica. 8.ed. Rio de Janeiro. Guanabara, 1991. p.1017-1032.
BENDICH, A., LANGSETH, L. The health effects of vitamin C supplementation: a review. American Journal of Clinical Nutrition, Bethesda, v.14, n.2, p.124-136, 1995.
PADH, H. Vitamin C: never insights into its biochemical functions. USA, v.49, 1991.
FRANCO, G. Tabela de composição química dos alimentos. 9.ed. São Paulo, 1992.
ARMSTRONG, L.E., MARESH, C.M. Vitamin and mineral supplements as nutricional aids to exercise performance and health. Nutrition Reviews, New York, v.54,1996.
