Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Físico-Química
TÍTULO: Síntese de Hidrixissais Lamelares e sua aplicação na Adsorção do Corante Alaranjado de Metila
AUTORES: Olieveira, C. (UNIVERSIDADE ESTADUAL DO CENTRO OESTE UNICENTRO)
RESUMO: O descarte inapropriado de corantes sintéticos utilizados em indústria têxteis
causa um grande risco ambiental, além de graves problemas à saúde humana. Devido
a esses fatos a remoção dos efluentes industriais é extremamente importante.
Entre os vários métodos utilizados para a despoluição de efluentes, o processo
de adsorção tem se destacado especialmente pela utilização de materiais de baixo
custo. A adsorção se baseia na capacidade de diversos sólidos em concentrar em
sua superfície certas substâncias provenientes de soluções aquosas, formando uma
ligação do tipo física ou química. Dentre estes sólidos estão os hidroxissais
lamelares (HSL’s), que são utilizados por apresentar porosidade e grande área
superficial que torna os HSL’s adsorventes potenciais.
PALAVRAS CHAVES: Adsorção; Hidroxissal Lamelar; Alaranjado de Metila
INTRODUÇÃO: O amplo uso de corantes em algumas indústrias (alimentícia, papeis, têxteis,
etc.) produzem elevadas quantidades de águas resíduas. Essas águas são
conhecidas pela abundância de sólidos suspensos, elevadas quantidades de sais e
compostos orgânicos, baixo potencial de biodegradação e coloração intensa. O
descarte direto de contaminantes coloridos causa, em muitos casos, o que
chamamos de poluição estética, a luz solar é impedida de penetrar no fluxo da
água, afetando o equilíbrio do sistema aquático.
Entre os vários métodos utilizados para a despoluição de efluentes, o
processo de adsorção tem se destacado especialmente pela utilização de materiais
de baixo custo. A adsorção se baseia na capacidade de diversos sólidos em
concentrar em sua superfície certas substâncias provenientes de soluções
aquosas, formando uma ligação do tipo física ou química. Dentre estes sólidos
estão os hidroxissais lamelares, que são utilizados por apresentar porosidade e
grande área superficial que os torna adsorventes potenciais. Os hidroxissais têm
uma estrutura porosa bem desenvolvida e a alta capacidade de adsorção está
associada principalmente com a distribuição de tamanho de poros, área
superficial e volume de poros.
Esse trabalho tem como objetivo investigar os fatores que afetam a
adsorção do corante aniônico alaranjado de metila (AM) em um hidroxissal lamelar
(HSL’s).
MATERIAL E MÉTODOS: Síntese do hidroxissal lamelare, é uma preparação simples que consiste em um
sistema de agitação com a adição ao mesmo tempo de uma solução de sais
[(Zn(NO3)2] e uma solução alcalina (NaOH), acompanhada por um controlador de pH
entre (5-7). A sua formação é rápida, em aproximadamente em 4h, e de baixo
custo.
O adsorvente preparado foi usado para adsorção do corante Alaranjado de Metila,
que apresenta massa molar igual a 327,33 g.mol-1. Foi utilizado para determinar
a capacidade da adsorção do hidroxissal lamelar.
Os testes de adsorção foram realizados, utilizando 0,1g de adsorvente e 50 mL de
solução de alaranjado de metila em 5 concentrações distintas, no intervalo de
0,4 g.L-1 a 0,8 g.L-1, por um período de 4h. Com agitação constante de 450 rpm e
em três temperaturas distintas (25, 45 e 60ºC). Alíquotas foram retiradas em
tempos pré-determinados, diluídas e então analisadas no espectrofotômetro
UV/visível..
A quantidade adsorvida do corante foi obtida pela equação:
q_e=(C_0- C_e)/m V (1)
Onde qe (mg g-1) é a quantidade adsorvida, C0 (mg L-1) a concentração final, Ce
a concentração final, m a massa (g), V o volume (L).
RESULTADOS E DISCUSSÃO: A Figura 2 mostra o efeito do tempo de contato na adsorção das moléculas do AM
no
adsorvente HSL a 25ºC. A adsorção do AM, em diferentes concentrações iniciais,
não
sofreu qualquer influencia no efeito do tempo de contato. O sistema alcançou o
equilíbrio em torno de 0,5 horas para todas as concentrações (400 – 800 mg L-1).
Adsorção de AM independe da concentração inicial sob o tempo de contato ao
atingir
o equilíbrio. Obtiveram-se resultados semelhantes nas temperaturas de 45ºC e
60ºC.
A quantidade de AM adsorvida no tempo (qt) foi obtida a partir da Equação 1
A quantidade adsorvida de AM foi diretamente proporcional à concentração
inicial, conforme mostrado na Figura 3. O contrário ocorre com a porcentagem
(diminui com o aumento da concentração inicial). Em concentrações baixas de AM,
os sítios ativos do adsorvente são ocupados sem nenhum impedimento, pois não há
competitividade entre as moléculas do AM pelos mesmos. Nos pontos de 400 e 500
mg L-1 as porcentagens de remoção foram de 100%, pois as moléculas do corante
foram atraídas e adsorvidas com facilidade pelos sítios ativos. Já em elevadas
concentrações essa competição aumenta. Devido a presença de outras moléculas já
adsorvida nas vizinhanças, as moléculas vão sendo atraídas pelos sítios ativos
disponíveis com mais dificuldade; efeito esse conhecido como impedimento
estérico. A capacidade máxima de adsorção da HSL foi de 281 mg g-1 a 25ºC
indicando a ocupação total dos sítios ativos disponíveis que foi obtida a partir
de C0 = 700 mg L-1, ocasionando a saturação do adsorvente. Em temperaturas mais
elevadas (45ºC e 60ºC) o comportamento observado no efeito da concentração
inicial foi semelhante ao obtido em 25ºC, com valores da capacidade de adsorção
máxima distintos
figura 1
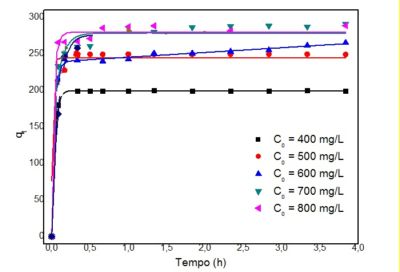
Efeito do tempo de contato na adsorção do AM a 25°C
Figura 2
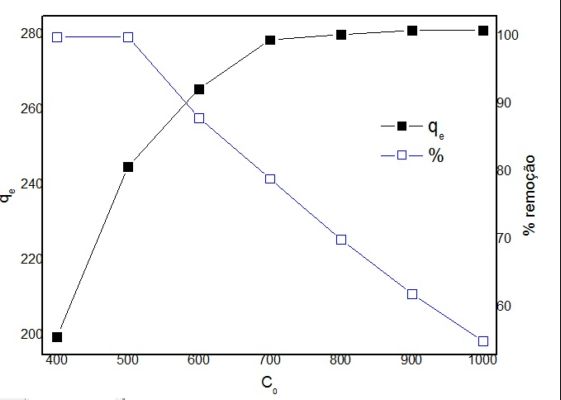
Efeito da concentração inicial na adsorção do AM à
25ºC.
CONCLUSÕES: Os estudos da adsorção do alaranjado de metila com o HSL’s apresentaram uma grande
capacidade de adsorção, quando comparado com resultados obtidos em outros
trabalhos presentes na literatura.
AGRADECIMENTOS: Ao laboratório LAPECI (laboratório de Pesquisa em Ciências Interfaciais) e a
UNICENTRO
REFERÊNCIAS BIBLIOGRÁFICA: ALKAN, M.; DOGAN, M.; TURHAN, Y.; DEMIRBAS, Ö; TURAN, P. Adsorption kinetics and mechanism of maxilon blue 5G dye on sepiolite from aqueous solutions. Chemical Engineering Journal, v. 139, p. 213-223, 2008.
ALMEIDA, C.A.P.; DEBACHER N.A.; DOWNS A.J.; COTTET L. MELLO C.A.D. Removal of methylene blue from colored effluents by adsorption on montmorillonite clay. Journal of Colloid and Interface Science, v. 332, p.46-53, 2009.
BULUT, E.; ÖZACAR, M.; SENGIL, A. Adsorption of malachite green onto bentonite: Equilibrium and kinetic studies and process design. Microporous and Mesoporous Materials, v. 115, p. 243-246, 2008.
CAGLAR, B.; AFSIN, B.; TABAK, A.; EREN, E. Characterization of the cation-exchanged bentonites by XRPD, ATR, DTA/TG analyses and BET measurement. Chemical Engineering Journal, v. 149, p. 242-248, 2009.
DOGAN, M.; ALKAN, M. Adsorption kinetics of methyl violet onto perlite. Chemosphere, v. 50, p. 517-528, 2003.
DOGAN, M.; ÖZDEMOI, Y.; ALKAN, M. Adsorption kinetics and mechanism of cationic methyl violet and methylene blue dyes onto sepiolite. Dyes and Pigments, v. 75, p. 701-713, 2007.
FREUNDLICH, H. M. F. Über die adsorption in lösungen. Z. Phys.Chem., v.57, p. 385-470, 1906.
HAJJAJI, M.; ALAMI, A. Influence of operating conditions on methylene blue uptake by a smectite rich clay fraction. Applied Clay Science, v. 44, p.127-129, 2009.
