Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Físico-Química
TÍTULO: ESTUDO DE ELETROCATALISADORES DE COBALTO PARA REAÇÃO DE ETANOL EM MEIO ÁCIDO
AUTORES: Miranda, I.S. (UFPA) ; Silva, U.L.V. (UFPA) ; Soares, A.M.S. (UFPA) ; Rocha, J.A.P. (UFPA) ; Quadros, F.M. (UFPA)
RESUMO: Estudo de eletrocatalisadores de cobalto para reação de etanol em meio ácido,
mostra o desempenho deste eletrocatalisador frente a eletro-oxidação do álcool.
Para realização destes estudos foram primeiramente sintetizados, através do método
de síntese via boro-hidreto, catalisadores de Pt/C e Co/C suportados nas
porcentagens de 20%, 40% e 60% em massa de metal/carbono para ambos
eletrocatalisadores, foram então empregados estudos de Voltametria Cíclica e
Cronoamperometria com o objetivo de encontrar área eletroquimicamente ativa e
corrente de oxidação, respectivamente. Os resultados mostram que o cobalto
apresentou baixa corrente para reação de oxidação do etanol, se este metal for
comparado com desempenho da platina.
PALAVRAS CHAVES: cobalto; etanol; eletrocatalisador
INTRODUÇÃO: A célula a combustível de etanol direto (DEFC), são dispositivos em que o
combustível utilizado no reservatório do ânodo é o etanol líquido. As DEFCs
operam desde a temperatura ambiente até 100 ºC onde oxidam o combustível
líquido, não tóxico e de fácil armazenamento (LOPES et al, 2006).
No caso do Brasil, estudos quanto à utilização de etanol, aplicados diretamente
em células a combustível, são bastante importantes, pois o etanol é produzido em
grandes quantidades, sendo de fácil armazenamento e distribuição (NETO et al,
2006). No entanto, apesar das vantagens do etanol, a sua oxidação direta na
célula a combustível é lenta devido à dificuldade de quebra da ligação C–C
(cerca de 347 kJ mol-1), outro fator negativo é a desativação ou envenenamento
do catalisador pela formação de intermediários fortemente adsorvidos *(ZHOU et
al, 2005). O trabalho estudado visa comparar o desempenho de eletrocatalisadores
de cobalto suportados com eletrocatalisadores de platina, os quais são comumente
usados nas células a combustível, através da eletro-oxidação destes metais em
meio ácido e em meio ácido na presença de um álcool.
MATERIAL E MÉTODOS: A síntese dos catalisadores foi realizada pelo método de redução via adição de
boro-hidreto de sódio. Neste método, primeiramente foram preparados uma solução
contendo 0,03g de carbono Vulcan XC-72, 8 ml de H2O ultra-pura, 2 ml de
isopropanol e os sais precursores (CoCl2.6H2O para Co/C e H2PtCl2.6H2O para o
Pt/C) em diferentes proporções, em seguida na foi adicionado solução de NaOH 0,1
Mol/L para ajustar o pH para 8, e por fim a solução resultante foi colocada em
banho-maria ate alcançar 80°C e foi adicionado 20 ml do agente redutor (solução
1:50 m/v de NaBH4) onde aqueceu-se a mistura durante 1h. Os ensaios
eletroquímicos de voltametria e cronoamperometria foram realizados com um
potenciostato modelo AUTOLAB PGSTAT 302. Os voltamogramas cíclicos foram obtidos
em soluções de 0,5 Mol/L de H2SO4 saturados com nitrogênio, onde o
eletrocatalisador sintetizado foi ancorado, com 60 micro-Litros de material,
sobre um eletrodo de trabalho de carbono vitro, na célula teste. Durante o
experimento o fluxo de nitrogênio é deslocado para a superfície da solução e as
curvas voltamétricas são obtidas a uma determinada velocidade de varredura do
potencial (50 mV/s). As curvas cronoamperométricas foram obtidas durante 700
segundos com um potencial fixo de 0,05 Volts. As medidas de cronoamperometria
foram realizadas em uma mistura de 0,5 Mol/L de H2SO4 + 0,5 Mol/L de etanol.
RESULTADOS E DISCUSSÃO: Para os testes de voltametria e cronoamperometria foram comparados primeiramente
os eletrocatalisadores de cobalto suportados nas proporções de 20, 40 e 60% de
metal/carbono. Foi observado para as analises voltamétricas que o catalisador
Co/C 40% apresentou maior potencial eletroquímico e para as analises de
cronoamperometria o Co/C 60% apresentou maior corrente para reação de oxidação
do etanol. A segunda parte do trabalho avaliou comparativamente os catalisadores
de Pt/C suportados em diferentes proporções de 20, 40 e 60% de metal/carbono.
Nas analises voltamétricas o catalisador que teve maior potencial foi o Pt/C 40%
e para os resultados de cronoamperometria o catalisador Pt/C 60% foi o que
apresentou maior corrente para reação de oxidação do álcool. A parte final do
trabalho comparou os melhores resultados de voltametria e cronoamperometria para
o cobalto e a platina, é possível observar um baixo potencial do
eletrocatalisador de cobalto em relação a platina como mostrado nas FIGURAS 1 e
2, apesar da platina adsorver intermediários, acetaldeidos e ácidos
carboxílicos, formados durante a reação de acordo com ZHOU et al, 2005.
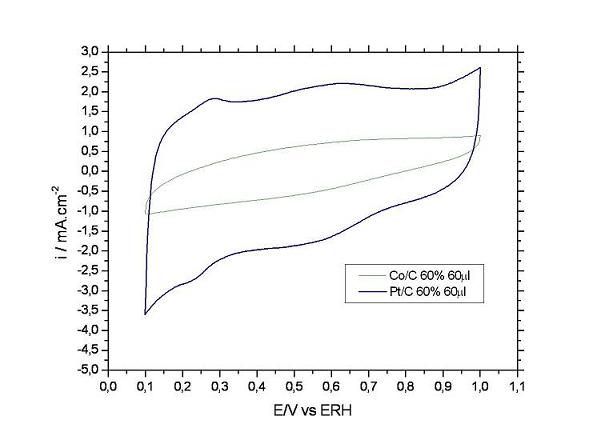
Figura 1. Voltamogramas cíclicos de Pt/C 60% e Co/C
60% em H2SO4 0,5Mol.L-1 com quantidades 60µl de
material sobre o eletrodo de trabalho (WE).
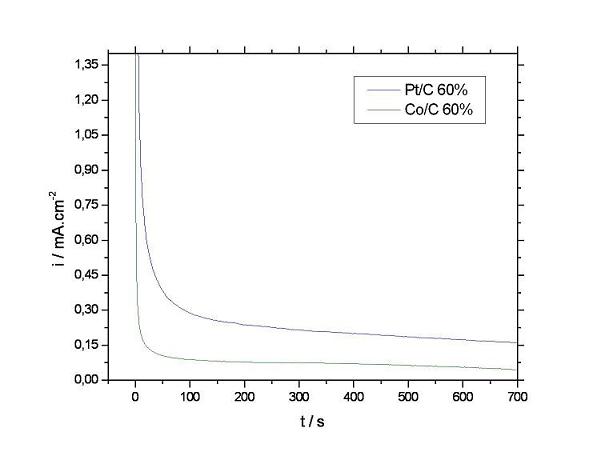
Figura 2. Curvas cronoamperometricas para eletro-
oxidação do etanol 0,5 M em H2SO4 0,5 M com
potêncial de 0,05V sobre eletrocatalisadores de Pt
e Co.
CONCLUSÕES: Apartir das avaliações eletroquímicas de voltametria e cronoamperometria, foi
possível observar que o catalisador de cobalto suportado apresentou semelhanças na
sua atividade eletroquímica com o da platina suportado, porém foi obtido um menor
potencial para o eletrocatalisador de Co/C, tanto em reações de adsorção/desorção
de hidrogênio em meio ácido, quanto na reação de oxidação do etanol em meio ácido,
o qual mostrou um baixo desempenho para uma possível utilização como DEFCs, porém
estudos nesta linha torna-se mais promissores a medida que os potenciais dos
eletrocatalisadores aumentarem.
AGRADECIMENTOS: A UFPA, ao Laboratório de eletroquímica e célula a combustível (LeCaC) e aos
amigos da universidade.
REFERÊNCIAS BIBLIOGRÁFICA: ZHOU, W. J.; SONG, S. Q.; LI, W. Z.; ZHOU, Z. H.; SUN, G. Q.; XIN, Q.; DOUVARTZIDES, S.; TSIAKARAS, P. Direct ethanol fuel cells based on PtSn anodes: the effect of Sn content on the fuel cell performance. Journal of Power Sources, v. 140, n. 1, p. 50-58, 2005.
NETO, A.O.; DIAS, R.R.; RIBEIRO, V.A.; SPINACÉ, E.V.; LINARDI, M. Eletro-oxidação de etanol sobre eletrocatalisadores PtRh/C, PtSn/C e PtSnRh/C preparados pelo método da redução por álcool. Eclética Química, v.31, n. 1, p. 81-88, 2006.
LOPES, T.; COLMATI, F., GONZALEZ, E. R. Estudo de células a combustível de etanol direto utilizando catalizadores de PtRu no ânodo e PtCo no cátodo. São Carlos-USP. 2006, 29º Reunião anual da SBQ.
