Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Iniciação Científica
TÍTULO: SÍNTESE E ELUCIDAÇÃO ESTRUTURAL DE NOVOS 1,2,4-OXADIAZÓIS OBTIDOS POR DIFERENTES METODOLOGIAS
AUTORES: Regueira, J. (UFRPE) ; Silva, E. (UFRPE) ; Freitas Filho, J. (UFRPE)
RESUMO: 1,2,4-oxadiazóis são compostos que têm atraído a atenção de muitos pesquisadores
devido às suas aplicações tanto na área de materiais como em química medicinal.
Neste trabalho descreve-se três metodologias (A, B e C) potencialmente
adaptáveis para a síntese de seis novos 3-aril-[1,2,4-oxadiazol-5-il]-propan-2-
ona (3a-f). Na metodologia A, a mistura reacional, sem qualquer solvente e na
ausência de base, foi submetida ao aquecimento direto. Na metodologia B, a
mistura foi submetida à irradiação em forno de microondas. E Finalmente, na
metodologia C, a arilamidoxima (1a-f) reagiu com o éster (2) durante 18h horas,
sob refluxo, utilizando base, DMF e Tolueno. As estruturas dos compostos foram
caracterizadas por ressonância magnética nuclear (RMN 1H e 13C) e espectroscopia
de infravermelho.
PALAVRAS CHAVES: 1,2,4-oxadiazol; Aquecimento; Elucidação Estrutural
INTRODUÇÃO: Os 1,2,4-oxadiazóis são compostos cíclicos que apresentam dois heteroátomos de
nitrogênio e um de oxigênio em sua estrutura. Estes heterociclos são bastante
relatados na literatura. Desde os primeiros trabalhos tratando da síntese e das
propriedades biológicas dos oxadiazóis, oito trabalhos de revisão já foram
publicados. Esses compostos têm atraído a atenção de muitos pesquisadores devido
às suas aplicações tanto na área de materiais como em química medicinal. A
primeira síntese de 1,2,4-oxadiazóis foi realizada em 1884 pelos pesquisadores
Tiemann e Krüger, os quais nomearam estes heterociclos como
furo[ab1]diazóis,devido a sua semelhança com o anel furano. Porém, o interesse
por este composto só se deu a partir 1950, principalmente devido à tendência dos
1,2,4-oxadiazóis de sofrerem rearranjos moleculares. Na década de 60, pelos
menos três oxadiazóis ganharam popularidade como drogas terapêuticas: oxolamina
e a libexina que apresentam ação antitussígena, e o irrigor, que tem ação
vasodilatadora das artérias coronárias e anestésico local. A utilização do
1,2,4-oxadiazol vem se destacando também na síntese de novos materiais
funcionais, pois permite a modificação na geometria e polarização molecular,
apresenta uma distribuição não-simétrica dos heteroátomos, resultando na
formação de momentos de dipolo longitudinais e aumentando as interações
laterais. Foram relatados alguns 1,2,4-oxadiazóis com propriedades de cristais
líquidos, líquidos iônicos e propriedades fotoluminescentes. Devido à
importância biológica dos 1,2,4-oxadiazóis, descrita acima, o presente trabalho
tem como objetivo sintetizar seis novos 3-aril-[1,2,4-oxadiazol-5-il] propan-2-
ona (3a-f) através de duas metodologias.
MATERIAL E MÉTODOS: Nas reações, utilizou-se reagentes e solventes, na sua forma comercial, p.a. O
acompanhamento das reações foi feito através de cromatografia em camada delgada
(ccd), onde o solvente usado para correr a placa foi CH2Cl2/AcOEt (9:1). Para
visualização dos compostos usamos lâmpada de ultravioleta. Para cromatografia em
coluna utilizamos sílica-gel 60 (Merck, 70 – 230 mesh). Os espectros de RMN 1H e
RMN 13C foram obtidos em espectrofotômetro VARIAN modelo Unity Plus (300 MHz e
75 MHz), usando CDCl3 como solvente e tetrametilsilano como padrão interno.
Espectros de infravermelho (IV) foram obtidos em espectrofotômetro de IV com
Transformada de Fourier no instrumento BRUKER Modelo IFS 66, em pastilha de KBr.
O microondas utilizado foi doméstico da marca Panasonic, modelo NN-5SSBK (220;
900W/2450 MHz). Para concentrar as soluções orgânicas foram utilizados
evaporadores rotatórios do modelo IKA-WERK operando a pressão reduzida.
RESULTADOS E DISCUSSÃO: A síntese 3-aril-[1,2,4-oxadiazol-5-il] propan-2-ona (3a-f), foi realizada
utilizando três metodologias (Esquema 1) e consistiu em reagir diferentes
arilamidoximas (Ar: fenil, m-toluil p-toluil, p-clorofenil, p-bromofenil, p-
nitrofenil), separadamente, com o acetoacetato de etila. Na metodologia A, a
mistura reacional foi submetida a aquecimento direto em banho de óleo, a uma a
temperatura de 110 0C, sem qualquer solvente e na ausência de base. Na
metodologia B, o composto 1a-f reage com o composto 2 na presença do Carbonato
de Potássio e uma gota de DMF (Dimetilformamida), que é o solvente polar
aprótico utilizado para aumentar a velocidade de reação nas reações de
microondas, produzindo o composto 3a-f. As metodologias, descritas acima,
forneceram os produtos com duração de 4 horas e 8 min, respectivamente e uma
química ambientalmente limpa. Na metodologia C, as arilamidoximas (1a-f)
reagiram, separadamente, com -ceto ésteres (2) durante 18h horas, sob refluxo,
utilizando solvente (tolueno e DMF) e na presença da base do K2CO3. Nas três
metodologias utilizadas os produtos foram obtidos em rendimentos moderados e
bons (Tabela 1).
As estruturas dos novos compostos foram comprovadas através dos espectros de
infravermelho, de RMN 13C e RMN 1H. A análise do espectro de RMN’1H do composto
3a, mostra que há um simpleto na região de aproximadamente 2,3o ppm referente
aos hidrogênios grupo metila. Os hidrogênios metilênicos como um simpleto na
região de 4,10 ppm. Na região entre 7,00 e 8,50 ppm aparecem picos
característicos dos hidrogênios do anel aromático. No espectro de RMN13C
observou-se um sinal em 199,34 ppm referente ao carbono da carbonila, bastante
desblindado. Os carbonos do anel oxadiazólico aparecem na região 173,39 ppm e
168,98 ppm respectivamente.
Esquema 1:

Síntese de 3-aril-[1,2,4-oxadiazol-5-il]-propan-2-
ona
Tabela 1:
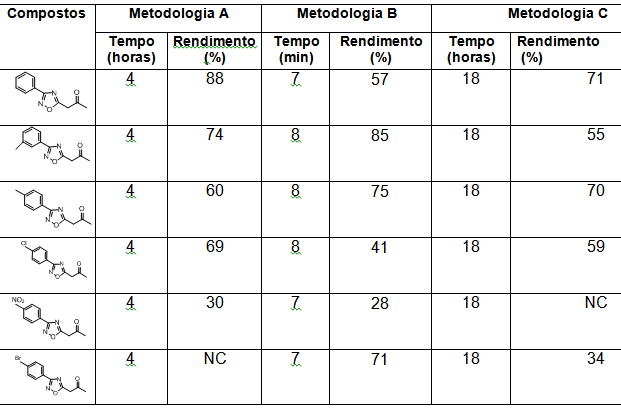
Rendimentos e tempo de reação dos 1,2,4-oxadiazóis
nas diferentes metodologias usadas.
CONCLUSÕES: As metodologias utilizadas se constituem em métodos simples e eficientes para a
síntese de seis novos 3-aril-[1,2,4-oxadiazol-5-il]-propan-2-ona (3a-f), a partir
de diferentes arilamidoximas(1a-f) e do acetoacetato de etila (2), em presença ou
ausência de carbonato de potássio (K2CO3), na ausência ou presença de solvente,
sob aquecimento direto ou refluxo ou irradiação em forno de microondas. Nas três
metodologias os rendimentos foram moderados e bons. As estruturas dos compostos
foram caracterizadas por ressonância magnética nuclear (RMN 1H e RMN 13C) e
espectroscopia de infravermelho.
AGRADECIMENTOS: Agradecemos à CAPES pela bolsa de mestrado (E. E. da Silva) e ao CNPq pela bolsa
de iniciação científica (J. L. L. F. Regueira).
REFERÊNCIAS BIBLIOGRÁFICA: 1 CLAPP, L.B., Advances In Heterocyclic Chemistry, Katritzky, A.R., Ed., Academic Press, New York, 1976, 20, 65
2 TIEMANN, F; KRÜGER, P. Ber., 1984, 17, 1685.
3BOYER, J. H. Heterocyclic Compounds (Elderfield, R. C., Ed), Wiley, New York, 1962, 7, 462
4ELOY, F.; LENAERS, R. Helv Chim Acta., 1966, 49,1430.
5 Parra, M. L; Hidalgo, P. I.; Elgueta, E. Y. Liq. Cryst. 2008, 35, 823.
6Pibiri, I.; Pace, A.; Piccionello, A. P.; Pierro, P; Buscemi, S. Heterocycles 2006, 68, 2653.
7Buscemi, S.; Pace, A.; Piccionello, A. P. Vivona, N. J. Fluorine Chem. 2006, 127, 1601.
