Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Iniciação Científica
TÍTULO: UM ESTUDO AB INITIO SOBRE AS PROPRIEDADES ESTRUTURAIS E ENERGÉTICAS DOS COMPLEXOS ENVOLVENDO FTALIMIDA E RCOOH (R=-H, -CH3 E –C6H5)
AUTORES: Handrezy Silvério da Silva, H. (UNIVERSIDADE FEDERAL DE PERNAMBUCO) ; Bezerra de Lima, N. (UNIVERSIDADE FEDERAL DE PERNAMBUCO)
RESUMO: Neste trabalho, tivemos como objetivos calcular as geometrias mais estáveis de
complexos envolvendo a ftalimida e ácidos carboxílicos (ácido fórmico, ácido
acético e ácido benzoico), bem como as mudanças nas propriedades estruturais e
energéticas devido à formação da ligação de hidrogênio. Para o desenvolvimento
deste trabalho, empregamos cálculos ab inito com o método B3LYP/6-31++G(d,p),
utilizando o programa de química quântica Gaussian 2003. Três estruturas estáveis
foram encontradas, nas quais duas possíveis ligações de hidrogênio foram formadas
(NH···OC e CO···HO), formando assim um quasi ciclo de oito membros. O processo
de formação das ligações de hidrogênio resultou no aumento do comprimento de todas
as ligações diretamente envolvidas nela.
PALAVRAS CHAVES: ab initio; ligação de hidrogênio; ftalimida
INTRODUÇÃO: As ftalimidas são moléculas orgânicas que possuem a capacidade de
reduzir taxas de colesterol e triglicerídeos do sangue [1-3]. Resultados
experimentais mostram que a ação hipolipidêmica da ftalimida provavelmente está
associada à planaridade do anel de cinco membros. Por exemplo, substituindo uma
das carbonilas da ftalimida por um grupo –CH2 transformando-a assim em
ftalimidina, produz uma redução substancial na atividade hipolidêmica.
Resultados obtidos através de cálculos computacionais revelaram que a atividade
hipolidêmica da ftalimida pode ser explicada em termos da energia do orbital
molecular LUMO e pela polaridade dos grupos C=O.
As propriedades eletrônicas das ftalimidas nos levaram a perguntar sobre os
efeitos de uma complexação, via ligação de hidrogênio envolvendo as carbonilas e
o grupamento N-H, em termos de suas propriedades estruturais e energéticas.
Motivados por essa questão, nosso trabalho teve como objetivos calcular as
geometrias mais estáveis de complexos envolvendo a ftalimida e ácidos
carboxílicos (ácido fórmico, ácido acético e ácido benzoico), bem como as
mudanças nas propriedades estruturais e energéticas devido a formação da ligação
de hidrogênio.
MATERIAL E MÉTODOS: Para o desenvolvimento deste trabalho, empregamos cálculos de orbitais moleculares
com a teoria do funcional de densidade (DFT)[4] com o funcional B3LYP[5] com o
conjunto de funções de base 6-31++G(d,p)[6]. Para isto, utilizamos o programa de
química quântica computacional GAUSSIAN 03.
RESULTADOS E DISCUSSÃO: A primeira etapa do cálculo computacional foi a otimização completa de
geometria, ou seja, calcular a geometria mais estável energeticamente. A Fig. 1
apresenta as geometrias encontradas para os três complexos envolvendo ftalimida
e RCOOH (R=-H, -CH3 e –C6H5).
Através da Fig. 1 observamos que duas possíveis ligações de hidrogênio podem ser
formadas entre a imida cíclica e os ácidos carboxílicos, sendo a primeira
envolvendo o grupo N-H e a carbonila do ácido carboxílico e a segunda
envolvendo a o grupo carbonila da ftalimida e a hidroxila dos ácidos
carboxílicos. Estas duas ligações de hidrogênio resultam na formação de um quasi
ciclo de 8 membros. É importante ressaltar que os comprimentos das ligações de
hidrogênio são similares em todos os complexos, sendo em média 1.881 Å para as
ligações NH···OC e 1.721 Å para as ligações CO···HO.
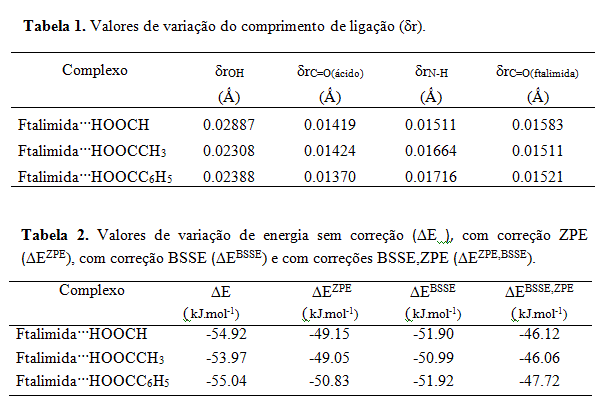
A tabela 1 apresenta as principais mudanças estruturais ocorridas após a
formação das ligações de hidrogênio. Através desta tabela é possível observar
que a ligação O-H é a mais afetada pela complexação, sendo a maior variação
observada para o complexo entre ftalimida e ácido fórmico, onde o comprimento
da ligação O-H aumentou 0.02887 A.
A tabela 2 mostra os valores de energia das ligações de hidrogênio dos complexos
estudados sem correções, e com correções do ponto zero (ZPE) e com correções
do erro de superposições de base (BSSE). Em média, os valores das energias das
ligações de hidrogênio foram similares entre os complexos envolvendo os ácidos
carboxílicos e a ftalimida, sendo estas energias em torno de 46 kJ/mol.
Figura 1
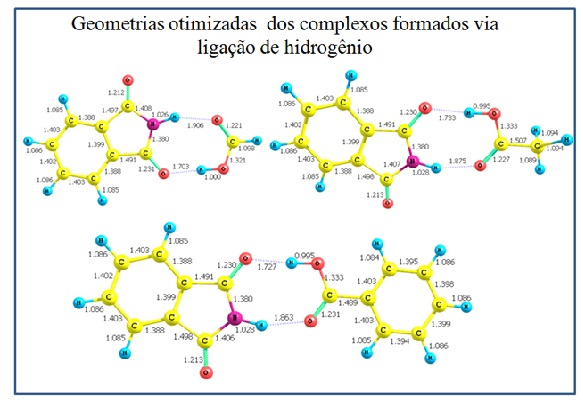
Geometrias otimizadas dos complexos envolvendo
ftalimida e RCOOH (R= -H, -CH3 e –C6H5).
Comprimentos das ligações em Å.
CONCLUSÕES: Neste trabalho foram utilizados cálculos ab inito para simular computacionalmente
as geometrias completamente otimizadas dos complexos envolvendo ftalimida e RCOOH
(R=-H, -CH3 e –C6H5). Três estruturas estáveis energeticamente foram encontradas,
nas quais duas possíveis ligações de hidrogênio foram formadas (NH···OC e
CO···HO) formando assim um quasi ciclo de oito membros, O processo de formação
das ligações de hidrogênio resultou no aumento do comprimento de todas as ligações
diretamente envolvidas nela, sendo os aumentos mais fortes na ligação OH dos
ácidos carboxílicos.
AGRADECIMENTOS: Os autores agradecem a PROPESQ/UFPE, DAE, CNPQ, FACEPE e PRONEX pelo suporte
financeiro e ao Laboratório de Química Computacional da UFPE (LQTC).
REFERÊNCIAS BIBLIOGRÁFICA: [1] J.M. Chapman Jr., S.D. Wyrick, P.J. Voorstad, J.H. Maguire, G. H. Cocolas e I.H. Hall, J. Pharm. Sci., 73, (1984), 1482.
[2] J.M. Chapman Jr., S.D. Wyrick, P.J. Voorstad e I.H. Hall, J., J. Med. Chem. 26 (1983) 237.
[3] A.R. Murthy, S.D. Wyrick e I.H. Hall, J. Med. Chem. 28, (1985), 1591.
[4] A.D. Becke, J. Chem. Phys. 1993, 98, 5648.
[5] P. Geerlings, F. De Proft, W. Langenacker, Chem. Rev. 2003, 103,1793.
[6] M.J. Frisch; J. A. Pople; J.S. Binkley, The J. of Chem. Phys. 80 (1984) 3265.
[7] S.F. Boys; F. Bernardi, Mol. Phys. 19, (1970), 553.
