ÁREA: Química Tecnológica
TÍTULO: PRODUÇÃO DE BIODIESEL A PARTIR DO ÓLEO DE CANOLA REFINADO UTILIZANDO UM CATALISADOR HETEROGÊNEO BÁSICO DE ÓXIDOS MISTOS
AUTORES: Correia, L.M. (DEQ/UFC) ; Campelo, N.S. (DEQ/UFC) ; Vieira, R.S. (DEQ/UFC)
RESUMO: A atividade catalítica da dolomita foi estudada usando-a como catalisador
heterogêneo para a produção de biodiesel. Este catalisador tem algumas
vantagens, tais como seu baixo custo, estrutura porosa, abundância e não é
tóxica. As reações de transesterificações foram realizadas usando diferentes
concentrações de catalisador (1, 2 e 3 % massa/massa) em diversas razões molares
do óleo de canola refinado e álcool metílico (1:6, 1:9 e 1:12), mantendo-se fixo
a temperatura (60 °C), o tempo reacional (4 horas) e a velocidade de agitação
(1000 rpm). Os parâmetros foram otimizados com a utilização de um planejamento
experimental 32 com ponto central em triplicata. O melhor resultado obtido para
conversão dos ésteres metílicos foi de 98,81%, quando se usa as variáveis de XRM
(1:6) e XCAT (1%).
PALAVRAS CHAVES: dolomita; catalisador heterogêneo; ésteres metílicos
INTRODUÇÃO: Atualmente nosso planeta está sofrendo diversas mudanças ambientas e assim, o
cuidado com o meio ambiente cresce a cada dia. O avanço tecnológico na área de
produtos biodegradáveis está surgindo com o intuito de desenvolver práticas para
minimizar essas mudanças. Como fonte energética renovável, atualmente, vem sendo
estudado, o Biodiesel, que é biodegradável, não tóxico e tem uma reduzida
emissão de gases nocivos em relação ao diesel (ALBUQUERQUE et al., 2008) mesmo
com rendimento e propriedades similares (XIE et al., 2006).
O biodiesel é um combustível composto de ésteres monoalquila de cadeia longa de
ácidos graxos derivado de óleos vegetais ou gorduras animais (ALBUQUERQUE et
al., 2008).
A catálise heterogênea apresenta a vantagem da recuperação do catalisador ser
mais simples e da eliminação da formação de sabão. Muitos catalisadores têm
mostrado alta eficiência e atividade na reação de transesterificação e
esterificação de ácidos graxos, porém sempre sob alta temperatura e pressão,
além de tempos reacionais mais longos (DARALOUB et al., 2009). Alguns destes
catalisadores, como a argila nanoporosa dolomita CaMg(CO3)2, o óxido de cálcio
impregnado no SBA-15 (ALBUQUERQUE et al., 2008) e no Lítio (Li/CaO), óxido de
zinco impregnado no KF (XIE et al., 2006), entre outros, vem sendo estudados
WEST et al., 2008).
A dolomita é um carbonato duplo de cálcio e magnésio, que se decompõe durante o
aquecimento, para dar origem aos óxidos de cálcio e magnésio (LLEGAN, 2011). A
reação geral de decomposição pode ser escrita:
CaMg(CO3)2 ↔ CaO + MgO + 2CO2
A reação de transesterificação com óleo de canola refinado e álcool metílico foi
estudada empregando a dolomita modificada termicamente como catalisador
heterogêneo para produção dos ésteres metílicos.
MATERIAL E MÉTODOS: Reagentes e Materiais
Os reagentes usados foram: álcool metílico com um grau de pureza > 99,8%
(VETEC), óleo de canola refinado comercial da marca (LIZA) obtido no mercado
local, a dolomita em forma de pó foi obtida de uma empresa local (ITAMIL-LTDA),
heptadecanoato de metila com grau de pureza de 99,5 % (FUKA) e os gases He, N2 e
Ar de grau analítico fornecidos pela empresa WHITE MARTINS.
Ensaio Cinético
Os ensaios cinéticos foram realizados para avaliar o tempo de equilíbrio da
reação de transesterificação tendo em vista manter o parâmetro de tempo como uma
variável fixa. A reação de transesterificação foi realizada em um reator
batelada composto de um balão de fundo chato com duas entradas equipado com
condensador e agitador magnético . Inicialmente, no balão de reação foram
introduzidos 60 mL do óleo de canola refinado e o álcool metílico e,
posteriormente, foi adicionado o catalisador dolomita, 3% p/p em relação à massa
de óleo pesada. Utilizou-se uma razão molar de 1:6 (óleo: álcool metílico),
temperatura de 60 oC e agitação de 1000 rpm. Após o término da reação de 7
horas, o catalisador foi separado por centrifugação a 2250 rpm por 30 minutos e
a mistura reacional foi colocada em um funil de decantação durante 24 horas para
a separação das fases (ésteres metílicos e glicerina). Em seguida, o álcool
metilico em excesso foi removido da fase éster por um equipamento de rotavapor.
Planejamento Experimental
Os parâmetros das reações do óleo de canola com álcool metílico foram otimizados
com a utilização de um planejamento [3*(K-P) and Box-Behnken designs], com duas
variáveis codificadas: razão molar (XRM) e concentração de catalisador (XCAT). A
resposta escolhida foi à conversão de ácidos graxos do óleo de canola refinado
em ésteres metílicos (Y0).
RESULTADOS E DISCUSSÃO: O estudo de cinética foi realizado a fim de prever o tempo de equilíbrio
reacional. Observa-se na Figura 1, a conversão em função do tempo reacional,
atingiu-se a conversão máxima em 4 h em ésteres metílicos, com transformação dos
ácidos graxos presentes no óleo vegetal de canola refinado em ésteres metílicos
com 98,81 %.
A Figura 2 mostra o gráfico da superfície de resposta para a variável dependente
conversão dos ésteres metílicos (Yo) em função das variáveis independentes: a
razão molar (XRM) e a concentração de catalisador (XCAT). Através da análise da
superfície de resposta, pode-se verificar que a variável XRM exerce efeito
negativo na produção dos ésteres metílicos e a variável XCAT tem efeito
positivo. Então os resultados indicam que quando se utiliza maior concentração
de catalisador entre os reagentes (óleo vegetal de canola refinado e o álcool
metílico), maior será a conversão em ésteres metílicos em menor XRM.No entanto,
a variável XRM, considerando que a reação de transesterificação é uma reação que
desloca o equilíbrio em excesso de álcool metílico, desloca o equilíbrio químico
da reação em direção à formação dos ésteres metílicos, aumentando a conversão em
ésteres metílicos. Porém, o uso de um alto volume de álcool metílico dificulta o
processo de separação por gravitação entre as fases do éster e glicerina formado
como coproduto, aumentando assim sua miscibilidade e favorecendo o deslocamento
do equilíbrio no sentido inverso, isto é, em direção à formação de mono, di e
triglicerídeo, diminuindo a produção dos ésteres metílicos. O melhor resultado
encontrado para produção dos ésteres metílicos foi quando se utiliza a XRM (1:6)
e XCAT (1%), conforme mostrado na Figura 2.
Figura 1
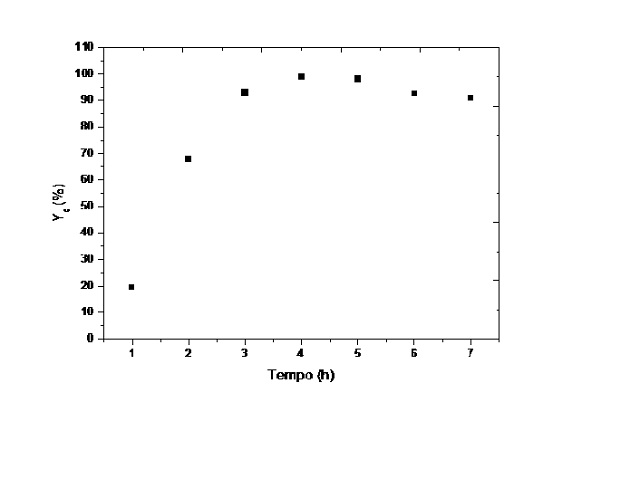
Curva de cinética obtida na reação de
transesterificação com álcool metílico.
Figura 2
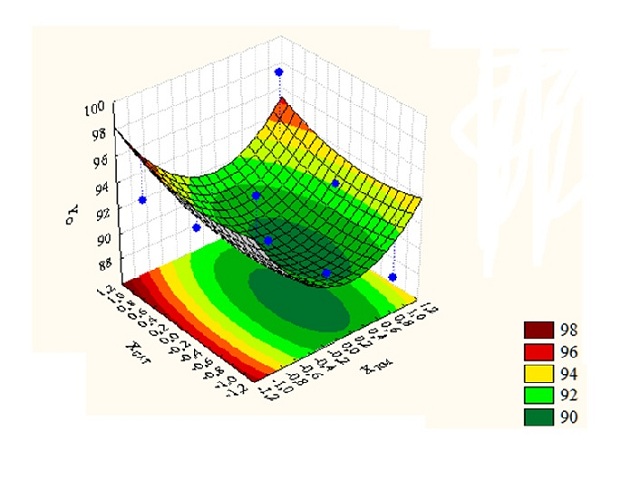
Superfície de resposta para o modelo do catalisador
dolomita modificada termicamente a 850oC/3h.
CONCLUSÕES: A dolomita modificada termicamente mostrou-se promissora para a produção de
biodiesel através da reação de transesterificação com óleo de canola refinado e
álcool metílico. Com a utilização de um planejamento experimental 32 foi possível
obtero ponto ótimo, ou seja, a melhor condição experimental de produção em ésteres
metílicos, a condição ótima encontrada foi quando se usa: XRM (1:6), XCAT (1%),
tempo (4 horas), temperatura (60oC) e velocidade de agitação (1000 rpm) obtendo-se
98,11 % em ésteres metílicos.
AGRADECIMENTOS: Os autores agradecem ao CNPq e FUNCAP pelas bolsas concedidas de mestrado e
iniciação científica.
REFERÊNCIAS BIBLIOGRÁFICA: ALBUQUERQUE, M.C.G., URBISTONDO, I.J.; GONZÁLES, J.S.; ROBLES, J.M.M.; TOST, R.M.; Castellón, E.R.; López, A.J.; Azevedo, D.C.S.; Cavalcante Jr., C.L. CaOsupportedonmesoporous sílicas as basiccatalysts for transesterification reactions, AppliedCatalysis A: General 334 (2008) 35-43.
DARDOUB, M.J.; BRONZEL, J.L.; RAMPING, M.A. Biodiesel: Visão crítica do status atual e perpectivas na academia e na indústria. Química Nova, v.32, n.3, p. 776-792, (2009).
EN 14103 Fats and Oil Derivatives- Fatty Acid Methyl Esters (FAME), (2001).
LLEGAN, O. Dolomite as a heterogeneous catalyst for transesterification of canola oil. Fuel Processing Technology 92 (2011) 452-455.
XIE, W.; HUANG, X. Synthesis of biodiesel from soybean oil using heterogeneous KF/ZnO catalyst.Catalysis Letters 107 (2006) 1-2.
