ÁREA: Ambiental
TÍTULO: CARACTERIZAÇÃO QUALITATIVA DE SUBSTÂNCIAS HÚMICAS EM SUBSTRATOS ORGÂNICOS POR ESPECTROSCOPIA NO UV-VISÍVEL
AUTORES: Silva, R.R. (UNIVERSIDADE FEDERAL DO TOCANTINS) ; Lucena, G.N. (UNIVERSIDADE FEDERAL DO TOCANTINS) ; Abrahão, V.A.P. (UNIVERSIDADE FEDERAL DE VIÇOSA) ; Matos, A.T. (UNIVERSIDADE FEDERAL DE VIÇOSA) ; Coelho, M.S. (UNIVERSIDADE FEDERAL DE VIÇOSA) ; Pimenta, L.A. (UNIVERSIDADE FEDERAL DE VIÇOSA)
RESUMO: As substâncias húmicas (SH) apresentam estrutura molecular complexa e heterogênea, que dificulta a sua caracterização qualitativa. Assim foi utilizada a espectroscopia no UV-VIS para caracterizar qualitativamente os ácidos fúlvicos (AF) e húmicos (AH) purificados das SH de cinco substratos orgânicos da região de Gurupi – TO. As porções húmicas foram fracionadas e purificadas segundo metodologia proposta pela Sociedade Internacional de Substâncias Húmicas. As leituras de absorbância (ABS) foram feitas na faixa de 230 a 700 nm. Devido aos picos de ABS na região de 270 e 390 nm e a baixa razão E4/E6, foi possível identificar as estruturas aromáticas condensadas e o maior grau de humificação dos AH em relação aos AF, indicando a boa qualidade dos cinco substratos.
PALAVRAS CHAVES: Ácidos Húmicos; Ácidos fúlvicos; Compostos Aromáticos
INTRODUÇÃO: A matéria orgânica (MO) é indicadora-chave da qualidade do solo, pois atua como fonte de nutrientes, aumenta a retenção de cátions, atua na complexação de metais, fonte de carbono e energia aos microorganismos do solo e auxilia na infiltração e retenção de água (PESSOA et al., 2012). Em substratos, atua também no aumento da difusão de oxigênio para as raízes, capacidade de troca de cátions (CTC) e pH (SILVA et al., 2009).
Os substratos são fontes de MO que contribuem na retenção de umidade, fornecimento de parte dos nutrientes e condições necessárias para manter o desenvolvimento da planta com qualidade (CAMARGO et al., 2011). A MO é composta pelas raízes de plantas e os organismos do solo e, ainda, da matéria macroorgânica, constituída de resíduos de plantas e animais em decomposição, substâncias humificadas e as não humificadas (PRIMO et al., 2011).
As substâncias húmicas (SH), principal constituinte da MO, são fracionadas em ácidos húmicos (AH), ácidos fúlvicos (AF) e humina (HUM). Além disso, são formadas por moléculas complexas e heterogêneas, modificadas química e biologicamente, o que dificulta a sua caracterização (SILVA & MENDONÇA, 2007).
A espectroscopia no UV-VIS é muito utilizada na caracterização das SH (DOBBSS et al., 2009). Essa técnica espectroscópica é útil na determinação da razão E4/E6 (ABS em 465 nm/ABS em 665 nm) e na ABS de sistemas aromáticos, que estão relacionadas com o grau de humificação de estruturas aromáticas e alifáticas das SH presentes na matéria orgânica, e consequentemente, com a qualidade do solo ou de um substrato orgânico (CANELLAS & SANTOS, 2005).
Diante do exposto, o presente estudo tem como objetivo caracterizar qualitativamente os AH e AF purificados de cinco substratos orgânicos regionais da cidade de Gurupi – TO.
MATERIAL E MÉTODOS: O experimento foi conduzido no departamento de solos da Universidade Federal de Viçosa em Viçosa – MG. Foram utilizados cinco substratos orgânicos regionais da cidade de Gurupi – TO. Os substratos utilizados foram designados como T1, T2, T3, T4 e T5, sendo que de cada substrato foi extraída e purificada a fração AH e AF.
O fracionamento químico das substâncias húmicas foi realizado com solução de NaOH 0,1 mol.L-1, segundo a metodologia proposta pela Sociedade Internacional de Substâncias Húmicas (IHSS) (SWIFT et al., 1996). Os ácidos húmicos e fúlvicos foram purificados e liofilizados conforme a IHSS.
As leituras na faixa do UV-Visível foram feitas em espectrofotômetro de varredura modelo UV/VIS 911A, da marca GBC, utilizando células de quartzo com caminho ótico de 1 cm. As leituras na faixa do visível, tanto de varredura (380 a 700 nm) quanto de determinação das ABS em 465 e 665 nm, foram feitas nas soluções de ácidos fúlvicos e húmicos purificados, diluídos apropriadamente em solução de bicarbonato de sódio (CHEN et al.,1977). As leituras na faixa do ultravioleta foram feitas nas soluções de ácidos fúlvicos purificados, diluídos em soluções com pH ajustado para 2,0 (com HCl) e 12,0 (com NaOH), além da solução tamponada neutra de bicarbonato. Os espectros diferenciais foram calculados pela diferença entre os espectros obtidos em pH 12,0 e 2,0, expressando os dados em absortividade (BLOOM & LEENHEER, 1989).
RESULTADOS E DISCUSSÃO: A figura 1 mostra os espectros no UV-VIS dos AF e AH dos cinco substratos. Os espectros apresentaram diminuições na ABS com o aumento do comprimento de onda. Os AH (Figura 1b) apresentaram pico de ABS na região de 270 nm, evidente nos cinco substratos, dando um indicativo de ABS de sistemas aromáticos (CANELLAS et al., 2000). Os AF (Figura 1a), não apresentaram pico em 270 nm, sugerindo uma diminuição na quantidade de estruturas aromáticas e, assim, na sua estabilidade em relação aos AH, o que vai de acordo com a estrutura sugerida para os AF (STEVENSON, 1994).
Os AH e os AF nos tratamentos T1 e T2 apresentaram pico de ABS na região de 390 nm. Esse é um comportamento característico de SH e ocorre devido à sobreposição de picos relativos a diferentes grupos cromóforos, tais como estruturas aromáticas, localizados em diversos pontos da macromolécula e em diversas formas de conjugação, ocorrendo o desdobramento dos picos e a junção dos mesmos em um espectro disforme (McCARTHY & RICE, 1985). Os AF nos tratamentos T3, T4 e T5, não apresentaram pico em 390 nm, o que prediz um menor grau de humificação e quantidade de estruturas aromáticas implicando em uma diminuição da CTC, pH e retenção de água.
As razões E4/E6 dos AF foram maiores que as dos AH (Figura 2a e 2b). Alta E4/E6 é característica de AF, uma vez que ela prediz a existência de estruturas alifáticas menos condensadas e uma diminuição das conjugações de ligações duplas e simples (PRIMO et al., 2011). Baixa E4/E6 relaciona-se ao aumento do peso molecular, condensação de carbonos aromáticos, aumento da humificação de estruturas aromáticas e maior conjugação de ligações duplas e simples características de AH, o que leva os AH a terem uma maior estabilidade e permanência no solo (DOBBSS et al., 2009).
Figura 1
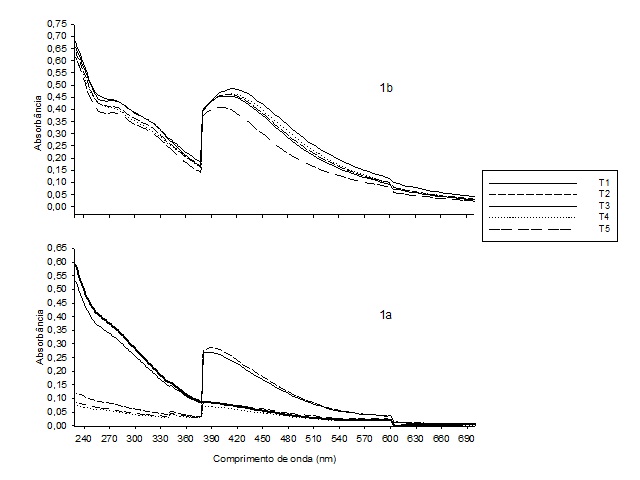
Espectros de UV-VIS dos Ácidos Fúlvicos (1a) e Ácidos Húmicos (1b) purificados dos cinco substratos orgânicos regionais. Gurupi - TO, 2012
Figura 2

Razão E4/E6 dos Ácidos Fúlvicos (1a) e Ácidos Húmicos (1b) purificados dos cinco substratos orgânicos regionais. Gurupi - TO, 2012
CONCLUSÕES: A espectroscopia no UV-VIS e a razão E4/E6 foram eficientes na determinação da maior presença de estruturas aromáticas nos ácidos húmicos e maior presença de estruturas alifáticas nos ácidos fúlvicos. Além disso, a fração AH dos cincos substratos apresentam uma maior estabilidade e maior presença estruturas aromáticas condensadas e humificadas, evidenciando uma boa qualidade dos cinco substratos.
AGRADECIMENTOS:
REFERÊNCIAS BIBLIOGRÁFICA: BLOOM, P. R.; LEENHEER, J. A. 1989. Vibrational, eletronic, and high-energy spectroscopic methods or characterizing humic substances. In: HAYES, M. H. B. et al. (Ed.) Humic substances II. In search for the structure. Chichester: John Wiley, p.409-446.
CAMARGO, R.; PIRES, S. C.; MALDONADO, A. C.; CARVALHO, H. P.; COSTA, T. R. 2011. Avaliação de substratos para a produção de mudas de Pinhão-Manso em sacolas plásticas. Revista Trópica – Ciências Agrárias e Biológicas, 5: 31-38.
CANELLAS, L. P.; SANTOS, G. A. 2005. Humosfera: tratado preliminar sobre a química das substâncias húmicas. UENF, 309 p.
CANELLAS, L. P.; SANTOS, G. A.; MORAES, A. A.; RUMJANEK, V. M.; OLIVARES, F. L. 2000. Avaliação de características de ácidos húmicos de resíduos de origem urbana: I. Métodos espectroscopia (Uv-vis, IV, RMN 13C-CP/MAS) e microscopia eletrônica de varredura. Revista Brasileira de Ciência do Solo, 24: 741-750.
CHEN, Y.; SENESI, N.; SCHNITZER, M. 1977. Information provide on humic substances by E4/E6 ratios. Soil Sci. Soc. Am J., Madison, 41: 352-358.
DOBBSS, L. B.; RUMJANECK, V. M.; BALDOTTO, M. A.; VELLOSO, A. C. X.; CANELLAS, L. P. 2009. Caracterização química e espectroscópica de ácidos húmicos e fúlvicos isolados da camada superficial de latossolos brasileiros. Revista Brasileira de Ciência do Solo, 33: 51-63.
MCCARTHY, P. E.; RICE, J. A. 1985. Spectroscopic methods (other than NMR) for determining functionality in humic substances. In: AIKEN et al. (Ed.) Humic substances in soil, sediment and water: geochemistry, isolation and characterization. p.527- 560. John Wiley & Sons, New York. 692p.
PESSOA, P. M. A.; DUBA, G. P. BARROS, R. B.; FREIRE, M. B. G. S.; NASCIMENTO, C. W. A.; CORREA, M. M. 2012. Frações de carbono orgânico de um latossolo húmico sob diferentes usos no agreste brasileiro. Revista Brasileira de Ciência do Solo, 36: 97-104.
PRIMO, D. C.; MENEZES, R. S. C.; SILVA, T. O. 2011. Substâncias húmicas da matéria orgânica do solo: uma revisão de técnicas analíticas e estudos no nordeste brasileiro. Scientia Plena, 7: 1-13.
SILVA, I. R.; MENDONÇA, E. S. 2007. Matéria orgânica do solo. In: NOVAIS, R. F.; ALVAREZ V., V. H.; BARROS, N. F.; FONTES, R. L. F.; CANTARUTTI, R. B.; NEVES, J. C. L. (Ed.). Fertilidade do solo. Viçosa: Sociedade Brasileira de Ciência do Solo, 1017p.
SILVA, L. J. B., CAVALCANTE, A. S. S., ARAÚJO NETO, S. E. 2009. Produção de mudas de rúcula em bandejas com substratos a base de resíduos orgânicos. Ciência e Agrotecnologia 33: 1301-1306.
STEVENSON, J.F. 1994. Humus chemisthy, genesis, composition, reactions. 2 ed. New York: John Wiley, 496p.
SWIFT, R. S. 1996. Organic matter characterization. In: SPARKS et al. (Eds.) Methods of soil analysis. Chemical methods, Madison, p. 1011-1020.
