ÁREA: Físico-Química
TÍTULO: ESTUDO DO DESEMPENHO DE ELETROCATALISADORES LIVRE DE PLATINA EM CÉLULAS A COMBUSTÍVEL DE ELETRÓLITO POLIMÉRICO (PEMFC)
AUTORES: Miranda, I.S. (UFPA) ; Fernandes, A.C. (UFPA)
RESUMO: As ligas metálicas binárias de SnyCox suportadas em Carbono Vulcan XC-72 foram
estudadas com o objetivo de comparar o desempenho e a eficiência de
eletrocatalisadores livre de platina utilizados como ânodo em células a
combustível do tipo PEM. Os catalisadores de SnyCox foram sintetizados pelo método
de redução por álcool e em diferentes proporções. Os resultados obtidos para
encontrar a razão atômica dos catalisadores foram feitos por analises de EDX. Para
determinar a área eletroquimicamente ativa e as propriedades superficiais das
ligas metálicas foram empregados testes de Voltametria Cíclica e
Cronoamperometria. A liga metálica de Sn47Co53 foi a que apresentou melhor
desempenho catalítico dentre todos os catalisadores preparados.
PALAVRAS CHAVES: liga metálica; célula a combustível; eletrocatalisador
INTRODUÇÃO: Nos próximos anos, uma nova tecnologia de geração limpa de energia elétrica deve
ganhar espaço para uso em veículos e estações geradoras de energia em
residências, hospitais e pequenas indústrias. É a tecnologia das células a
combustível (também conhecidas como pilhas a combustível), dispositivos
silenciosos que transformam energia química em energia elétrica sem causar danos
ao ambiente. As células a combustível são sistemas eletroquímicos que produzem
energia elétrica à medida que os reagentes são introduzidos no sistema. O
combustível (hidrogênio, alcoóis, etc) é oxidado de forma contínua no ânodo,
enquanto o oxigênio é reduzido no cátodo. O resultado do funcionamento da célula
é a geração de eletricidade, água e calor gerado pela dissipação do sistema
(MERCEDES et al, 2002). A platina é o principal metal utilizado como
eletrocatalisadores em células a combustível, podendo ser usado tanto para a
oxidação anódica quanto para a redução catódica, porém o alto custo da platina,
o comprometimento das reservas no caso de um uso generalizado e o processo de
envenenamento da platina pela adsorção de impurezas como CO limitam sua
utilização (EDSON et al, 2005).
A redução de custo da célula devido à substituição da Pt por um metal não nobre,
como o Co ou ligas metálicas contendo este metal por exemplo, seria muito
significante, uma vez que o custo do cobalto é de aproximadamente 90 $/Kg em
comparação com o preço da Pt que está em torno de 37.000 $/Kg, o que se torna
uma alternativa promissora para aplicações em células a combustível (GVOZDEN et
al, 2009). A partir do exposto verifica-se a necessidade de mais estudo na busca
de eletrocatalisadores de metais não nobres que possam substituir a Pt para se
obter mais opções comerciais na geração de energia limpa.
MATERIAL E MÉTODOS: A síntese dos catalisadores foi realizada pelo método de redução por álcool.
Neste método, o refluxo ajustado à 120 ºC por um tempo de 3 horas, contendo uma
solução alcoólica de etineloglicol e os íons metálicos (solução de SnCl2.2H2O e
CoCl2.6H2O) na presença de um agente estabilizante, normalmente um polímero ou
uma solução básica para ajuste do pH=12, sendo que o álcool funciona como
solvente e agente redutor, sendo oxidado a aldeídos e cetonas. No final do
processo o metal reduzido é filtrado, lavado com água morna e colocado para
secar em uma estufa.
As composições atômicas dos catalisadores foram obtidos através das análises de
espectroscopia de energia dispersiva de raios-X (EDX). Os ensaios eletroquímicos
de voltametria e cronoamperometria foram realizados com um potenciostato modelo
AUTOLAB PGSTAT 302. Os voltamogramas cíclicos foram obtidos em soluções de 0,5
Mol/L de H2SO4 saturados com nitrogênio. Durante o experimento o fluxo de
nitrogênio é deslocado para a superfície da solução e as curvas voltamétricas
são obtidas a uma determinada velocidade de varredura do potencial (50 mV/s). As
curvas amperométricas foram obtidas durante 700 s. As medidas de
cronoamperometria foram realizadas em soluções de (0,5 Mol/L de H2SO4 + 0,5
Mol/L de etanol).
RESULTADOS E DISCUSSÃO: Na técnica de EDX para avaliar a composição atômica média dos materiais, tivemos
os seguintes resultados: Sn71Co29, Sn27Co73 e Sn47Co53.
Os voltamogramas cíclicos dos eletrocatalisadores Sn71Co29, Sn27Co73 e Sn47Co53
(FIGURA 1) não apresentam uma região de adsorção/desorção de hidrogênio (0,05 a
0,4 V) bem definida em comparação com o eletrocatalisador de Pt 60%, isso pode
estar relacionado com o fato das ligas SnyCox possuírem menos sítios ativos com
relação a reação de adsorção/desorção do hidrogênio do que a Pt 60%. O
eletrocatalisador Sn71Co29 mostrou um aumento nas correntes para a região da
dupla camada elétrica (0,4 a 0,8 V) em relação aos eletrocatalisadores de
Sn27Co73 e Sn47Co53, porém estes valores foram bem inferiores que do
eletrocatalisador de Pt 60%. Nos potenciais acima de 0,8 V continuamos a
observar que a Pt 60% se manteve com maiores potenciais tanto para oxidação
catódica (corrente positiva) como para redução anódica (corrente negativa), fato
que pode ser atribuído a formação de mais espécies oxigenadas na composição do
catalisador de Pt 60% (TICIANELLI et al, 1998).
As cronoamperometrias para eletro-oxidação do etanol nas ligas metálicas
suportadas demonstram que se comparadas temos um melhor desempenho catalítico
para o Sn47Co53, porém observamos que a platina 60% se manteve com maior
corrente até aproximadamente 200 segundos e depois deste intervalo vemos que a
liga de Sn47Co53 se manteve constante e tendo a maior corrente como mostrada na
FIGURA 2, este fato pode estar associado por uma maior formação de acetaldeído
pela oxidação do álcool, fato que não ocorre com a Platina uma vez que este
metal reage com a molécula de álcool quebrando o mesmo, formando assim uma
quantidade considerada de CO o qual é adsorvido e diminui suas propriedades.
Voltamograma Cíclico das Ligas de SnxCoy e Platina 60%
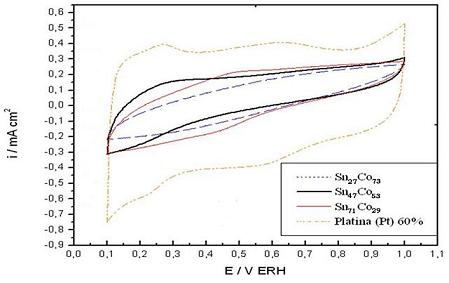
FIGURA 1. Voltamograma Cíclico da Pt 60% e Sn27C073,
Sn47Co53, Sn71Co29, em solução 0,5 Mol/L de H2SO4
com velocidade de varredura de 50mV/s.
Cronoamperometria das ligas de SnxCoy e Platina 60%
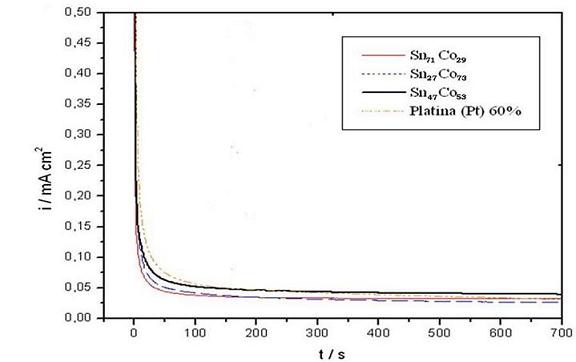
FIGURA 2. Curvas Cronoamperometricas de
eletroxidação de etanol sobre Pt 60% e Sn27Co73,
Sn47Co53, Sn71Co29 em solução 0,5 Mol/L de etanol
e H2SO4.
CONCLUSÕES: A partir das avaliações eletroquímicas, por voltametria cíclica e
cronoamperometria, verificou-se que os catalisadores de Sn47Co53 apresentam os
melhores desempenhos como ânodos de células a combustível do que as demais ligas
de Sn27Co73 e Sn71Co29. Apesar do baixo desempenho no estudo da área eletroquímica
ativa se comparado com a Platina, a liga de Sn47Co53 se apresentou melhor para
eletro-oxidação do etanol no lado do ânodo podendo em potencial substituir a
Platina. Os catalisadores de metais não nobres se tornam cada vez mais promissores
à medida que, seus desempenhos forem aumentados.
AGRADECIMENTOS: Ao LeCaC pela disponibilidade para realização dos experimentos, a UFPA pelo
incentivo e ao PARD pela bolsa de pesquisa.
REFERÊNCIAS BIBLIOGRÁFICA: EDSON A. TICIANELLI*, GIUSEPPE A. CAMARA E LUÍS G. R. A. SANTOS. Eletrocatálise das reações de oxidação de hidrogênio e de redução de oxigênio. Química Nova,Vol. 28. No 4, 664-669, 2005.
GVOZDEN S. TASIC ¹, SCEPAN S. MILJANIC ², MILICA P. MARETA KANINSKI, DJORDJE P. SAPONJIC, VLADIMIR M. NIKOLIC. Non-noble metal catalyst for a future Pt free PEMFC. Electrochesmistry Communications, N. 11 (2009) 2097-2100.
MERCEDES H. VILLULLAS, EDSON A. TICIANELLI E ERNESTO R. GONZÁLEZ, Célula a combustível: energia limpa a partir de fontes renováveis, Química nova na escola, n. 15 2002.
