ÁREA: Química Inorgânica
TÍTULO: Compostos de coordenação: complexos ternários formados entre o alumínio(III), a fosfocreatina e os aminoácidos sulfurados.
AUTORES: Tenório, T. (PUC-RIO) ; Ramos, J.M. (UFRJ) ; Buarque, C.D. (PUC-RIO) ; Felcman, J. (PUC-RIO)
RESUMO: O estudo de complexos ternários de Al(III) com a fosfocreatina (PCr) e os
aminoácidos (aas) sulfurados (metionina, cisteína, homocisteína e penicilamina)
foi realizado em solução aquosa por meio de titulações potenciométricas na
proporção metal:ligante:ligante 1:1:1. Através da potenciometria determinaram-se
as constantes de estabilidade [T=25°C e I=0,1 mol.L-1 (KNO3)] dos complexos
ternários com o Al(III). A especiação dos sistemas também foi feita. A partir
dos valores das constantes de estabilidade dos complexos propõe-se que a
penicilamina comporte-se distintamente dos demais aminoácidos. Nas espécies
AlPCraas, a PCr deve comportar-se como ligante tridentado. A metionina, a
cisteína e a homocisteína atuam como bidentados enquanto a penicilamina parece
atuar como ligante tridentado.
PALAVRAS CHAVES: Potenciometria; Especiação; Sistemas ternários
INTRODUÇÃO: O alumínio(III) é encontrado em pequenas concentrações na maioria dos organismos
vivos, porém, em maiores quantidades é considerado tóxico (OMS, 1998). Ele pode
causar inúmeros efeitos nocivos entre os quais se destaca a osteomalácia, a
anemia hipocrômica microcítica e as doenças neurodegenerativas, como Parkinson,
Alzheimer e escleroses, especialmente, a esclerose lateral amiotrófica
(BARQUERO-QUIROS et al., 2001).
A absorção do Al(III) ocorre no estômago e no duodeno proximal e é facilitada
pela formação de complexos por meio da interação com ligantes biológicos
(EICHHORN et al., 1980), em especial, aqueles com grupos carboxilatos,
catecolatos, fenolatos e fosfatos (EICHHORN et al., 1980). Ligantes dietéticos,
como os aminoácidos, também podem afetar a absorção e a distribuição do alumínio
in vivo (BERTHON, 2002).
Em fluidos corporais com baixa concentração de transferrina, globulinas e
citrato, os nucleosídeos di e trifosfatos podem agir como ligantes do metal
compondo formas solúveis. Se há pequena concentração desses ligantes, as
catecolaminas funcionam como tais, seguidas pelos aminoácidos (SCHÄFER e
JAHREIS, 2006).
Ao considerar os grupos funcionais, a presença nos fluidos corporais ou na dieta
humana nota-se que a fosfocreatina (PCr) e os aminoácidos sulfurados (L),
metionina, cisteína, homocisteína e penicilamina, são possíveis ligantes para o
Al(III), podendo promover sua absorção. A penicilamina não é um aminoácido
comumente encontrado no organismo, mas é usado como agente quelante em
intoxicações por metais e no tratamento de algumas doenças, como na doença de
Wilson.
O presente estudo tem como escopo avaliar a capacidade de formação e a
estabilidade de complexos ternários em solução aquosa formados entre o Al(III),
a PCr e os aminoácidos sulfurados.
MATERIAL E MÉTODOS: O estudo em solução aquosa de complexos ternários revela além da possibilidade
da formação de complexos e das ligações que podem suceder nesses, as interações
ou sua ausência quando certos sítios coordenativos estão impedidos e outros
livres nos complexos com metais.
Os reagentes utilizados para a análise foram o nitrato de alumínio nonahidratado
P.A. (Merck), a fosfocreatina (Sigma), a metionina (Reagen), a cisteína (Sigma-
Aldrich), a homocisteína (Sigma) e a DL-Penicilamina (Acros Organics).
Empregou-se nas titulações, o aparelho de titulação potenciométrica Metrohm 809
Titrando, o pHmetro Micronal B375 e o agitador magnético Metrohm 801 Stirrer.
Antes da realização de qualquer experimento, as vidrarias foram limpas e secas
adequadamente de modo a evitar possíveis contaminações e erros experimentais.
Todas as titulações foram realizadas no mesmo dia em que se efetuou o preparo
das soluções.
Conservou-se à temperatura, à agitação e à força iônica constantes, sendo a
temperatura mantida a 25,0°C, a partir da utilização de um equipamento de banho
termostatizado, a agitação mantida constante e branda pelo agitador magnético e
a força iônica mantida a 0,1 mol.L-1. O eletrólito suporte KNO3 foi usado,
devido às características de seus íons, que não interfere na titulação,
evitando-se a competição com os ligantes e o metal.
As titulações foram realizadas a partir de adições sucessivas de incrementos de
0,1 mL de solução padrão de KOH 0,1 mol.L-1 a um volume inicial de 120,00 mL de
mistura.
Titulou-se 50,00 mL da solução de fosfocreatina 2x10-3 mol.L-1, 50,00 mL da
solução de um dos aminoácidos 2x10-3 mol.L-1, 10,00 mL de KNO3 1,2M e 10,00 mL
da solução de íon metálico Al 1x10-2 mol.L-1.
RESULTADOS E DISCUSSÃO: Os gráficos de distribuição de espécies em função do pH para os quatro sistemas,
Figura 1 (a)-(d), mostram que as espécies hidrolisadas do metal ou dos complexos
binários e ternários predominam em pH fisiológico.
encontrados para as espécies AlPCrL são semelhantes para os aminoácidos Met, Cis
e Hcis. Contudo, para a espécie AlPCrPen é encontrado um valor diverso, próximo
a 25,00, por isso, propõe-se que as espécies ternárias AlPCrL apresentam modos
de coordenação distintos em relação aos aminoácidos. Provavelmente, a Met, a
Cis e a Hcis atuam como ligantes bidentados através do oxigênio do carboxilato e
do nitrogênio do grupo amino, comportamento este característico para os
aminoácidos. Já a Pen deve se comportar como tridentada através do oxigênio do
carboxilato, do nitrogênio do grupo amino e do enxofre do grupo tiol. Na figura
2 podem ser vistas algumas das estruturas propostas para os complexos.
Tabela 1
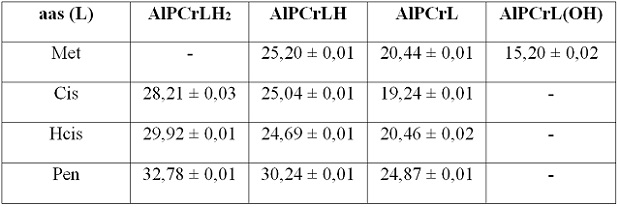
Logaritmos das constantes de estabilidade dos complexos ternários formados no sistema AlIII:PCr:L 1:1:1 a 25°C e I = 0,1 mol.L-1 (KNO3).
Figura 1
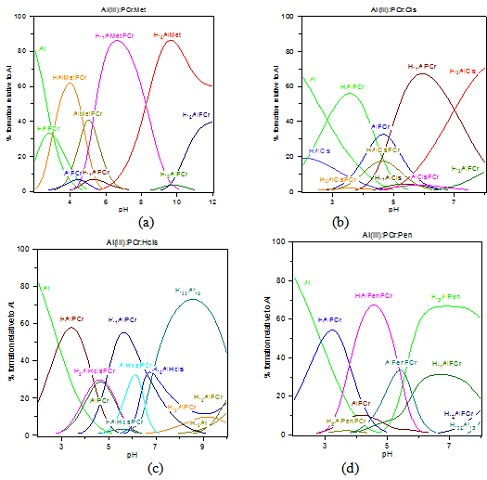
Gráficos de distribuição de espécies dos sistemas ternários.
CONCLUSÕES: No que diz respeito aos complexos ternários com a fosfocreatina, os valores das
constantes de estabilidade para as espécies AlPCrL (log βAlPCrL) sugerem que os
aminoácidos Met, Cis e Hcis atuam como ligantes bidentados. Para a Pen indica-se o
comportamento tridentado através dos átomos de oxigênio do carboxilato, de
nitrogênio da amina e de enxofre. A fosfocreatina agiria como ligante tridentado.
O íon metálico adotaria então o número de coordenação seis, com uma geometria
octaédrica. A esfera de coordenação do Al(III) seria completada com água de
coordenação, quando necessário.
AGRADECIMENTOS: O trabalho foi apoiado pelo CNPq, pela PUC-Rio e pela UFRJ.
REFERÊNCIAS BIBLIOGRÁFICA: BARQUERO-QUIROS, M.; VARGAS-ROJAS, R.; BLANCO-SAENZ, R. 2001. Neurotoxicidad y enfermedades óseas provocadas por la contaminación con aluminio de soluciones de diálisis renal. Revista Costarricense de Ciencias Médicas, 22: 179 -189.
BERTHON, G. 2002. Aluminium speciation in relation to aluminium bioavailability, metabolism and toxicity. Coordination Chemistry Reviews, 228: 319-341.
EICHHORN, G. L.; BUTZOW, J. J.; CLARK, P.; VON HAHN, H. P.; RAO, G.; HEIM, J. M.; TARIEN, E.; CRAPPER, D. R.; KARLIK, S. J. Em: MARTELL, A. E., editor. 1980. Metal Ion-Nucleic Acid Interactions: Aging and Alzheimer's Disease. Inorganic chemistry in biology and medicine, American Chemical Society, 140: 75-88.
ORGANIZAÇÃO MUNDIAL DA SAÚDE (OMS). 1998. Elementos traço na nutrição e saúde humanas, Ed. Roca, 18: 194-195.
SCHÄFER, U.; JAHREIS, G. 2206. Exposure, bioavailability, distribution and excretion of aluminum and its toxicological relevance to humans. Trace Elements and Electrolytes, 23: 162-172.
