ÁREA: Físico-Química
TÍTULO: ESTUDO TEÓRICO COMPARATIVO EM OER E DM DE PROPRIEDADES ESTRUTURAIS PARA AS DIFERENTES MIOTOXINAS DE PEÇONHAS DE CROTALUS SP.
AUTORES: SOUZA, S. B (UEA) ; FERNANDES, A. J. N (UEA) ; ROCHA,J. R. C. C (UEA)
RESUMO: A peçonha de Crotalus durissus terrificus tem sido uma das mais estudadas, tanto suas atividades biológicas quanto químicas possuem cadeias com elevado grau de homologia com outras toxinas pertencentes à família das miotoxinas básicas, porém, suas diferenças de propriedades podem estar relacionadas a aspectos tridimensionais destas proteínas tendo como características em comum, a indução de efeitos mionecróticos. Foram realizados estudos de modelagem molecular e cálculos químico-quânticos que possibilitaram estabelecer aspectos estruturais que justifiquem as diferenças nas atividades mioliticas. Um dos fatores que indicam a influência dessas diferenças na ação biológica dessas estruturas é a disponibilidade de sítios pelas conformações apresentadas.
PALAVRAS CHAVES: miotoxina, aspectos estruturais, proteínas
INTRODUÇÃO: Experimentalmente, foi demonstrado que o veneno crotálico é mais tóxico que veneno das diferentes espécies de Bothops. Venenos de cobras contêm proteínas que são responsáveis por atividades neurotóxica, cardiotóxica, hemorrágicas e miotóxicas. Entre essas toxinas, há um grande interesse em relação às miotoxinas, pois elas desencadeiam diversas reações biológicas (Ownby, 1998).
Apesar de uma considerável quantia de trabalhos, há apenas uma estrutura para a crotamina obtida por RMN disponível no banco de dados PDB (Protein Data Bank). Há, portanto, a necessidade da relação estrutura-função das miotoxinas que seja possível correlacionar com suas propriedades biológicas. Várias técnicas têm sido utilizadas para a elucidação de aspectos tridimensionais, incluindo análises estruturais por SAXS (Beltran etal. 1990), por espectroscopia de Laser-RAMAN (Kawano et al., 1982) e por RMN H1 (Endo et al., 1989; Nicastro et al., 2003). Recentemente, através do uso de RMN H1 de alta resolução, além de técnicas de elucidação mais eficientes, foram confirmadas as interações das ligações dissulfídicas (Fadel et al., 2005).
A Modelagem Computacional é um método complementar útil, pois prever valiosa informação quando dificuldades na cristalização dessas proteínas são encontradas.
MATERIAL E MÉTODOS: Experimentalmente, foi demonstrado que o veneno crotálico é mais tóxico que veneno das diferentes espécies de Bothops. Venenos de cobras contêm proteínas que são responsáveis por atividades neurotóxica, cardiotóxica, hemorrágicas e miotóxicas. Entre essas toxinas, há um grande interesse em relação às miotoxinas, pois elas desencadeiam diversas reações biológicas (Ownby, 1998).
Apesar de uma considerável quantia de trabalhos, há apenas uma estrutura para a crotamina obtida por RMN disponível no banco de dados PDB (Protein Data Bank). Há, portanto, a necessidade da relação estrutura-função das miotoxinas que seja possível correlacionar com suas propriedades biológicas. Várias técnicas têm sido utilizadas para a elucidação de aspectos tridimensionais, incluindo análises estruturais por SAXS (Beltran etal. 1990), por espectroscopia de Laser-RAMAN (Kawano et al., 1982) e por RMN H1 (Endo et al., 1989; Nicastro et al., 2003). Recentemente, através do uso de RMN H1 de alta resolução, além de técnicas de elucidação mais eficientes, foram confirmadas as interações das ligações dissulfídicas (Fadel et al., 2005).
A Modelagem Computacional é um método complementar útil, pois prever valiosa informação quando dificuldades na cristalização dessas proteínas são encontradas.
RESULTADOS E DISCUSSÃO: Foi realizado alinhamento dessas toxinas utilizando a ferramenta ClustalW, podendo-se verificar coincidências entre as seqüências em toda sua extensão mostrando elevado grau de homologia na sequência primária.
Os métodos baseados em ER/MC mostram resultados satisfatórios para análises conformacionais de estruturas peptídicas, considerando-se o tamanho da seqüência e o respectivo custo computacional disponível, quando comparados com os baseados em DM. Pelos resultados de ER/MC, o turno apresentado nos AA 20 e 21 de ambas crotaminas estudadas mostram diferenciação que deve ser provocada pelo AA da posição 19. Além disso, nos cálculos em MC com construção por homologia a mesma diferenciação é percebida.As principais atividades verificadas por essas miotoxinas são a ação no canal de sódio interferindo na permeabilidade, atividade mionecrótica do tecido esquelético e atividade analgésica.
Foi realizado alinhamento dessas toxinas utilizando a ferramenta ClustalW, mostrado na Figura 1. Pode-se verificar coincidências entre as sequências em toda sua extensão mostrando elevado grau de homologia na sequência primária.
Os cálculos em MC dinâmico realizados para a crotamina Ile(19), construída por homologia a partir da estrutura da crotamina leu(19) com o código 1Z99 do PDB, mostram estruturas gerais de mesma tendência globular para as convergidas em MMFF94, como verificado para os três melhores confôrmeros mostrados na Figura 2.
Os confôrmeros sobrepostos indicam, para as regiões de maior coincidência, pouca variação da estrutura. As que mostram menor coincidência indica maior variação nas posições. A maior liberdade de movimento pode influenciar na seletividade em um processo enzimático.

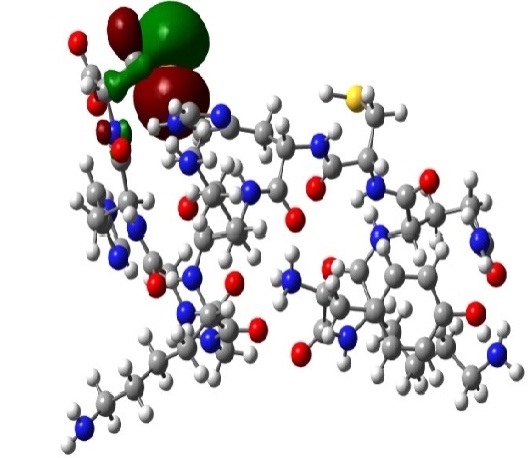
CONCLUSÕES: Após as análises dos dados obtidos, foi possível concluir que os mapas de superfícies pertencentes aos fragmentos dos primeiros AA mostram maior participação do fragmento histidina nos OMf, indicando este resíduo como importante sítio de atividade química, considerando-se a formação das ligações dissulfídicas. Esse procedimento de otimizações por etapas das geometrias dessas proteínas mostrou-se apropriado para buscas conformacionais de mínimos globais de energia, podendo ser aplicado satisfatoriamente a outras estruturas proteicas.
AGRADECIMENTOS: Agradeço a minha mãe pelo incentivo e apoio, aos meus amigos pela preocupação e a FAPEAM pela oportunidade concebida na aquisição de novos conhecimentos.
REFERÊNCIAS BIBLIOGRÁFICA: OWNBY, C., . Structure, function and biophysical aspects of the myotoxins from snake venoms. J. Toxicol. Toxin 1998.
BELTRAN, J.R., Mascarenhas, Y.P., Craievich, A.F., Laure, C.J.. SAXS study of the snake toxin a-crotamine. Eur. Biophys. J..1990.
KAWANO, Y., Laure, C.J., Giglio, J.R.. Laser Raman study on crotamine. Biochim. Biophys. Acta,1982
ENDO, T., Oya, M., Ozawa, H., Kawano, Y., Giglio, J.R., Miyazawa, T.. A proton nuclear magnetic resonance study on the solution structure of crotamine. J. Protein Chem. 8, 1989.
NICASTRO, G.; Franzoni, L.; de Chiara, C.; Mancin, A. C.; Giglio, J. R. and Spisni, A.; Solution structure of crotamine, a Na+ channel affecting toxin from Crotalus durissus terrificus venom; Eur. J. Biochem. 270 (9), 1969-1979 (2003)
FADEL, V.; Bettendorff, P.; Herrmann, T.; De Azevedo, W. F.; Oliveira, E. B.; Yamane, T. and Wuthrich, K. Automated NMR structure determination and disulfide bond identification of the myotoxin crotamine from Crotalus durissus terrificus; Toxicon 46 (7), (2005).
BERMAN et al.: Berman, H. M., Westbrook, J., Feng, Z., Gilliland, G., Bhat, T. N., Weissig, H., Shindyalov, I. N. and Bourne, The Protein Data Bank.
Nucl Acid Res, P. E. 2000.
