ÁREA: Química Inorgânica
TÍTULO: SÍNTESE, CARACTERIZAÇÃO E ESTRUTURAS DE RAIOS X DOS COMPLEXOS CIS-[RuCl2(BIPY)(DPPP)], [RU(N-S)(BIPY)(DPPP)]PF6, ONDE N-S = 2-MERCAPTOPIRIDINA, 2-MERCAPTOPIRIMIDINA E 4,6-DIMETIL 2-MERCAPTOPIRIMIDINA
AUTORES: LIMA, B. A. V. (IQSC-USP) ; BATISTA, A. A. (UFSCAR) ; ELLENA, J. (IFSC-USP) ; CASTELLANO (IFSC-USP)
RESUMO: A reação do complexo cis-[RuCl2(bipy)(dppp)], bipy = 2,2-bipiridina e dppp = 1,3-bis(difenilfosfino)propano com os ligantes N-S: 2-mercaptopiridina (pySH), 2-mercaptopirimidina (Spym) e 4,6-dimetil-2-mercaptopirimidina (SpymMe2) resulta em complexos do tipo [Ru(N-S)(bipy)(dppp)]PF6, os quais foram caracterizados por técnicas espectroscópicas (RMN de 31P{1H}, 1H, IV, UV-Vis) eletroquímicas (voltametria cíclica e condutância molar), de cristalografia de raios X e análise elementar (C, H, N, S). Os espectros de RMN de 31P{1H} apresentam dois dubletos e os voltamogramas apresentam um processo redox, as estruturas de raios X mostraram que os átomos de fósforo da bifosfina encontram-se trans posicionados aos de nitrogênio da bipy e dos ligantes N-S. Os dados corroboram as estruturas propostas.
PALAVRAS CHAVES: mercaptoligantes, bifosfina, rutênio
INTRODUÇÃO: Complexos de rutênio atraem atenção pela versatilidade e ampla área de aplicação como: conversão de energia solar em elétrica, fotodecomposição da água, catálise etc. além de formarem compostos com variados ligantes (BIGNOZZI et al., 1991). Na bioinorgânica, estes complexos têm sido estudados por suas potencialidades como agentes antitumorais (CLARKE et al., 2003). Ligantes fosfínicos, comumente estudados em catálise, apresentam propriedades pi-doadora e pi-receptora, estabilizando valências dos estados de oxidação mais baixos aos mais altos dos metais de transição (MCAULIFFE et al., 1994). Nas últimas duas décadas os ligantes N-S, modelos úteis como análogos das nucleobases pirimidina e purina, têm ganhado especial atenção por suas implicações bioquímicas (DOUGAN et al., 2006). Mercaptorimidinas têm importância em vários processos biológicos, pois apresentam atividades antivirais, antibacterial (VON POELHSITZ et al., 2007), antitumorais, antitireoidais (O'DONOGHUE et al., 1994) e fungicidas (KUKUSHKIN et al., 2002) e por suas propriedades fotoquímicas (MASSEY et al., 2001). Alguns destes compostos encontram uso como drogas antivirais, antimetabólitos e antitumorais (CORRAL et al., 2009). Além disso, estes ligantes são de grande interesse na química de coordenação, por apresentarem grande variedade de modos de coordenação ao metal: monodentado neutro (CONSTABLE et al., 1991), bidentado (GUPTA et al., 1995), ligante ponte (ASLANIDIS et al., 1994), monodentado aniônico (AKRIVOS et al., 2001) ou ainda poderem se ligar a dois átomos metálicos (LANG et. al., 2003). Este trabalho tem por objetivo a síntese (Figura 1), caracterização (espectroscopica e eletroquímica) e estudo estrutural dos complexos cis-[RuCl2(bipy)(dppp)] e [Ru(N-S)(bipy)(dppp)] (N-S= pyS, Spym and SpymMe2).
MATERIAL E MÉTODOS: Todos os reagentes utilizados foram de alto grau de pureza. RuCl33H2O, 1,3 bis(difenilfosfina)propano (dppp), 2,2-bipiridina (bipy), 2-mercaptopiridina (pySH), 2-mercaptopirimidina (Spym) e 4,6-dimetil-2-mercaptopirimidina (SpymMe2), de origem Aldrich, foram usados sem prévio tratamento. Experimentos de RMN foram realizados em CH2Cl2 (D2O), CDCl3, C2D6CO a 293 K, num espectrômetro Bruker, 9.4 T, 1H a 400.13 e 31P{1H} a 161.98 MHz. Os espectros de UV-Visível foram medidos num espectrofotômetro HP8452A (diode array) e os de IV foram medidos em pastilha de KBr num espectrofotômetro FTIR BomemMichelson 102, na região de 4000400 cm-1. Os voltamogramas cíclicos foram medidos a 293 K em CH2Cl2 contendo 0.10 M Bu4NClO4, com um BAS-100B/W Bioanalytical Systems Inc. electrochemical analyzer; Os eletrodos de trabalho e auxiliar utilizados foram de platina e o de referência foi Ag/AgCl. As medidas de condutividade molar foram realizadas em um condutivímetro MICRONAL, modelo B-330. As microanálises foram realizadas num EA 1108 CHNS. Os cristais foram medidos num difratômetro EnrafNonius Kappa-CCD (k = 0.71073 Å). Os dados foram coletados usando o programa COLLECT (ENRAF-NONIUS, 1997-2000) e tratados com os programas HKL DENZO-SCALEPACK (OTWINOWSKI, 1997). As correções foram realizadas pelo método Gaussian (BLESSING, 1995). As estruturas foram resolvidas usando SHELXS-97 (SHELDRICKa, 1997) e refinadas por meio do SHELXL-97 (SHELDRICKb, 1997). As estruturas ORTEP foram preparadas usando ORTEP-3 for Windows (FARRUGIA, 1997).
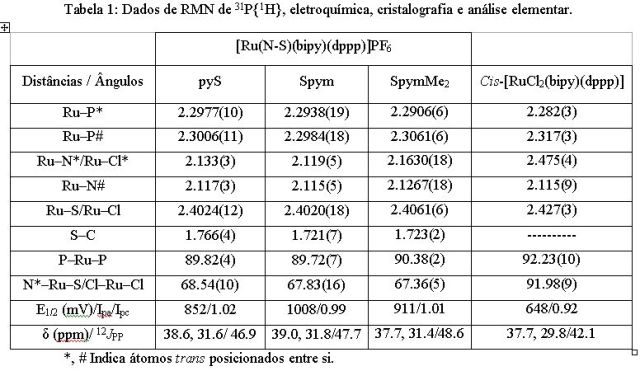
RESULTADOS E DISCUSSÃO: Os anéis de 4 e 5 membros formados pelos ligantes N-S e bipy, NRuS ≈ 67.5⁰ e NRuN ≈ 77⁰ levam os complexos a apresentarem estruturas octaédricas distorcidas. As distâncias das ligações RuP e os ângulos PRuP estão dentro do intervalo normalmente encontrado para complexos de rutênio (II) com fosfinas terciárias (Tabela 1). A distância RuN (N-S) é maior no complexo contendo SpymMe2. As distâncias C=S observadas nos complexos são maiores que essas distâncias nos ligantes livres na forma tiona (pySH C=S = 1.68 Å) (PENFOLD et al., 1953) e menores que na forma tiol (CS = 1.81 Å) (PAULING, 1960). Os espectros de RMN de 31P{1H} apresentam o típico sistema de spin AX (Tabela 1). Os espectros de RMN de 1H apresentam uma série de multipletos no intervalo de δ 7.686.38 ppm, correspondentes a 20 átomos de hidrogênio dos grupos fenila, 9.50-6.87 ppm relativos a 8 átomos de hidrogênio da bipy. Os prótons dos grupos CH2, pyS, Spym and SpymMe2 aparecem nas regiões 3.471.81 ppm, 7.42-6.22 ppm, 8.186.20 ppm e em 5.84 ppm, respectivamente. Os grupos metila do SpymMe2 são observados em 5.84 e 6.49 ppm. Os voltamogramas cíclicos mostram um par redox reversível. Os valores de E1/2 seguem a basicidade dos ligantes N-S (Tabela 1). Os espectros de IV apresentam bandas correspondentes a ν(C=S) (≈1269 cm-1), ν(C=N) (≈1435 cm-1), ν(P-CH2) (≈665 cm-1) e ao contra-íon ν(PF6-) a 840 e 557 cm-1 (Nakamoto, 1997). Os espectros eletrônicos dos complexos apresentam bandas na região UV ~300 nm atribuídas a uma transição intraligante e outra banda em ~430 nm atribuída a uma transferência de carga metal-ligante. A Condutância molar indica eletrólito 1:1 para os complexos contendo os ligantes N-S e as análises elementares confirmam as fórmulas propostas.
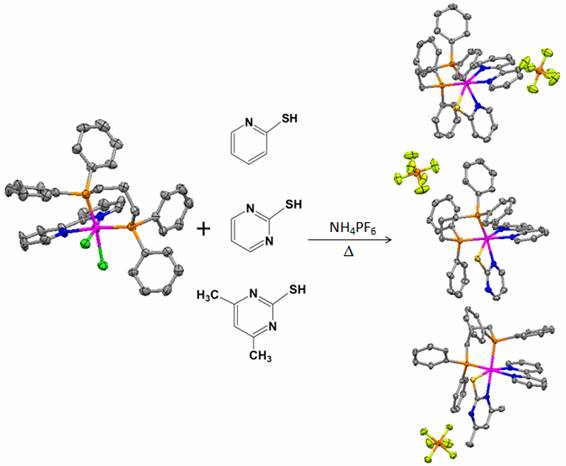
CONCLUSÕES: Neste trabalho quatro novos complexos: cis-[RuCl2(bipy)(dppp)] e [Ru(N-S)(bipy)(dppp)]PF6, N-S = pyS, Spym and SpymMe2 foram sintetizados e caracterizados. Os espectros de RMN de 31P{1H} mostram a não-equivalência dos átomos de fósforo e os dubletos dos complexos com os ligantes N-S apresentam frequências maiores que o complexo precursor. As estruturas de raios X mostram que os átomos de fósforo estão trans posicionados aos de nitrogênio da bipy e dos ligantes N-S. Os dados de voltametria cíclica, IV, UV-Visível, condutância molar e análise elementar confirmam as estruturas propostas.
AGRADECIMENTOS: Agradecemos à FAPESP, CNPq e CAPES pelo suporte financeiro.
REFERÊNCIAS BIBLIOGRÁFICA: AKRIVOS, P. D. Recent studies in the coordination chemistry of heterocyclic thiones and thionates. Coord. Chem. Rev., 213: 181, 2001.
ASLANIDIS, P.; HADJIKAKOU, S. K.; KARAGIANNIDIS, P.; KOJICPRODIC, B.; LUIC, M. Preparation and spectral studies of dinuclear mixed ligand copper(I) complexes - the crystal-structure of bis[μ-S(pyridine-2-thione)(tmtp) copper(I)bromide]. Polyhedron, 13: 3119, 1994.
BIGNOZZI, C. A.; ARGAZZI, R.; CHIORBOLI, C.; ROFFIA, S.; SCANDOLA, F. Photoinduced intramolecular energy-transfer processes in polynuclear ruthenium(II) polypyridine complexes - design of long-chain cyanobridged polynuclear species featuring vectorial energy-transfer. Coord. Chem. Rev., 111: 261, 1991.
BLESSING, R. H. An empirical correction for absorption anisotropy. Acta Crystallogr. Sect. A 51: 33, 1995.
CLARKE, M. J. Ruthenium metallopharmaceuticals, Coord. Chem. Rev., 236: 209, 2003.
CONSTABLE, E. C.; KING, A. C.; PALMER, C. A.; RAITHBY, P. R. The 1st structurally characterized example of a manganese(II) complex with monodentate thione ligands - the crystal and molecular-structure of trans-dichloro(tetrakis(2(1H)-pyridinethione-S))manganese(II). Inorg. Chim Acta, 184: 43, 1991.
CORRAL, E.; HOTZE, A. C.; DEN DULK, H.; LECZKOWSKA, A.; RODGER, A.; HANNON, M. J.; REEDIJK, J. Ruthenium polypyridyl complexes and their modes of interaction with DNA: Is there a correlation between these interactions and the antitumor activity of the compounds?. J. Biol. Inorg. Chem., 14: 439, 2009.
DOUGAN, S. J.; MELCHART, M.; HABTEMARIAM, A.; PARSONS, S.; SADLER, P. J. Phenylazopyridine and phenylazo-pyrazole chloride ruthenium(II) arene complexes: arene loss, aquation, and cancer cell cytotoxicity. Inorg Chem, 45: 10882, 2006.
ENRAF-NONIUS, Collect, Nonius BV, Delft, The Netherlands, 19972000.
FARRUGIA, L. J. Ortep-3 for Windows - A Version of ORTEP-III with a Graphical User Interface (GUI) . J. Appl. Crystallogr. 30: 565, 1997.
GUPTA, M.; CRAMER, R. E.; HO, K.; PETTERSEN, C.; MISHINA, S.; BELLI, J.; JENSEN, C. M. Trans influence of phosphines on dimer-monomer interconversion of 2-pyridinethiolate complexes - structures of [Pd(μ-η2-pySN, S)Cl(L)]2 (L=PMe2Ph, PMePh2) and Pd(η2-pyS)Cl(PPh3). Inorg. Chem., 34: 60, 1995.
KUKUSHKIN, V. Y.; POMBEIRO, A. J. L. Additions to metal-activated organonitriles. Chem. Rev., 102: 1771, 2002.
LANG, E. S.; DE OLIVEIRA, G. M.; CASAGRANDE, G. A.; VÁZQUEZ-LÓPES, E. M. Induced crystallization of polymeric Cd(II)-dmpyS assemblies (dmpyS=4,6-dimethyl-pyrimidine-2-thiolato): synthesis and chaining structures of α-and β-[Cd(dmpyS)2]n. Inorg. Chem. Commun., 6: 1297, 2003.
MASSEY, A.; XU, Y. Z.; HARRAN, P. Photoactivation of DNA thiobases as a potential novel therapeutic option. Curr. Biol., 11: 1142, 2001.
MCAULIFFE, C. A.; MACKIE, A. G. P donor ligands In: Encyclopedia of Inorganic Chemistry. KING, R. B. Ed. New York, Wiley, Interscience, p. 2989, 1994.
Nakamoto, K. Infrared and Raman Spectra of Inorganic and Coordination Compounds, fifth ed. Wiley-Interscience, New York, 1997.
O'DONOGHUE, J. L, Ed. Neurotoxicity Of Industrial and Commercial Chemicals CRC Press, Inc.: Boca Raton, FL, 1984.
OROWINOWSKI, Z., MINOR, W. Macromolecular Crystallography, Part A, Academic
Press, New York, 1997.
PAULING, L. The Nature of the Chemical Bond, third ed., Cornell University Press, New York, 1960.
PENFOLD, B. R. The crystal structure of alpha-thiopyridone Acta Crystallogr., 6: 707, 1953.
SHELDRICK, G. M. (Ed.), Shelxl-97. Program for Crystal Structures Analysis,
University of Göttingen, Göttingen, Germany, 1997.
SHELDRICK, G. M. (Ed.), Shelxs-97. Program for Crystal Structure Resolution,
University of Göttingen, Göttingen, Germany, 1997.
VON POELHSITZ, G.; BOGADO, A. L.; DE ARAUJO, M. P.; SELISTRE-DE-ARAUJO, H. S.; ELLENA, J.; CASTELLANO, E. E.; BATISTA, A. A. Synthesis, characterization, X-ray structure and preliminary in vitro antitumor activity of the nitrosyl complex fac-[RuCl3(NO)(dppf)], dppf=1,1 '-bis(diphenylphosphine)ferrocene. Polyhedron, 26: 4707, 2007.
