ÁREA: Nanociência e Nanotecnologia
TÍTULO: Obtenção de aluminato de bário nanométrico na superfície de alfa-alumina
AUTORES: A. P. MACIEL (UFMA) ; R. S. MELO (UFMA) ; M. H. A. TAVARES (UFMA) ; E. LONGO (UNESP) ; E. R. LEITE (UFSCAR) ; F. C. SILVA (UFMA)
RESUMO: Aluminato de bário em escala nanométrica foi obtido na superfície de partículas de alfa-alumina pelo método dos precursores poliméricos. O aluminato de bário foi caracterizado por Espectroscopia na Região do Infravermelho com transformada de Fourier, Análise de área superfícial e distribuição de poros, Difração de raios-X e microscopia eletrônica de varredura. Esse sólido obtido mostrou boa conversão em reações de transesterificação para obtenção de ésteres metílico a partir do óleo de babaçu.
PALAVRAS CHAVES: aluminato de bário, nanomateriais, catálise heterogênea
INTRODUÇÃO: A síntese de novos compostos em escala nanométrica figura como uma alternativa para a obtenção de substância com características melhoradas para serem aplicados nos variodos processos químicos. Dentre essas aplicações podemos destacar a catálise heterogênea.
A preparação de catalisadores, eficientes e disponíveis em grande quantidade, figura como ponto crucial para que o país possa produzir insumos industriais de boa qualidade e até energia limpa de forma competitiva frente a outras fontes de energias.
O desenvolvimento de novos catalisadores é uma das metas da chamada Química verde, que visa principalmente a redução de cargas poluidoras sobre o meio ambiente. Some-se, ainda, a necessidade de redução de tempo e energia nos processos industriais com conseqüente diminuição de custos de produção.
O Brasil é um grande produtor de alumina, porém a maior produção é de alfa-alumina e esse tipo de alumina não apresenta boa atividade catalítica. Propomos a modificação da alfa-alumina no intuito de torná-la um bom catalisador heterogêneo, dessa forma podemos agregar valor a esse produto.
A alumina é um material cerâmico que se apresenta em diversas formas alotrópicas (estruturais) sendo a mais estável a forma α-Al2O3, corundum. Na literatura pode-se encontrar uma grande variedade de metodologias para obtenção de recobrimento em alumina [1-5]. Neste trabalho foi utilizado o método sol-gel [6], combinado com o método do precursor polimérico [7]. A grande vantagem desta metodologia reside no fato de que ocorre a formação de uma fina película do precursor polimérico na superfície das partículas facilitando a obtenção de nanocápsula na superfície de partículas sólidas.
MATERIAL E MÉTODOS: Para a obtenção do precursor polimérico foram utilizados nitrato de bário (ECIBRA, 99 %), ácido cítrico (CQA, 99,5%) e etilenoglicol(CROMOLINE, 99,5 %). A resina polimérica foi obtida a partir da dissolução de 10,00 gramas de nitrato de bário, em solução aquosa de ácido cítrico na proporção de 1:3 em razão molar, em seguida foi adicionado etilenoglicol, na razão de 1:1 em massa (metal alcalino-terroso: etilenoglicol). O precursor foi caracterizado por FTIR e gravimetria.
A alumina foi dispersa em água destilada, em seguida foi adicionada a resina sob agitação ultra-sônica. A resina fo1 adicionada de tal forma que depois do tratamento térmico a percentagem de metal alcalino-terroso fosse igual 5 % em mol.
As suspensões foram aquecidas em banho-maria a 90°C até completa evaporação da água. O material resultante foi tratado termicamente a 500°C por duas horas para decomposição do polímero, eliminação da matéria orgânica e modificação da superfície do suporte.
Os materiais foram caracterizados morfologicamente por microscopia ótica digital, equipamento TNB - 41T-PL - Opton e microscopia eletrônica de varredura, equipamento da Zeiss modelo FEG-VP Zeiss modelo Supra 35. A caracterização estrutural foi realizada por difração de raios X, equipamento DRX da Siemmens, modelo D-5000. As análises de área superficial específica e distribuição de tamanho de poros foram obtidas por intermédio da adsorção de N2 num equipamento Micrometrics ASAP 2000.
Para reação de transesterificação foram usados 50 mL de óleo, 32 mL de metanol e 2g de catalisador.
Utilizou-se um Cromatógrafo a gás, modelo Shimadzu GC-2010, com um detector de ionização em chama (CG-DIC), para quantificação, do teor de ésteres nas amostras de biodiesel metílico de babaçu obtidas na reação de transesterificação.
RESULTADOS E DISCUSSÃO: Os resultados de FTIR confirmam a formação da resinas de metais alcalino-terrosos e não foram observados picos referentes a contaminantes. Todas as resinas obtidas são límpidas e transparentes, levemente viscosas e solúveis em água.
O aluminato de bário exibe uma forte absorção em 1475 cm-1, na região do infravermelho, característica de ligação Ba-O, além das vibrações relativas aos estiramentos Al-O-Al na região compreendida entre 500 e 900 cm-1.
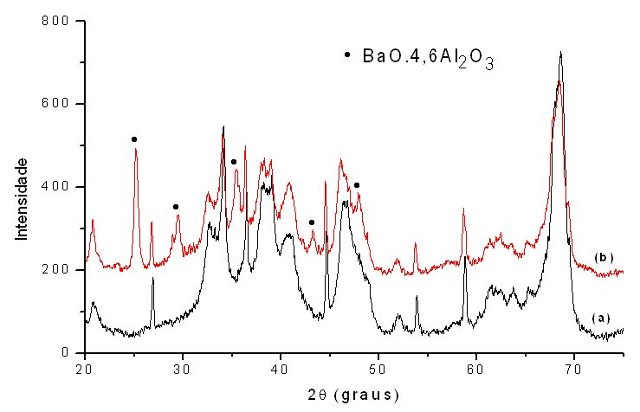
Na Figura 1 estão expostos os difratogramas de raios-x da alumina pura e modificada com 5 % de bário. Ambas as amostras foram tratadas termicamente a 700°C por duas horas. Na amostra de alumina modificada com bário, além das fases da alumina (α-Al2O3 e monoclínica), foi observada a fase do aluminato de bário BaO.4,6Al2O3 (ficha JCPDS N 33-0129). Não se observou nenhuma mudança nos picos de difração do suporte (alumina).
As micrografias do sólido obtido mostrou que a morfologia dos grãos de alumina pura sofreu mudança com o surgimento de uma nova fase finamente dividida e distribuída na superfície da alumina. Essa fase de aluminato de bário é composta por partículas nanométricas que recobrem a superfície do suporte.
A análise textural mostrou uma diminuição na área específica da alumina pura após a modificação de superfície. A alumina pura apresentou área específica de 58,2 m2/g, após a modificação da superfície com o alumnato de bário a área específica reduziu-se para 45,2 m2/g. Essa redução pode está relacionada ao fechamento de alguns poros na superfície das partículas da alumina.
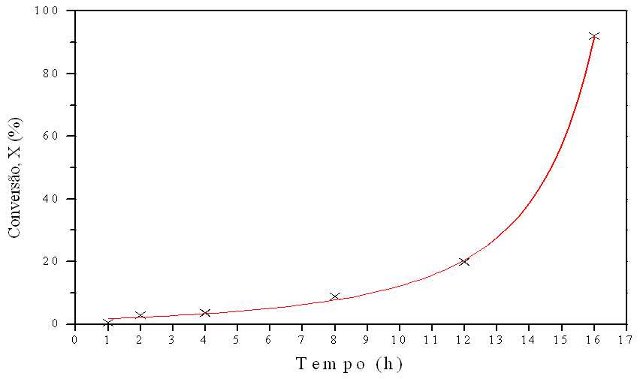
O material obtido exibiu boa conversão catalítica para reação de transesterificação do óleo de babaçu com metanol. Observou-se que a 16h de reação há uma conversão superior a 90%, vide Figura 2.
CONCLUSÕES: Com base nos resultados obtidos podemos concluir que o método dos precursores poliméricos é eficiente para obtenção de aluminato de bário em escala nanométrica na superfície de alumina pura.
O aluminato de bário superficial conferiu a alumina atividade catalítica para reação de transesterificação de óleo de babaçu com metanol. Esse resultado mostra que sólidos inativos pode ser transformados em bons catalisadores por modificações de superfície utilizando-se métodos químicos de preparação.
AGRADECIMENTOS: Os autores agradecem ao apoio financeiro do CNPQ, FAPEMA, FAPESP e FINEP.
REFERÊNCIAS BIBLIOGRÁFICA: 1. BOFFA, V.; TEN ELSHOF, J. E.; BLANK, D. H. A.; Preparation of templated mesoporous silica membranes on macroporous alpha-alumina supports via direct coating of thixotropic polymeric sols, Microporous and Mesoporous Materials, 100 (1-3), 173-182, 2007.
2. GREMILLARD, L.; CASADEI, R.; SAIZ, E.; TOMSIA, A. P.; Elaboration of self-coating alumina-based porous ceramics, Journal of Materials Science, 41 (16), 5200-5207, 2006.
3. BAO, Y. H.; NICHOLSON, P. S.; AlPO4 coating on alumina/mullite fibers as a weak interface in fiber-reinforced oxide composites, Journal of the American Ceramic Society, 89 (2), 465-470, 2006.
4. WANG, S. F,; HSU, Y. F.; YANG, T. C. K.; CHANG, C. M.; CHEN, Y.; HUANG, C. Y.; YEN, F. S.; Silica coating on ultrafine alpha-alumina particles. Materials Science and Engineering A-Structural Materials Properties Microstructure and Processing, 395 (1-2), 148-152, 2005.
5. NIKOLIC, L.; RADONJIC, L.; Alumina strengthening by silica sol-gel coating.
Thin Solid Films, 295 (1-2), 101-103, 1997.
6. ATTIA, S. M.; WANG, J.; WU, G. M.; SHEN, J.; MA, J. H.; Review on sol-gel derived coatings: Process, techniques and optical applications Journal of Materials Science & Technology, 18 (3), 211-218, 2002.
7. PECHINI, M., Method of preparing lead and alkaline earth titanates and niobates and coating method using the same to form a capacitor. Us Pat. No. 3330697, 1967.
