ÁREA: Química Analítica
TÍTULO: Uso de biomassa (casca de banana triturada) na remoção de cobre e chumbo em meio aquoso
AUTORES: CASTRO, R.S.D. (FCA /UNESP) ; FERREIRA, G. (IBB / UNESP) ; CAETANO, L. (FEIS / UNESP) ; MARTINES, M.A.U. (UFMS ) ; PADILHA, P.M. (IBB / UNESP) ; CASTRO, G.R. (IBB / UNESP)
RESUMO: O presente trabalho apresenta os resultados da aplicação da casca de banana triturada (após secagem em estufa)na remoção de íons cobre e chumbo em meio aquoso. Após secagem e caracterização do material por FTIR a fração de 100 a 150 micrometros foi selecionada para os experimentos. Os estudos cinéticos e da capacidade máxima de adsorção foram realizados pelo procedimento de batelada. Os estudos para a determinação do tempo de contato dinâmico revelaram uma cinética rápida, ~10 minutos. Os estudos de pH revelaram que o material pode ser aplicado em soluções ácidas, pH 3,0, com recuperação de ~100% e a capacidade máxima de adsorção calculada para os íons Cd(II) e Pb(II)após linearização das isotermas, utilizando a equação modificada de Langmuir, foi de 0,33 e 0,20 mmol/g, respectivamente.
PALAVRAS CHAVES: casca de banana; extração em fase sólida; íons metálicos
INTRODUÇÃO: A contaminação ambiental dos compartimentos com substâncias orgânicas e inorgânicas, como os metais potencialmente tóxicos e pesticidas, tem motivado o desenvolvimento de métodos de extração e purificação. Atualmente, uma grande variedade de espécies metálicas tóxicas entram nos compartimentos aquáticos através de processos como deposição atmosférica, lixiviação de áreas de cultivo e mineração, atividades industriais, resultado do crescimento populacional e das suas necessidades [1]. Assim, pesquisas relacionadas com a contaminação dos recursos hídricos por espécies metálicas tem atraído a atenção de diversos cientistas devido a grande capacidade de diluição dos corpos dágua, da possibilidade de bioacumulação de espécies metálicas em plantas e animais e dos efeitos tóxicos sobre os organismos.
Para a remoção destas espécies em meio aquoso, normalmente, são utilizados materiais como sílicas e celuloses modificadas em procedimentos de extração em fase sólida (SPE) e que apesar das vantagens o desenvolvimento de tais materiais apresenta um elevado custo [2]. Desta forma, diversos produtos naturais as vezes considerados resíduos, como o bagaço de cana de açúcar, casca de amendoim e casca de maça, têm sido empregados na remoção de metais de amostras aquosas [3,4], e esta possibilidade se deve a presença de grupos carboxílicos e fenólicos presentes nessas substâncias.
No presente trabalho, a casca de banana triturada foi caracterizada por FTIR para identificação de bandas relacionadas aos grupos funcionais responsáveis pela coordenação das espécies metálicas. Após a caracterização do material o mesmo foi submetido a experimentos em batelada para a determinação do tempo de contato dinâmico, influência do pH e determinação da capacidade máxima de adsorção em meio aquoso.
MATERIAL E MÉTODOS: Reagentes e equipamentos
Todos os reagentes utilizados foram de elevada pureza e as soluções foram preparadas com água desionizada em sistema Millipore (Direct-Q). As espécies metálicas foram determinadas por espectrometria de absorção atômica (AAS, Perkin Elmer AA700). Nos experimentos de adsorção, a casca de banana triturada, foi separada da solução sobrenadante por centrifugação a 3500 rpm (Centrífuga FANEM Excelsa II).
Caracterização da casca de banana
A superfície da casca de banana triturada foi caracterizada por espectroscopia na região do infravermelho (FTIR, Nicolet Nexus 670) com 1 mg do material misturado com 500 mg de KBr.
Experimentos em batelada
Alíquotas de 10 mL da solução padrão dos metais (10 mg/L) foram transferidas para frascos tipo Falcon de 50 mL onde adicionou-se 0,02 g de casca de banana triturada. A suspensão foi agitada mecanicamente em um intervalo de 1-60 minutos a temperatura ambiente (28°C). O efeito do pH na extração foi investigado em um intervalo de 1-5, o qual foi ajustado com NaOH e HNO3 diluído. A capacidade de adsorção dos metais (Nf) foi determinada utilizando alíquotas de 10 mL de soluções em um determinado intervalo de concentração, de acordo com a seguinte equação: Nf = (ni ns)/m. Onde ni representa o número de mol inicial, ns representa o número de mol no sobrenadante depois da extração e m representa a massa da casca de banana utilizada no experimento. A concentração residual do metal no sobrenadante foi determinada por espectrometria de absorção atômica.
RESULTADOS E DISCUSSÃO: O espectro de infravermelho revelou presença de bandas na região de 3486 e 3286 cm-1 atribuídas a estiramentos de grupos O-H, na região de 2920 e 2951 cm-1 atribuídas a estiramento de C-H e em 1730 cm-1 atribuída a ligação C=O de ácidos carboxílicos, como pode ser observado na Figura 1.
Após a aplicação do material no experimento em função do tempo verificou-se uma recuperação superior a 95% para as duas espécies em um tempo de 10 minutos, apresentando uma cinética rápida e em concordância com outros trabalhos da literatura [2]. O estudo da influência do pH revelou que o material pode ser aplicado na extração de cobre e chumbo em soluções / amostras ácidas, pois a recuperação foi superior a 95% em pH 3. Neste valor de pH muitos materiais apresentam uma recuperação reduzida devido a protonação dos sítios de adsorção.
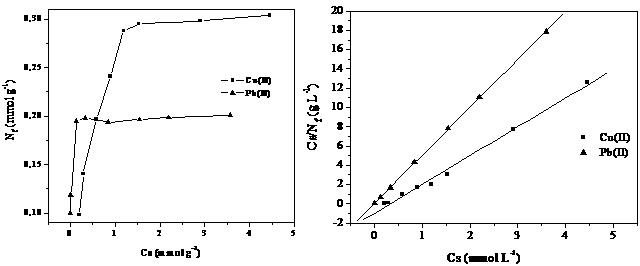
Os resultados mostraram uma capacidade de adsorção de 0,30 e 0,20 mmol/g para cobre e chumbo, respectivamente (Figura 2a). A maior capacidade de extração de íons Cu(II) pode ser explicada pelo fato do grupos carboxílico, considerado base dura [5], ter grande afinidade por ácidos duros, como o cobre. Íons Pb(II) são considerados moles devido ao seu grande raio iônico e elevada polarizabilidade, fazendo com que sua extração ocorra em menor extensão. A capacidade máxima de adsorção foi determinada utilizando a equação modificada de Langmuir: Cs/Nf = Cs/ Ns + 1/Ns b. Onde Cs é a concentração da solução em equilíbrio (mmol/L), Nf é a quantidade da espécie adsorvida na massa de casca de banana (mmol/g), Ns é a quantidade máxima da espécie adsorvida na massa de casca de banana (mmol/g). Assim os valores de Ns, baseados nas isotermas de adsorção linearizadas (Figura 2b), para os íons cobre e chumbo foram 0,33 e 0,20 mmol/g, respectivamente.

CONCLUSÕES: Com base nos resultados apresentados para a aplicação da biomassa (casca de banana) na adsorção / remoção de íons Cu(II) e Pb(II) em meio aquoso pode-se concluir que o material apresenta capacidade de adsorção semelhantes aos materiais sintéticos, 0,33 e 0,2 mmol/g para Cu(II) e Pb(II), respectivamente. O bom funcionamento do material também em valores de pH ácido (pH 3) sugere uma possível aplicação do mesmo na remoção de espécies metálicas tóxicas em efluentes industriais. Dentre as várias vantagens na utilização da casca de banana a principal delas esta relacionada ao seu baixo custo.
AGRADECIMENTOS: FAPESP Proc: 2006/54946-9
REFERÊNCIAS BIBLIOGRÁFICA: [1] Minello, M. C.; Paçó, A. L.; Martines, M. A. U.; Caetano, L.; Santos, A.; Padilha, P. M.; Castro, G. R. Sediment grain size distribution and heavy metals determination in a dam on the Paraná River at Ilha Solteira, Brazil. J. Environ. Sci. Health. Part A Toxic/Hazard. Subst. Environ. Eng. 44 (2009) 861-865.
[2] Pereira, A. S.; Ferreira, G.; Caetano, L.; Martines, M. A. U.; Padilha, P. M.; Santos, A.; Castro, G. R. Preconcentration and determination of Cu(II) in a fresh water sample using modified silica gel as a solid-phase extraction adsorbent. J. Hazard. Mater. 175 (2010) 399-403.
[3] Gurgel, L. V. A.; Gil, L. F. Adsorption of Cu(II), Cd(II) and Pb(II) from aqueous single metal solutions by succinylated twice-mercerized sugarcane bagasse functionalized with triethylenetetramine. Water Res. 43 (2009) 4479-4488.
[4] Johnson, P. D.; Watson, M. A.; Brown, J.; Jefcoat, I. A. Peanut hull pellets as a single use sorbent for the capture of Cu(II) from wastewater. Waste Manage. 22 (2002) 471-480.
[5] Pearson, G. R. Hard and soft acids and bases. J. Am. Chem. Soc. 85 (1963) 3533-3539.
