ÁREA: Produtos Naturais
TÍTULO: ASSOCIAÇÃO QUITOSANA/ZEÓLITO NA ADSORÇÃO DE METAIS PESADOS
AUTORES: BATISTA, A C L (UNICAP/RENOR) ; VILLANUEVA, E (UVIGO) ; TAVARES, T (DEB/UMINHO) ; CAMPOS-TAKAKI, G M (UNICAP)
RESUMO: O presente trabalho propõe a utilização do conjugado quitosana/zeólito (CH/Zeo) como membrana na adsorção de metais pesados em solução. As soluções padrões de metal Cr(VI) e Pb(II) foram ajustadas para pH 4 e 6 e, então diluídas nas concentrações de 26 260mg/L. O "uptake" da capacidade de adsorção das membranas em solução foi calculado por balanço de massa e as isotermas de equilíbrio foram ajustadas para os modelos de Langmuir, Freundlich e Redlich-Peterson. As análises por infravermelho demonstraram que houve ligação entre a CH e Zeo nas bandas dos grupos funcionais amina I e II. A CH demonstrou ser um importante ligante de metais a pH 4, contudo a sua instabilidade desfavoreceu a sua utilização isolada. A ligação CH/Zeo vem favorecer experimentos posteriores na adsorção de metais.
PALAVRAS CHAVES: quitosana, zeolito, metal pesado
INTRODUÇÃO: INTRODUÇÃO: O desenvolvimento industrial vem revolucionando a economia global trazendo benefícios sociais a diversos países, contudo esse desenvolvimento, em sua maioria, promove o depósito de substâncias de ação recalcitrante no meio ambiente. Por esse motivo diversos pesquisadores vêm trabalhando na proposição de substâncias e técnicas que possam favorecer a montagem de uma estratégia rentável de tratamento de áreas poluídas (SILVA et al., 2008, AHMARUZZAMAN, 2008, SUKSABYE et al., 2008, BARRIADA et al., 2008, BRINZA et al., 2009, QUINTELAS et al., 2009, WANG and CHEN, 2009), contudo, em geral, elas apresentam alto custo e não são úteis na remoção de baixas concentrações tóxicas.
Um produto rentável economicamente para ser usado no tratamento de áreas poluídas deve requerer pouco processamento, ser abundante na natureza, ou ser um subproduto ou material residual proveniente de outro setor (BAILEY et al., 1999). Considerando esses fatores, estudos atuais têm demonstrado resultados satisfatórios em processo de biorremediação por adsorção de metais pesados do solo e de sistemas aquáticos com a utilização da quitosana (CH), um produto natural, de fácil obtenção e abundante na natureza (JEON; PARK, 2005; CESTARI et al., 2005, LIMA, 2005).
Devido a alta solubilidade da CH em solução ácida, a associação da quitosana com zeólito (Zeo) vem sendo sugerida na melhora das características físico-químicas da membrana de CH (KITTUR et al., 2005).
Até o presente momento, essa combinação CH/Zeo na formação de membranas já foi descrita por diversos autores no uso de sistemas de separação de líquidos por pervaporização (LIU et al., 2007, WANG et al., 2008). Assim, o presente trabalho propõe a utilização do conjugado quitosana/zeólito na adsorção de metais pesados em solução.
MATERIAL E MÉTODOS: MATERIAIS E MÉTODOS: A CH foi obtida da Aqua Premier Company, Thailandia e o Zeo 13X a partir da Xiamen Zhongzhao Imp. & Exp. Co., Ltd. Antes de ser utilizado o Zeo foi macerado e calcinado. A preparação das membranas de CH (0,5 2,5% p/v ácido acético 1% v/v) e CH/Zeo (1:10 p/p ácido acético 1% v/v) foi realizada de acordo com LIU et al., 2007, com pequenas modificações. A mistura CH/Zeo permaneceu por 1h em banho ultrasônico com freqüência fixa de 50kHz. A solubilidade foi realizada segundo GONTARD et al. 1994, com pequenas modificações. O peso das membranas de CH e CH/Zeo variou entre 8 10mg e 47 55mg, respectivamente. As soluções padrões de metal foram preparadas pela diluição em água destilada de K2Cr2O7 e Pb(NO3)2 e ajustado o pH das soluções para 4 e 6. Os padrões foram diluídos nas concentrações de 26 260mg/L. Os experimentos de adsorção foram conduzidos em batelada (150rpm/12h/25ºC), em frasco de 1L com rosca contendo 500mL de solução de metal, nas diferentes concentrações, e uma membrana de CH, CH/Zeo ou as esferas de Zeo (controle). O branco do experimento foi realizado utilizando água destilada. Pequenas alíquotas foram retiradas em diferentes tempos, centrifugadas (5000rpm/10min) e mensuradas (CLESCERI et al. 1998). O "uptake" da capacidade de adsorção das membranas foi calculado por balanço de massa. As isotermas de equilíbrio foram ajustadas para os modelos de Langmuir, Freundlich e Redlich-Peterson. Durante os experimentos o pH das soluções não foi controlado na tentativa de aproximar o experimento das condições reais de aplicação. Os experimentos de desorção foram realizados segundo ZHAO et al. 2007, com pequenas modificações. As alíquotas foram mensuradas segundo CLESCERI et al. 1998. O infravermelho foi realizado segundo KITTUR et al. 2005.
RESULTADOS E DISCUSSÃO: RESULTADOS e DISCUSSÃO: As análises por infravermelho demonstraram que houve ligação da CH e Zeo nas bandas dos grupos funcionais amina I e II (KITTUR et al. 2005). O aumento da solubilidade da membrana de CH é diretamente proporcional ao aumento da concentração da mesma (ASSIS e SILVA 2003, CASARIEGO et al. 2009). A ligação com Zeo aumentou a solubilidade da membrana (KITTUR et al 2005; LIU et al. 2007), contudo favoreceu a estabilidade física da membrana em solução. (GUIBAL et al. 2004, CHEN et al. 2008). A solubilidade das membranas em solução de metal foi dependente da concentração, pH e tipo de metal. Em experimentos de cinética, a membrana de CH demonstrou maior poder adsorvente quando comparado com a membrana CH/Zeo (Figura 1), entretanto em concentrações baixas (26mg/L) de solução de Cr(VI) ou em qualquer concentração de solução de Pb(II) a membrana de CH não foi fisicamente estável. O valor de pH sugerido para experimentos futuros é 4, devido a alta percentagem de grupos protonados na cadeia de CH, os quais interagem com o metal pesado mais facilmente (Figura 1) (YANG e ZALL 1984; RANGEL-MENDEZ et al. 2008). Devido ao baixo poder adsorvente da membrana de CH/Zeo para o Pb(II) e a baixa estabilidade física da membrana de CH em solução, os mesmo não foram avaliados quanto aos modelos de isotérmicas. Os modelos de isotérmicas propostos sugerem que o processo de adsorção de Cr(VI) por CH/Zeo ainda não entrou no patamar de equilíbrio (Figura 2) (PEHLIVAN e ARSLAN, 2007, ERTUGAY e BAYHAN, 2007), sugerindo que ainda há sítios vazios na superfície de adsorção (Figura 2). Segundo AKHTAR et al. (2007) a interação direta entre os compostos não consumiu energia de reação, havendo apenas interações físico-químicas entre o Cr(VI) e a membrana CH/Zeo.

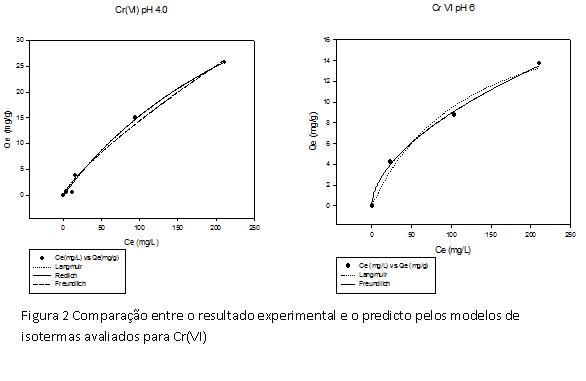
CONCLUSÕES: CONCLUSÃO: A CH demonstrou ser um importante ligante de metais, contudo a sua instabilidade a baixos pHs e em solução desfavorece a sua utilização isolada. Assim, a ligação CH/Zeo vem favorecer experimentos posteriores onde seja utilizada a membrana como agente adsorvente a outros metais e em concentrações diferentes onde se possa encontrar o equilíbrio isotérmico.
AGRADECIMENTOS: AGRADECIMENTOS: Ao suporte financeiro da CAPES, CNPq, UMINHO (Portugal) e UNICAP-PE; ao Prof. Dr. António Soares Vicente da UMINHO, por gentilmente ceder a CH.
REFERÊNCIAS BIBLIOGRÁFICA: AHMARUZZAMAN, M. D. 2008. Adsorption of phenolic compounds on low-cost adsorbents: A review. Advances in Colloid and Interface Science, 143: 48-67.
AKHTAR, K.; AKHTAR, M.W.; KHALID, A.M. 2007. Removal and recovery of uranium from aqueous solutions by Trichoderma harzianum. Water Research, 41: 13661378.
ASSIS, O. B. G.; SILVA, V. L. 2003. Caracterização Estrutural e da Capacidade de Absorção de Água em Filmes Finos de Quitosana Processados em Diversas Concentrações. Polímeros: Ciência e Tecnologia, 13: 223-228.
BAILEY, S. E.; OLIN, T. J.; BRICKA, R. M.; ADRIAN, D. D. 1999. A review of potentially low-cost sorbents for heavy metals. Journal of Hazardous Materials, 152: 11551163.
BARRIADA, J. L.; HERRERO, R.; PRADA-RODRÍGUEZ, D.; VICENTE, M. E. S. 2008. Interaction of mercury with chitin: A physicochemical study of metal binding by a natural biopolymer. Reactive & Functional Polymers, 68: 16091618.
BRINZA, L.; NYGÅRD, C. A.; DRING, M. J.; GAVRILESCU, M.; BENNING, L. G. 2009. Cadmium tolerance and adsorption by the marine brown alga Fucus vesiculosus from the Irish Sea and the Bothnian Sea. Bioresource Technology, 100: 17271733.
CASARIEGO, A.; SOUZA, B.W.S.; CERQUEIRA, M.A.; TEIXEIRA, J.A.; CRUZ, L.; DI´AZ, R.; VICENTE, A.A. 2009. Chitosan/clay films properties as affected by biopolymer and clay micro/nanoparticles concentrations. Food Hydrocolloids, 23: 1895-1902.
CESTARI, A. R.; VIEIRA, E. F.S.; MATOS, J. D.S.; ANJOS, D. S.C. 2005. Determination of kinetic parameters of Cu(II) interaction with chemically modified thin chitosan membranes. Journal of Colloid and Interface Science, 258: 288-295.
CHEN, A-H. ; LIU, S-C.; CHEN, C-Y.; CHEN, C-Y. 2008. Comparative adsorption of Cu(II), Zn(II), and Pb(II) ions in aqueous solution on the crosslinked chitosan with epichlorohydrin. Journal of Hazardous Materials, 154:184191.
CLESCERI, L. S.; GREENBERG, A. E.; TRUSSELL, R. R. 1989. Standard methods for the examination of water and wastewater. 17th ed., Washington.
ERTUGAY, N.; BAYHAN, Y.K. 2007. Biosorption of Cr(VI) from aqueous solutions by biomass of Agaricus bisporus. Journal of Hazardous Materials, 154: 432439.
GONTARD, N.; DUCHEZ, C.; CUQ, J.-L.; GUILBERT, S. 1994. Edible composite films of wheat gluten and lipids: water vapour permeability and other physical properties. International Journal of Food Science & Technology, 29: 39-50.
GUIBAL, E. 2004. Interactions of metal ions with chitosan-based sorbents: a review. Separation and Purification Technology, 38:4374.
JEON, C.; PARK, K. H. 2005. Adsorption and desorption characteristics of mercury(II) ions using aminated chitosan bead. Water Researcher, 39: 3938-3944.
KITTUR, A.A.; KULKARNI, S.S.; ARALAGUPPI, M.I.; KARIDURAGANAVAR, M.Y. 2005. Preparation and characterization of novel pervaporation membranes for the separation of waterisopropanol mixtures using chitosan and NaY zeolite. Journal of Membrane Science, 247: 7586.
LIMA, I. S.; LAZARIN, A. M.; AIROLDI, C. 2005. Favorable chitosan/cellulose film combinations for copper removal from aqueous solutions. International Journal of Biological Macromolecules, 36: 79-83.
LIU, B.; CAO, Y.; WANG, T.;YUAN, Q. 2007. Preparation of Novel ZSM-5 Zeolite-Filled Chitosan Membranes for Pervaporation Separation of Dimethyl Carbonate/Methanol Mixtures. Journal of Applied Polymer Science, 106: 2117-225.
PEHLIVAN, E., ARSLAN, G. 2007. Removal of metal ions using lignite in aqueous solution low cost biosorbents. Fuel Processing Technology, 88: 99106.
QUINTELAS, C.; FONSECA, B.; SILVA, B.; FIGUEIREDO, H.; TAVARES, T. 2009. Treatment of chromium(VI) solutions in a pilot-scale bioreactor through a biofilm of Arthrobacter viscosus supported on GAC. Bioresource Technology, 100: 220226.
RANGEL-MENDEZA, J. R.; MONROY-ZEPEDAB, R.; LEYVA-RAMOSB, E.; DIAZ-FLORESA, P. E.; SHIRAI, K. 2008. Chitosan selectivity for removing cadmium (II), copper (II), and lead (II) from aqueous phase: pH and organic matter effect. Journal of Hazardous Materials, 162: 503-511.
SILVA, B.; FIGUEIREDO, H.; QUINTELAS, C.; NEVES, I. C.; TAVARES, T. 2008. Zeolites as supports for the biorecovery of hexavalent and trivalent chromium. Microporous and Mesoporous Materials, 116: 555-560.
SUKSABYE, P.; THIRAVETYAN, P.; NAKBANPOTE, W. Column study of chromium(VI) adsorption from electroplating industry by coconut coir pith. Journal of Hazardous Materials, 160: 5662.
WANG, J.; CHEN, C. 2009. Biosorbents for heavy metals removal and their future. Biotechnology Advances, 27: 195226.
WANG, J; ZHENG, X.; WU, H.; ZHENG, B.; JIANG, Z.; HAO, X.; WANG, B. 2008. Effect of zeolites on chitosan/zeolite hybrid membranes for direct methanol fuel cell. Journal of Power Sources, 178: 9-19.
YANG, T. C.; ZALL R. R. 1984. Absorption of metals by natural polymers generated from seafood processing wastes. Industrial & Engineering Chemistry Product Research and Development, 23: 168-172.
ZHAO, F.; YU, B.; YUE, Z.; WANG, T.; WEN, X.; LIU, Z.; ZHAO, C. 2007. Preparation of porous chitosan gel beads for copper(II) ion adsorption. Journal of Hazardous Materials, 147: 67-73.
