ÁREA: Produtos Naturais
TÍTULO: ESTUDO QUÍMICO DE UM FUNGO ENDOFÍTICO DE POTHOMORPHE PELTATA.
AUTORES: AROUCHA, J. M. Z. (UFAM) ; PEREIRA, J. O. (UFAM) ; BARISON, A. (UFPR) ; AQUINO, P. F. (UFAM) ; MARCON, E. L. (UFAM) ; SOUZA, A. Q. L. (UEA) ; SOUZA, A. D. L. (UFAM)
RESUMO: Os fungos endofíticos são microorganismos capazes de produzir diversos metabólitos secundários de interesse farmacológico. As plantas do gênero Pothomorphe sp. pertencentes a família Piperaceae apresentam diversas atividades biológicas, incluindo a anticancerígena, e entre seus principais compostos estão monoterpenos, fenilpropanóis, substâncias fenólicas e alcalóides. Neste trabalho, será apresentada a caracterização do austdiol, composto mais abundante no líquido fermentado do fungo PpC1 1.2b, isolado do caule da planta Pothomorphe peltata. Esse metabólito foi purificado por fracionamento em coluna e recristalização e sua identificação foi feita através de análises espectroscópicas e espectrométricas (RMN de 1H e de 13C, HMBC e HSQC).
PALAVRAS CHAVES: fungo endofítico, pothomorphe peltata e austdiol
INTRODUÇÃO: Abundantes nas plantas, os fungos endofíticos estão entre os seres vivos menos conhecidos do planeta, particularmente, do ponto de vista químico, apesar do crescente aumento de interesse pelos seus metabólitos, especialmente após a descoberta de fungos que podem produzir substâncias semelhantes às das suas hospedeiras (ZHANG et al., 1997; STROBEL et al., 2004). Em contraste com a rica literatura botânica a respeito das plantas do gênero Pothomorphe, poucos são os registros sobre os seus microorganismos endofíticos. Logo, há um conhecimento muito restrito da química e do comportamento biológico dos microorganismos dessas plantas. Entretanto, com relação a pothomorphe peltalta, vários são os estudos realizados sobre suas atividades biológicas, como por exemplo: analgésica, anticancer, antimicrobiana, antibacteriana, antiinflamatória, antimalárica, antioxidante, fotoprotetora, entre outros (DI STASI et al., 2002).
Entre a gama de substâncias que os microorganismos podem produzir está a toxina gastrointestinal austdiol, principal metabólito tóxico de Aspergillus ustus. Esse policetídeo é um sólido cristalino amarelo e inodoro, de fórmula molecular C12H12O5 e que tem na citrinina um dos seus precursores (VLEGGAAR et a1., 1974). Neste trabalho, será apresentada a caracterização do austdiol, composto mais abundante no líquido fermentado do fungo endofítico PpC1 1.2b, isolado de Pothomorphe peltata. A sua identificação foi feita através de análises espectroscópicas e espectrométricas. Estudos dos metabólitos de microorganismos endofíticos justificam-se pela sua importância em diversos setores, especialmente na área farmacêutica.
MATERIAL E MÉTODOS: As partes coletadas da planta Pothomorphe peltata (folha, caule, inflorescência, raiz e haste) foram submetidas a um processo de desinfecção, o qual consistiu em uma lavagem com detergente líquido e água corrente. Seguiu-se, em câmara asséptica, a esterilização superficial com álcool 70%, tratamento com hipoclorito de sódio 3% por 4 minutos, nova imersão em álcool 70% por 30 segundos e finalmente a lavagem em água destilada e autoclavada. O material vegetal foi cortado e os fragmentos, colocados em placas de petri contendo três meios de cultura (BDA + Ext. lev. 0,2%, aveia e ISP2). Da água de lavagem 50 µL foram espalhados separadamente nos mesmos meios, para o controle da assepsia. A partir do terceiro dia os fungos endofíticos foram isolados e preservados pela metodologia de Castellani, em água com glicerol 15% e em óleo mineral.
Entre os fungos isolados, a linhagem PpC1 1.2b foi selecionada para o cultivo em larga escala, após análise em microscópio, onde foi observada a formação de cristais extracelulares. O fungo foi inoculado e incubado por 30 dias a 26-28 ºC em 50 erlenmeyers de 1 L contendo 300 mL do meio ISP2 sem ágar. O meio fermentado foi separado do micélio por filtração e particionado com acetato de etila e mistura deste com álcool isopropílico 8:2. Durante a concentração da fração em acetato de etila foi observada a formação de um precipitado, o qual foi submetido a purificação complementar em coluna de sílica e por recristalização, e codificado Pp01. A amostra obtida foi submetida a análises espectroscópicas e espectrométricas (RMN de 1H e de 13C, HMBC e HSQC) com dois solventes diferentes, o MeOD e o d6-DMSO.
RESULTADOS E DISCUSSÃO: No espectro de RMN de 1H da amostra PpC11.2b em MeOD foram observados seis sinais de hidrogênios, correspondentes a quatro grupos CH e dois CH3. No espectro de RMN de 13C, no mesmo solvente, foram observados 12 sinais, dois de carbonos de carbonilas, em 200,6 e 191,5 ppm, dois de carbonos carbinólicos e diversos na região de carbonos sp2. Um singleto em 8,20 ppm foi observado em conexão (HSQC) com um carbono em 154,7 ppm e em correlações a ligações múltiplas (HMBC) com carbonos em 73,4, 122,3, 150,6 e 168,3 ppm. Ao carbono em 73,4 ppm está conectado um hidrogênio em 4,43 ppm, correlacionado com carbonos em 200,6, cetônico, 154,7, 150,6, 122,3, 76,2, carbinólico e 22,9 ppm, metílico. Os hidrogênios desta metila, singleto em 1,24 ppm, têm correlações com o carbono carbonílico em 200,6 ppm e os carbinólicos em 73,4 e 76,2 ppm. O outro sinal de hidrogênio, singleto largo em 8,53 ppm, foi observado em conexão com um carbono em 109,0 ppm e em correlações com os sinais de carbonos em 168,3, 122,3, 109,7 e 20,3 ppm, metílico. Os hidrogênios desta metila foram observados como um dupleto em 2,44 ppm (0,5 Hz), correlacionado com os carbonos em 168,3 e 109,0 ppm. O sinal mais desblindado, em 10,03 ppm, típico de hidrogênios de aldeídos, foi observado em conexão com o carbono em 191,5 ppm e em correlações com os carbonos olefínicos em 109,7, 150,6 e 122,3 ppm. Os dados de RMN em d6-DMSO são coerentes com os apresentados acima e os complementam, principalmente pelas correlações observadas nos espectros de HMBC e HSQC para os hidrogênios alcoólicos da amostra, os quais não foram naturalmente detectadas em MeOD. As informações obtidas por RMN nos dois solventes e dados da literatura (POHLAND et a1., 1982) são compatíveis com a estrutura do austdiol (figura 1).
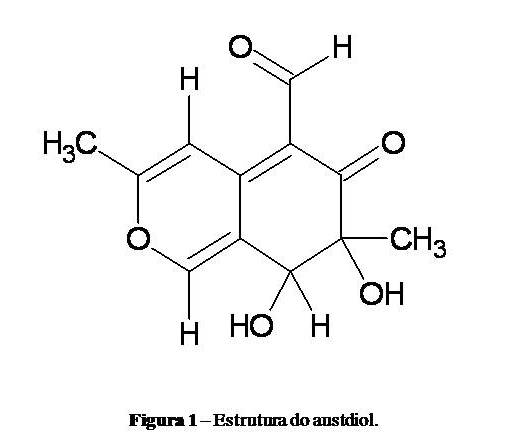
CONCLUSÕES: O estudo químico do fungo endofítico não identificado PpC1 1.2b, obtido de Pothomorphe peltata, levou a identificação do sólido cristalino Pp01 como sendo o austdiol, um policetídeo com fórmula molecular C12H12O5, isolado anteriormente do fungo Aspergillus ustus.
AGRADECIMENTOS: A FAPEAM, ao CNPQ, pelo apoio financeiro aos trabalhos realizados e aqui parcialmente apresentados.
REFERÊNCIAS BIBLIOGRÁFICA: STROBEL, G.; DAISY, B.; CASTILLO, U.; HARPER, J. Natural products from endophytic microorganisms. J. Nat. Prod., 2004.
VLEGGAAR, R.; STEYN, P. S. ; NAGEL, D. W. J. Chem. Soc.,Perkin Trans. I, 1974.
ZHANG, W.; WENDEL, J. F.; & CLARK, L. G. Bamboozled again! Inadverted isolation of fungal rDNA sequences from bamboos (Poaceae: Bambusoideae). Molecular Phylogenetics and Evolution, 8(2): 205-217, 1997.
DI STASI, L.C. & HIRUMA-LIMA, C.A. Plantas medicinais na Amazônia e na Mata Atlântica. 2. ed. São Paulo: Editora Universidade Estadual Paulista, 2002. 604p.
POHLAND, A. E.; SCHULLER, P.L.; STEYN, P. S. Physicochemical data for some selected mycotoxins. Pure & Apply Chem, vol. 54, nº 11, p. 2219-2284, 1982.
