ÁREA: Produtos Naturais
TÍTULO: Investigação Fitoquímica e avaliação da atividade alelopática das folhas de Derris urucu (Killip et Smith) Macbr. (Leguminosae)
AUTORES: SILVA, G. A (UFPA) ; SANTOS, A. K. S. (UFPA) ; LOBO, L. T. (UFPA) ; SOUZA FILHO, A. P. S. (EMMBRAPA) ; ARRUDA, M. S. P (UFPA) ; SILVA, M. N. (UFPA) ; GUILHON, G. M. S. P. (UFPA) ; ARRUDA, A. C. (UFPA) ; SANTOS, L. S (UFPA)
RESUMO: Derris urucu é uma planta da Amazônia com propriedades inseticida e ictiotóxica1. Estudos com esta espécie reportam a presença de flavonóides, principalmente os rotenóides2. A partir do extrato etanólico das folhas de Derris urucu (Leguminosae), três novos diidroflavonóis, codificados como Urucuol A (S1),Urucuol B (S2), Urucuol C (S3) e a Isotirumalina foram isolados por CLAE e identificados por técnicas de RMN uni e bidimencionais. As substâncias isoladas foram submetidas a ensaios de atividade alelopática frente a invasoras de pastagens malícia (Mimosa pudica) e mata-pasto (Senna obtusifolia), objetivando-se encontrar um herbicida natural.
PALAVRAS CHAVES: diidriflavonol, derris urucu, clae.
INTRODUÇÃO: A espécie botânica Derris urucu (Leguminosae), conhecida popularmente como "timbó", é o alvo deste trabalho. Existem relatos na literatura, em que plantas do gênero Derris, assim como D. urucu, apresentaram atividades biológicas diversas e levaram ao isolamento de substâncias pertencentes à classe dos flavonóides. Inicialmente realizou-se uma investigação da atividade alelopática do extrato etanólico das folhas, para determinar o potencial de inibição da germinação de sementes, desenvolvimento da radícula e hipocótilo das espécies daninhas Mimosa pudica (Malícia) e Senna obtusifolia (Mata-pasto); como os resultados foram positivos, iniciou-se o estudo fitoquímico. Com base em métodos cromatográficos, o extrato foi fracionado utilizando-se hexano, acetato de etila e metanol como fase móvel e sílica como fase estacionária. A fração acetato de etila foi selecionado para o isolamento de constituintes químicos com base nas características espectrométricas de RMN 1H; quatro substâncias foram isoladas e purificadas utilizando-se técnicas de CLAE e identificadas com base nos dados espectrais de RMN 1H, 13C e dados bidimensionais. As substâncias nomeadas como urucuol A, urucuol B, urucuol C e isotirumalina foram submetidas a ensaios alelopáticos na concentração de 150 ppm sobre plantas invasores pastagens. Os resultados mostraram um percentual de inibição muito baixo para todas as substâncias quando foram testados separadamente. Atividades importantes foram detectadas quando substâncias foram testadas aos pares; os resultados mais importantes foram obtidos na associação entre urucuol C e isotirumalina, que resultaram em inibição de 60% sobre radícula e de 39% sobre o desenvolvimento do hipocótilo da espécie Mimosa pudica.
MATERIAL E MÉTODOS: O extrato etanólico das folhas de D. urucu foi fracionado em CCVU com misturas dos solventes Hexano e Acetato de Etila, em ordem crescente de polaridade. A fração Acetato 100% foi submetida a um clean up e injetada em CLAE analítico (VARIAN) para obtenção de um gradiente, variando-se de 5-100% de B (Acetonitrila), em 60 min. Com base neste gradiente, o sistema que apresentou melhor separação foi: H2O:ACN 40:60, o qual foi empregado na separação. Para o isolamento dos compostos, utilizou-se uma coluna Gemini C18, 5 micra, 250 x 10,0 mm, monitorada em comprimento de onda de 270 e 320 nm, com fluxo de 4.7 ml/min, obtendo-se as seguintes frações: S1 (71 mg), S2 (20 mg), S3 (80 mg) e S4 (28 mg). As substâncias isoladas foram submetidas à ensaios de germinação de sementes, desenvolvimento da radícula e hipocótilo na concentração de 150 ppm, usando como testemunho água destilada.
RESULTADOS E DISCUSSÃO: A análise dos espectros de RMN de 1H e 13C (uni e bidimensionais) indicou que todas as estruturas apresentam o esqueleto básico dos diidroflavonóides. Os espectros de RMN de 1H de S1-S4 apresentam, em comum, sinais característicos de H-2 e H-3 relativo ao anel C; sinais de sistema AMX aromático, atribuído a anel B trisubstituído, bem como singleto aromático relacionado a anel A pentasubstituído. As substâncias S1, e S2, apresentam também, em comum, o sinal de hidroxila quelada; S3 e S4 diferenciam-se pela metilação na posição C-5; S2, S3 e S4 apresentam o anel 2,2-dimetilpirano ligado nas posições C6-C7, enquanto que S1 possui o grupo C-prenil na posição C-6. As posições C-4` e C-3` de todas as substâncias são metoxilada e hidroxilada, respectivamente, à exceção de S4, que apresenta metoxila nas duas posições (Figura 1). As substâncias S1, S2 e S4 foram submetidas a testes para avaliação de atividade alelopática na concentração de 150% (m/V), utilizando como tratamento testemunha água destilada. No bioensaio de germinação de sementes, observou-se que S4 inibiu 26 e 16%, respectivamente, para malícia e mata-pasto. Enquanto que no teste da radícula, S2 inibiu 14% para malícia e S1 23% para mata-pasto. E para o bioensaio do hipocótilo, S1 inibiu 25 e 28%, respectivamente, para malícia e mata-pasto. Aos pares, S1 + S4, apresentou melhor resultado, inibindo 7% da germinação de mata-pasto; inibindo 60% no desenvolvimento da radícula de malícia, 19% de mata-pasto e 39% no desenvolvimento do hipocótilo de malícia, enquanto o par S1 + S2 inibiu 24% do hipocótilo de mata-pasto.
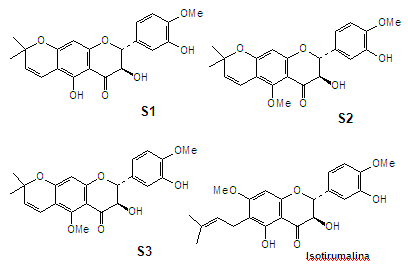
CONCLUSÕES: Os resultados observados nos testes para avaliação de atividade alelopática das substâncias isoladas de folhas de D. urucu foram pouco significativos, porém observou-se melhores resultados com as substâncias aos pares, especialmente o par S1 + S4, que inibiu 60% do desenvolvimento da radícula de malícia, evidenciando sinergismo. Levantamento bibliográfico preliminar indicou que três diidroflavonóis isolados de folhas de D. urucu (S1, S2 e S3) são estruturas inéditas.
AGRADECIMENTOS: Ao CNPq/FINEP/PPG7 e a CAPES pelo apoio financeiro. A UFPA e a EMBRAPA pela infra-estrutura para realização do trabalho.
REFERÊNCIAS BIBLIOGRÁFICA: 1 Mascaro , U. C. P., et al. Pesquisa Veterinária Brasileira 18(2):53-56,1998.
2Cravero, E. S.; Guerra, M. de S.; Silveira, C. P. D. da. Manual de inseticidas e acaricidas: aspe ctos toxicológicos. Pelotas, Aimara, 1976.
