ÁREA: Química Analítica
TÍTULO: SÍNTESE, CARACTERIZAÇÃO E ESTUDO TERMOANALÍTICO DOS L-TARTARATOS DE Ce (III) E Nd (III)
AUTORES: AMBROZINI, B. (AFA) ; DAMETTO, P. R. (UNESP) ; CARVALHO, C. T. (AFA) ; LOCATELLI, J. R. (UNESP) ; IONASHIRO, M. (UNESP)
RESUMO: RESUMO: Foram sintetizados no estado sólido, compostos do tipo Ln-Tar em que Ln representa os íons trivalentes cério (Ce) e neodímio (Nd), e Tar representa o L-Tartarato. Esses compostos foram caracterizados, utilizando-se as técnicas de espectroscopia de absorção na região do infravermelho, complexometria, termogravimetria análise térmica diferencial simultânea (TG-DTA) e calorimetria exploratória diferencial (DSC). Os resultados forneceram informações com respeito à estequiometria, desidratação, estabilidade e decomposição térmica desses compostos.
PALAVRAS CHAVES: palavras chave: l-tartaratos, lantanídeos, comportamento térmico.
INTRODUÇÃO: INTRODUÇÃO: A análise térmica é um grupo de técnicas em que uma propriedade física de uma substância e/ou seus produtos de reação são medidos como uma função da temperatura, enquanto a substância é submetida a um programa controlado de temperatura (MACKENZIE, 1979).
Verifica-se um aumento relativamente grande de pesquisas que utilizam as técnicas termogravimétricas como TG/DTG, TG-DTA e DSC para caracterizar e estudar o comportamento térmico de materiais.
O Ácido tartárico (ácido dihidroxi-butanodióico) é um composto orgânico de função mista que apresenta os grupos funcionais de ácido carboxílico e álcool. Este ácido não tem uma escala tão ampla de utilização quanto o ácido cítrico e málico, porém tem grande importância na indústria alimentícia. Ele é utilizado como acidulantes em alguns alimentos (acidulante INS 334) e também pode ser encontrado em alguns bolos ou sobremesas, onde é adicionado com o objetivo de captar pigmentos que se formem durante o cozimento e assim manter a cor original do produto (YALCIN et al., 2008). Entre os ácidos orgânicos da uva, o tartárico é o mais importante (RIZZON et al., 1998). É um ácido específico da uva e a videira é uma das raras plantas que o sintetiza em quantidade elevada, possibilitando sua extração comercial (RUFFNER et al., 1982).
Tendo em vista que poucos trabalhos envolvendo derivados do ácido tartárico e do ânion tartarato encontram-se descritos na literatura, compostos no estado sólido dos L-tartaratos de Ce (III) e Nd (III) foram preparados e investigados utilizando as técnicas TG-DTA, DSC, espectroscopia de absorção na região do infravermelho, e complexometria com solução padrão de EDTA.
MATERIAL E MÉTODOS: MATERIAIS E MÉTODOS: No presente trabalho foi sintetizado os L-Tartaratos de Ce (III) e Nd (III). O L-Tartarato de sódio foi adicionado aos respectivos cloretos destes metais. Os precipitados foram filtrados e lavados com água destilada até eliminação dos íons cloreto.
As curvas TG-DTA foram obtidas no termoanalisador SDT 2960, da TA Instruments. Este sistema é constituído de um comparador de massa horizontal com capacidade máxima de 2000 mg e precisão de ± 1% e um sistema de termopares controlados por um software Thermal Solutions da TA instruments. As análises das amostras foram realizadas no intervalo de 30 a 1200 ºC, razão de aquecimento de 20 ºC min-1, atmosfera de ar seco com fluxo de 100 mL min-1, cadinhos de α-alumina e massa da amostra da ordem de 7 mg.
As curvas DSC foram obtidas no DSC Q10 da TA instruments. As curvas DSC foram realizadas no intervalo de 30 a 600 ºC, razão de aquecimento de 20 ºC min-1, atmosfera de ar seco com fluxo de 50 mL min-1 e massa da amostra da ordem de 5 mg.
Os espectros de absorção na região do infravermelho foram obtidos com o emprego do espectrofotômetro Nicolet, FTIR, Impact-400, com resolução de 4 cm-1, na região compreendida entre 4000-400 cm-1, utilizando-se a técnica de pastilhas de brometo de potássio.
O teor total dos metais foi determinado por complexometria utilizando-se solução de EDTA como agente complexante e alaranjado de xilenol como indicador. As soluções de íons metálicos foram preparadas, a partir da calcinação de uma massa de cerca de 0,05 g dos compostos, para a conversão dos compostos nos seus respectivos óxidos. Os produtos da calcinação foram dissolvidos em HCl concentrado. Estas soluções foram devidamente tratadas e tituladas em triplicata.
RESULTADOS E DISCUSSÃO: RESULTADOS E DISCUSSÃO: A fórmula geral Ln2(C4H4O6)3.nH2O, onde n = 5 (Ce e Nd), foi estabelecida pelos resultados analíticos e termoanalíticos.
Os dados da espectroscopia de absorção na região do IV foram investigados com enfoque na faixa de 1700-1400 cm-1. As bandas do carboxilato no composto de Ce (III) e de Nd (III) foram observadas em: 1597 cm-1 (estiramento assimétrico COO-) e 1385 cm-1 (estiramento simétrico COO-). A região na qual ocorre estas bandas indica que o grupo COO- faz ligação bidentada com os lantanídeos com equalização incompleta devido a ligação fraca do ligante (LAM et al., 2003).
As curvas TG-DTA (Fig. 1) mostraram 2 etapas de perda de massa para o composto de cério e 5 para o de neodímio. Nas curvas TG, a primeira perda de massa entre 50 180 ºC foi atribuída à desidratação dos compostos.
Para o composto de cério, a decomposição térmica ocorre até 350°C, com formação de CeO2.
Para o composto de neodímio são observadas perdas de massa até 700°C, com aparecimento de picos endotérmicos e exotérmicos atribuídos à decomposição térmica, sendo eventos exotérmicos devidos à oxidação da matéria orgânica. Na etapa final de decomposição térmica o composto de Nd apresenta um pico endotérmico em 655°C, com formação de dioxicarbonato, como observado durante a decomposição térmica de outros compostos de lantanídeos (SIQUEIRA et al., 2008; IONASHIRO, et al., 2008). A última perda de massa é atribuída à decomposição térmica do intermediário e oxidação do resíduo carbonáceo, com formação de Nd2O3.
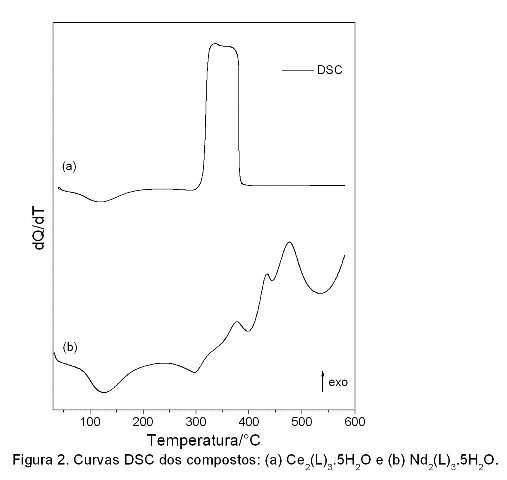
As curvas DSC (Figura 2) mostraram eventos endotérmicos e exotérmicos correspondentes às perdas de massa observadas nas curvas TG. O pico endotérmico entre 116-125°C é atribuído à desidratação, a qual ocorre em uma única etapa, sendo as entalpias 157,9 e 165,7 kJ mol-1 para Ce (III) e Nd (III), respectivamente.

CONCLUSÕES: CONCLUSÃO: Os resultados analíticos e termoanalíticos estabeleceram a fórmula geral para os compostos sintetizados.
O estudo dos espectros de absorção na região do infravermelho sugeriu que o L-Tartarato se coordena como um ligante bidentado com o respectivo lantanídeo.
As curvas TG-DTA e DSC forneceram informações não relatadas em outros trabalhos como comportamento térmico e decomposição térmica dos compostos sintetizados.
AGRADECIMENTOS: AGRADECIMENTOS: À FAPESP, CNPq e CAPES pelo apoio financeiro.
REFERÊNCIAS BIBLIOGRÁFICA: REFERÊNCIAS BIBLIOGRÁFICAS: IONASHIRO, E. Y.; BANNACH, G.; SIQUEIRA, A. B.; CARVALHO C. T.; RODRIGUES E. C.; IONASHIRO M. 2008. 2-Methoxybenzylidenepyruvate with heavier trivalent lanthanides and yttrium(III): Synthesis and characterization. Journal of Thermal Analysis and Calorimetry, 92: 953-959.
LAM, A. W. H.; WANG, W. T.; GAO, S.; WEN, G.; ZHANG, X. X. 2003. Synthesis, crystal structure, and photophysical and magnetic properties of dimeric and polymeric lanthanide complexes with benzoic acid and its derivatives. European Journal Inorganic Chemistry, 1: 149-163.
MACKENZIE, R. C. 1979. Nomenclature in Thermal Analysis, part IV. Thermochimica Acta, 28: 1-6.
RIZZON, L. A.; ZANUZ, M. C.; MIELE, A. 1998. Evolução da acidez durante a vinificação de uvas tintas de três regiões vitícolas do Rio Grande do Sul. Ciência e Tecnologia de Alimentos, 18: 179-183.
RUFFNER, H. P. 1982. Metabolism of tartaric and malic acids in Vitis: A review. Vitis, v: 247-259.
SIQUEIRA, A. B.; BANNACH, G.; RODRIGUES, E. C.; CARVALHO, C. T.; IONASHIRO, M. 2008. Solid-state 2-methoxybenzoates of light trivalent lanthanides: Synthesis, characterization and thermal behaviour. Journal of Thermal Analysis and Calorimetry, 91: 897-902.
YALCIN, D.; OZCALIK, E.; ALTIOK, E.; BAYRAKTAR, O. 2008. Characterization and recovery of tartaric acid from wastes of wine and grape juice industries. Journal of Thermal Analysis and Calorimetry, 94:767-771.
