ÁREA: Química Inorgânica
TÍTULO: (EMIm)3[Ln(pic)6] Uma nova série de complexos aniônicos
AUTORES: BORGES, A.S (UFMG) ; AYALA, J.D (UFMG) ; ARAÚJO, M.H (UFMG)
RESUMO: A síntese e o estudo do comportamento térmico dos complexos aniônicos dos picratos de lantanídeos(III) contendo como contra-íon o 1-etil-3-metilimidazol será discutida neste trabalho. A análise das curvas TG/DTG e DTA, obtidas em um equipamento TGA/DTA-60 Shimadzu, mostram que os compostos de coordenação de (EMIm)3[Ln(pic)6] (EMIm = 1-etil 3-metilimidazol; Ln = Sm3+, Pr3+ e Nd3+, pic = picrato), em atmosfera dinâmica de ar (80mL/mim) apresentam três etapas de decomposição e a 600ºC é obtido, como resíduo final, os respectivos Ln2O3.
PALAVRAS CHAVES: 1-etil-3-metilimidazol, lantanídeos(iii), análise térmica
INTRODUÇÃO: Líquidos iônicos (LI) são definidos como líquidos eletrolíticos constituídos apenas de íons e possuem temperaturas de fusão perto da temperatura ambiente, abaixo de 100ºC. Seu uso como solvente na química orgânica é hoje muito difundido. Com o surgimento da Química Verde e a preocupação com o meio ambiente e a saúde humana o uso dos solventes verdes tornou-se cada vez mais comum e suas aplicações estão sendo cada vez mais exploradas pelos grupos de pesquisa em todo mundo. Algumas propriedades dos LI, tais como a elevada solubilidade, janela eletroquímica larga e pressão de vapor muito baixa são responsáveis pela sua aplicação na indústria. Um novo ramo de pesquisa com LI vem surgindo com a formação de seus complexos com lantanídeos, com o objetivo de aproveitarem as propriedades tanto dos LI como dos íons metálicos. A aplicação em catálise e como eletrólitos em processos eletroquímicos, incluindo eletrodeposição, baterias e células solares, vem sendo investigada.
O trabalho foi iniciado com a síntese do emim(pic), em seguida a sua reação com o Ln(pic)3.xH2O, obtendo-se assim os complexos aniônicos. A introdução dos Ln(pic)3 como principais componentes dos LI fornecem maior estabilidade térmica.
MATERIAL E MÉTODOS: O 1-metilimidazol (Aldrich) foi purificados por destilação com uma pequena quantidade de KOH. A Acetonitrila (Vetec) foi seca através de destilação com uma pequena quantidade de P2O5. O ácido pícrico (nuclear), diclorometano (Vetec) e o bromo-etano (Aldrich) foram usados como recebidos. Os Ln2O3 foram adquiridos da Strem Chemical Inc. O 1-eti-3metilimidazol (emimBr) foi preparado em atmosfera de argônio, enquanto o emim(pic) em sistema aberto, assim como a reação para a formação do complexo. Os espectros de absorção na região do infravermelho dos LI, dos complexos e dos resíduos da TG a 800ºC, foram obtidos pela técnica em pastilhas de KBr na região de 4500 a 370 cm-1, utilizando um espectrofotômetro da Perkin Elmer FTIR GX, à temperatura ambiente. As curvas TG/DTG e DTA foram registradas em uma termobalança TGA/DTA-60 da Shimadzu, com aproximadamente 2 mg de amostra em cadinho de Al2O3, na faixa de temperatura de 25 a 800ºC , razão de aquecimento de 10ºC/min sob atmosfera dinâmica de ar (80mL/mim).
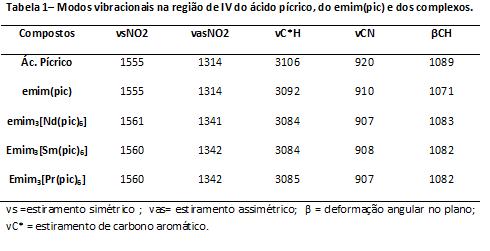
RESULTADOS E DISCUSSÃO: O emimBr foi sintetizado conforme(DUPONT et al.,2003). O emim(pic) foi preparado por extração com diclorometano a partir da solução aquosa do emimBr com picrato de potássio. As soluções dos sais de picrato foram lavadas três vezes com diclorometano, e após a evaporação do solvente os produtos foram secos sob vácuo a 50°C por 12h(75% de rendimento). Foi realizada a reação entre os Ln2O3 e o ácido pícrico em solução aquosa, obtendo-se Ln(pic)3.xH2O e em seguida a reação com emim(pic) em acetonitrila para se obter o complexo de fórmula (emim)3[Ln(Pic)6]. A Tabela 1 apresenta as bandas dos espectros de absorção na região de IV do ácido pícrico, do emim(pic) e dos complexos. O deslocamento dos estiramentos simétrico e assimétrico do grupo nitro (-NO2) para regiões de maiores números de ondas, quando comparamos o ácido pícrico com os complexos, sugere que o ãnion picrato se coordena aos íons lantanídeos de forma bidentada através do oxigênio fenólico e um dos oxigênios do grupo -NO2 adjacente. A análise das curvas TG/DTG e DTA, mostraram que os compostos são estáveis até temperaturas próximas á 250ºC, onde se iniciam a decomposição térmica em três etapas exotérmicas (Fig.2) para os complexos de Ln.
1ªETAPA(253ºC-365ºC): emim3[Ln(pic)6](s) ---> Ln(pic)3(s) + 3 emim(pic)
2ªETAPA(365ºC-470ºC): Ln(pic)3(s) + 1/2O2(g)---> LnOpic(s) + 2 pic
3ºETAPA(470ºC600ºC): 2LnOpic(s) + 1/2O2 ---> Ln2O3(s) + 2 pic

CONCLUSÕES: A síntese dos complexos de Ln(III) com picratos de líquidos iônicos, descrito neste trabalho, são inéditos. Estes complexos são estáveis até 250ºC e a decomposição térmica ocorre em três etapas exotérmicas, sendo o resíduo a 800ºC caracterizado como Ln2O3. Os complexos de Ln(III) com líquidos iônicos têm sido estudados como possíveis propulsores, pois a energia liberada em sua decomposição pode ser usada para este fim[6]. As soluções dos complexos de Ln(III), (Cat+)3[Ln(Pic3)6]3- , têm grande potencial também para aplicações em eletrodeposição, catálise e agentes de contrastes.
AGRADECIMENTOS: CNPq, FAPEMIG, UFMG
REFERÊNCIAS BIBLIOGRÁFICA: CONSORTI, Crestina S.; SOUZA, Roberto F. de; DUPONT, Jairton and SUAREZ, Paulo A. Z.. Líquidos iônicos contendo o cátion dialquilimidazólio: estrutura, propriedades físico-químicas e comportamento em solução. Quím. Nova, 24, 830-837, 2001.
Dupont, J., Consorti, C. S., Suarez, P. A., Souza, R. F. Org.Synth. Preparation of 1-butyl-3-methyl imidazolium-based room temperature ionic liquids. 79, 236, 2003;
Guo-Hong Tao, Yangen Huang, Jerry A. Boatz, and Jean_ne M. Shreeve ; Chem. Eur. J., Energetic Ionic Liquids based on Lanthanide Nitrate Complex Anions, 14, 11167 11173, 2008;
Koen Binnemans, Lanthanides and Actinides in Ionic Liquids, Chemical Reviews, 107, 6, 2593, 2007;
SILVA, Flavia Martins da; LACERDA, Paulo Sérgio Bergo de and JONES JUNIOR, Joel. Desenvolvimento sustentável e química verde. Quím. Nova, 28, 1, 103-110, 2005.
Welton, T., Wasserscheid P., Ionic Liquids in Synthesis, first edition, Wiley-VCH, pp. 1-2, 2002;
