ÁREA: Produtos Naturais
TÍTULO: PROCESSOS EXTRATIVOS PARA FLAVONÓIDES DE Bauhinia cheilantha (BONG) STEUDEL (PATA-DE-VACA)
AUTORES: PEIXOTO SOBRINHO, T.J.S. (UFPE) ; SILVA, T.C.L (UFPE) ; SILVA, C.H.T.P. (UFPE) ; ALBUQUERQUE, U.P. (UFRPE) ; AMORIM, E.L.C. (UFPE)
RESUMO: Os flavonóides são utilizados nas indústrias alimentícia, química e, principalmente, farmacêutica. B. cheilantha é um planta que possui vários usos na medicina popular, geralmente associado à flavonóides. Este trabalho apresenta uma avaliação do processo de extração por diferentes solventes orgânicos para flavonóides presentes nas folhas de B. cheilantha. As amostras foram coletadas em Caruaru, secas à temperatura ambiente e pulverizadas. Para a quantificação foi empregada metodologia analítica por espectrofotometria utilizando-se rutina como padrão e cloreto de alumínio como complexante. Verificou-se que acetona 80% possibilitou extração mais eficiente que os demais solventes. O uso de solventes orgânicos continua sendo uma excelente forma de se obter substância de interesse industrial.
PALAVRAS CHAVES: bauhinia cheilantha, flavonóides e extração
INTRODUÇÃO: Bauhinia cheilantha (Bongard) Steudel (pata-de-vaca ou mororó) é uma espécie nativa do Brasil e encontra-se amplamente distribuída na Caatinga (ALBUQUERQUE, 1997). Este gênero apresenta importantes propriedades medicinais atribuídas popularmente e testadas empiricamente, como antioxidante, antimicrobiana, hipocolesterolemiante e antidiabética, sendo estas atividades geralmente atribuídas às substâncias fenólicas (principalmente flavonóides) encontradas em suas folhas (ALBUQUERQUE et al, 2005; SILVA & CECHINEL FILHO, 2002).
Compostos fenólicos de origem vegetal são economicamente importantes sendo usados nas indústrias alimentícia, química e farmacêutica. Atualmente existem diversas metodologias de extração para estas substâncias bioativas, empregando-se geralmente a extração por solventes orgânicos (água, metanol, etanol e acetona) ou suas misturas (OLIVEIRA, 2005). Contudo, há uma grande dificuldade em estabelecer qual o melhor solvente ou sistema extrativo mais eficiente, já que vários fatores estão envolvidos neste processo, como a espécie, as propriedades físico-químicas das substâncias, o tempo e a temperatura da extração (ANDREO & JORGE, 2006).
Diante do exposto, o objetivo deste trabalho foi avaliar o processo de extração por diferentes solventes orgânicos (água quente, metanol p.a., metanol 80%, etanol p.a., etanol 80% e acetona 80% e 60%) para flavonóides foliares de B. cheilantha, utilizando-se para isto metodologia analítica de quantificação por espectrofotometria.
MATERIAL E MÉTODOS: As amostras de B. cheilantha foram coletadas durante os meses de abril-setembro/2006 na Estação Experimental de Caruaru da Empresa Pernambucana de Pesquisa Agropecuária, situado na Mesorregião do Agreste pernambucano (08º1418,2S e 35º5457,1) e a identificação foi realizada pelo Prof. Dr. Ulysses P. de Albuquerque. As folhas coletadas foram acondicionadas em sacos de papel e pulverizadas, após secagem à temperatura ambiente. A droga foi armazenada em sacos de papel até a realização das análises.
O padrão (rutina) foi preparado em balão volumétrico de 100mL, obtendo concentração final de 0,5 mg/mL. A curva de calibração foi construída utilizando cinco pontos (5, 10, 15, 20, 25, 30 µg/mL).
Cada fator foi analisado por seis determinações. A amostra vegetal (0,5g) foi transferida para erlenmeyers de 50mL, sendo adicionados 25mL do solvente extrator (água quente, MeOH p.a; MeOH 80%; EtOH p.a; EtOH 80%; Acetona; Acetona 80%) e aquecidos em placa de aquecimento até temperatura de ebulição por 30 minutos. Os extratos foram filtrados em papel de filtro e transferidos quantitativamente para balão volumétrico de 50mL. O resíduo do material foi lavado com 25mL do respectivo solvente e novamente filtrado para o balão, tendo o volume completado com o mesmo solvente.
Desta solução, foi pipetada e transferida a alíquota para balão volumétrico de 25mL, onde foram adicionados 0,6mL de ácido acético glacial, 10mL de solução piridina-metanol (2:8) e 2,5mL de uma solução metanólica de cloreto de alumínio a 5%, sendo utilizada água destilada para completar o volume do balão. Após intervalo de 30 minutos em repouso à temperatura ambiente, as leituras foram realizadas a 420 nm em cubetas de vidro.
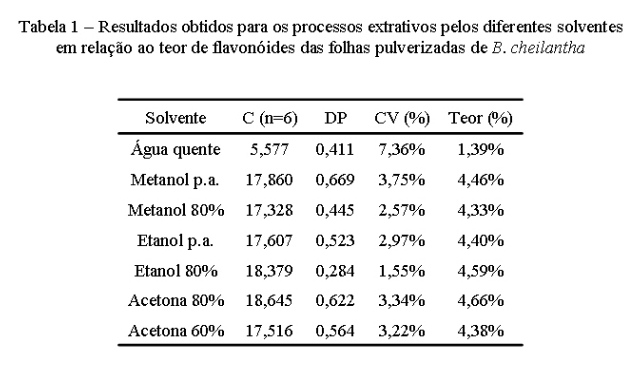
RESULTADOS E DISCUSSÃO: Na tabela 1 pode-se observar os resultados obtidos para a extração por diferentes solventes em relação ao teor de flavonóides das folhas pulverizadas de B. cheilantha. A equação de correlação e o valor de R2 obtidos foram, respectivamente, y = 0,0257x + 0,0135 e R2 = 0,9993.
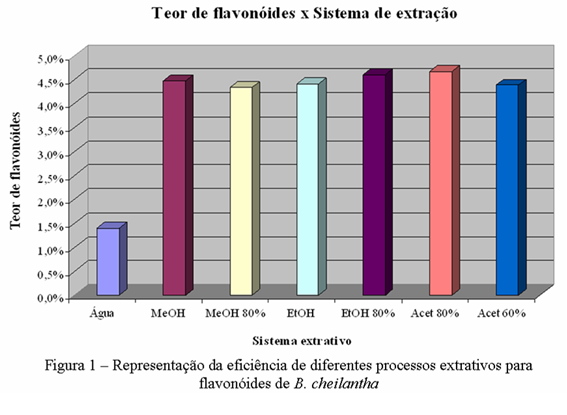
Através da Análise de Variância, ANOVA one way, podemos constatar que há diferenças significativas entre solventes (F=5,680>Fcrítico=2,534, P<0,005), indicando que o método de extração com acetona 80% foi mais eficiente, seguido por etanol 80% e metanol, como pode ser visto na figura 1.
Na literatura, este tipo de estudo tem sido realizado principalmente para taninos. A extração de taninos da aroeira-preta (Myracrodruon urundeuva), realizadas com metanol 80% e acetona 70% revelou que este último obteve um rendimento 3,7% maior que a extração hidroalcoólica, confirmando os resultados deste estudo (QUEIROZ et al, 2002).
Estes dados também puderam ser confirmados por AGOSTINI-COSTA et al (2003), que visando à extração de taninos de Anacardium occidentale, observou que a acetona 50-70% apresentou extração 30-50% superior.
Avaliando a extração de polifenóis contidos no fruto do cacau (Theobroma cacao) por metanol (100% e 50%), etanol (100% e 50%) e acetona (40%, 50% e 60%), KIM et al (2003) encontrou valores do rendimento para o metanol (8 e 17%), etanol (9 e 22%) e a acetona (19, 26 e 25%), revelando que o uso de acetona promoveu extrações mais eficientes.
Contudo, um estudo realizado com a finalidade de extrair produtos de T. cacao por metanol, clorofórmio, sistema I (clorofórmio, éter e dicloroetano) e sistema II (metanol e dicloroetano) visando substâncias fenólicas, mostrou que o metanol apresentou a melhor extração (AZIZAH et al, 1999).
CONCLUSÕES: Os resultados permitem concluir que para a extração de flavonóides foliares de B. cheilantha, a acetona 80% apresentou extração mais eficiente (com 95% de confiança), possibilitando teores mais elevados em relação à droga pulverizada. Os melhores resultados foram obtidos usando sistemas com água, reduzindo os custos da produção industrial.
A extração de flavonóides envolve diferentes metodologias, e estas possuem particular relação com suas propriedades físico-químicas. Contudo, o uso de solventes continua sendo a maneira mais eficiente de extrair substâncias para a aplicação nas indústrias.
AGRADECIMENTOS: À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior - CAPES.
REFERÊNCIAS BIBLIOGRÁFICA: AGOSTINI-COSTA, T.S.; LIMA, A.; LIMA, M.V. 2003. Determinação de tanino em pedúnculo de caju: método da vanilina versus método do butanol ácido. Química Nova. 26(5): 763-765.
ALBUQUERQUE, U.P. 1997. Folhas Sagradas: as plantas litúrgicas e medicinais nos cultos afro-brasileiros. Recife: Ed. Universitária UFPE, 195p.
ALBUQUERQUE, U.P.; ANDRADE, L.H.C.; SILVA, A.C.O. 2005. Use of plant resources in a seasonal dry forest (Northeastern Brazil). Acta Botanica Brasilica, 19(1): 27-38.
ANDREO, D.; JORGE, N. 2006. Antioxidantes Naturais: técnicas de extração. B. CEPPA, 24(2): 319-336.
AZIZAH, A.H.; RUSLAWATTI, N.M.; TEE, T.S. 1999. Extraction and caracterization of antioxidant from cocoa by-products. Food Chemistry, 64(2): 199-202.
KIM, K. H.; LEE, K.W.; KIM, D.Y.; PARK, H.H.; KWON, I.B.; LEE, H.J. 2003. Extraction and fractionation of glucosyltransferase inhibitiors from caco bean husk. Process Biochemistry, 70: 41-46.
OLIVEIRA, M.A. 2005. Extração de polifenóis da semente de cacau (Theobroma cacao). Dissertação (Mestrado em Engenharia Química) Universidade Federal de Santa Catarina, Florianópolis. 72p.
QUEIROZ, C.R.A. dos A.; MORAIS, S.A.L.; NASCIMENTO, E.A. 2002. Caracterizaçao dos taninos da aroeira-preta (Myracrodruon urundeuva). Revista Árvore, 26(4): 485-492.
SILVA, R. L.; CECHINEL FILHO, V. 2002. Plantas do Gênero Bauhinia: Composição química e potencial farmacológico. Química Nova, 25(3): 449-454.
