ÁREA: Química Inorgânica
TÍTULO: ATIVIDADE CATALITICA DE N-BENZOIL-GUANIDINAS DE COBRE(II) NA REAÇÃO DE OXIDAÇÃO DE PIROCATECOL
AUTORES: DE SOUZA, A.R. (IQ/UFG) ; QUINTINO, M.P. (IQ/UFG) ; FERREIRA, R.M.M. (IQ/UFG) ; DA SILVA, A.M. (NPQ/UCG) ; CUNHA, S. (IQ/UFBA)
RESUMO: Complexos de cobre(II) com N-benzoil-guanidina, [Cu(bmpg)Cl2], [Cu(bcmg)2], [Cu(bhpg)Cl]Cl.H2O e [Cu(bcpg)Cl2].H2O, foram preparados e estudados como catalisador da reação de oxidação do pirocatecol na presença de peróxido de hidrogênio, monitorando banda de 370 nm da formação da o-quinona equivalente.
Foi possível observar que todos os compostos preparados catalisam a reação de oxidação de pirocatecol, sendo que os compostos com esterioquímica tetraédrica, [Cu(bmpg)Cl2] e [Cu(bcpg)Cl2].H2O, apresentam maior atividade catalítica que os demais, kobs = 5,74 e 4,54 x 102 min-1, respectivamente.
PALAVRAS CHAVES: guanidina, cobre(ii), catálise
INTRODUÇÃO: Reações de complexos de Cu(I) e Cu(II) com O2 e as propriedades oxidativas desses sistemas (Cu/O2) tem atraído a atenção de muitos pesquisadores nas últimas décadas, principalmente, devido à relevância em sistemas bioquímicos e em processos de catálise. Diferentes aspectos destes sistemas têm sido revisados e as perspectivas no campo da ativação de O2 em processos bioquímicos e em catálise industrial têm sido discutidas [Tolman, 1997].
Interessantes avanços no conhecimento estrutural e nas propriedades químicas das metaloenzimas de cobre têm sido alcançados por meio do estudo de modelos de análogos sintéticos [Horn Jr., et al., 2005]. Muitos trabalhos mostram que a substituição de ligantes em complexos de cobre pode afetar as reações de oxigenação e oxidação, enquanto fornecem excelentes sistemas para estudos mecanísticos de oxidação. Ligantes usados para estabilizar cobre nos estados de oxidação (I/II/III) são frequentemente baseados em aminas funcionalizadas, que possuem grupos N,O e N, N-doadores [Ugozzoli, et al., 2002; Adams, et al., 2003].
Guanidinas são moléculas orgânicas que possuem em sua estrutura um carbono sp2 ligado a três átomos de nitrogênio. Sua estrutura permite a fomação de diferentes estruturas N, N, N-substituídas, sendo este um dos fatores mais atrativos na utilização desses compostos como ligantes [Bailey & Pace, 2001].
Nosso laboratório tem preparado diferentes complexos de cobre(II) com N-benzoil-guanidinas substituídas. Dando continuidade a esse trabalho, no objetivo aqui foi avaliar o potencial catalítico desses complexos frente a uma reação modelo de oxidação de pirocatecol.
MATERIAL E MÉTODOS: Os complexos de cobre(II) foram preparados pela reação direta entre cloreto de cobre(II) e a respectiva guanidina. Os estudos catalíticos foram realizados na região do UV (370 nm), utilizando um espectrofotômetro Ultrospec 2100 pro. Foi estudada a reação de oxidação do pirocatecol na presença de H2O2 catalisada pelos complexos [Cu(bmpg)Cl2] e [Cu(bcmg)2] em solução de clorofórmio, [Cu(bhpg)Cl]Cl.H2O em metanol e [Cu(bcpg)Cl2].H2O em diclorometano, para formação da o-quinona equivalente. As análises foram feitas com concentrações variando entre 10-5 mol/dm3 a 10-3 mol/dm3 dos complexos, 10-3 mol/dm3 de pirocatecol e 10-3 mol/dm3 de H2O2.
RESULTADOS E DISCUSSÃO: Uma série de complexos de cobre(II) com N-benzoil-guanidina com estruturas moleculares distintas foram preparados e caracterizados por difração de raios-X.
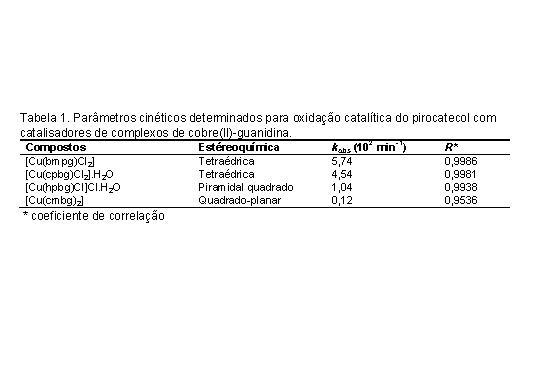
Os compostos foram estudados frente à catálise oxidativa do pirocatecol a o-benzoquinona. A medida da taxa de formação o-benzoquinona foi empregada para determinar a velocidade da reação de oxidação catalítica. A reação foi monitorada por espectroscopia no UV pelo aparecimento da banda em 370 nm da formação da o-quinona. Os gráficos de velocidade de cada composto mostraram que quando a concentração do complexo varia, numa dada concentração de catecol, a velocidade da reação aumenta linearmente até uma certa concentração do complexo. A atividade catalítica dos compostos foi avaliada pela determinação da constante cinética kobs para cada composto em função da concentração de cobre (Tabela 1).
Comparando as constantes (kobs) e a estrutura dos complexos, pode ser observado que complexos de geometria tetraédrica distorcida ([Cu(bmpg)Cl2] e [Cu(bcpg)Cl2].H2O), apresentam maior atividade catalítica. Enquanto que, complexos planares [Cu(bcmg)2] e [Cu(bhpg)Cl]Cl.H2O são menos ativos (kobs = 1,04 e 0,12), sugerindo que a atividade catalítica pode estar relacionada com a geometria do complexo.
CONCLUSÕES: Todos os compostos preparados nesse trabalho catalisam reação de oxidação de pirocatecol à correspondente o-quinona. Os compostos com esterioquímica tetraédrica apresentam maior atividade catalítica que os demais.
AGRADECIMENTOS: Os autores agradecem CNPq, a Capes, FUNAPE/UFG e ao LAMES da Universidade Federal de Goiás.
REFERÊNCIAS BIBLIOGRÁFICA: Adams, H., Clunas, S., Cummings, L.R., Fenton, D. E., Mahugh, P. E., Inorg. Chem. Comm. 6, 837, 2003.
Bailey, P. J., Pace, S., Chemistry Reviews, 214, 91, 2001.
Horn JR, A., Fernandes, C., Bortoluzzi, A. J., Vugnan, N. V., Herbst, H., J. Mol. Str., 749, 96, 2005.
Tolman, W. B., Acc. Chem. Res. 30, 227, 1997.
Ugozzoli, F., Massera, C., Lanfredi, A. M. M., Marsich, N., Camus, A., Inorg. Quim. Acta, 340, 97, 2002.
