ÁREA: Físico-Química
TÍTULO: OXIDAÇÃO ELETROQUIMICA DO CARBENDAZIM SOBRE ELETRODO DE PASTA DE CARBONO
AUTORES: RIGOTTI, M.G.M. (UEMS)
ARRUDA, G. J. (UEMS)
FIORUCCI, A. R. (UEMS)
RESUMO: Dentre os defensivos agrícolas existentes, o carbendazim é um fungicida, de atividade sistêmica, bastante aplicado para controle de doenças de final de ciclo em culturas de citrus, feijão, trigo e soja. O uso indevido deste e de outros pesticidas podem acarretar danos ao meio ambiente e ao homem. Este trabalho tem como objetivo estudar a reversibilidade do processo de oxi-redução da molécula de carbendazim, utilizando voltametria cíclica (CV) e eletrodo de pasta de carbono como eletrodo de trabalho. Os resultados obtidos mostraram que o processo não é puramente difusional, podendo ocorrer adsorção do carbendazim na superfície do eletrodo e que o processo de oxidação do carbendazim não é totalmente reversível podendo existir uma reação química acoplada ao processo de transferência de carga.
PALAVRAS CHAVES: carbendazim, voltametria cíclica
INTRODUÇÃO: Agrotóxicos ou defensivos agrícolas são denominações genéricas de substâncias utilizadas para o controle de animais ou vegetais que possam trazer problemas a agricultura ou saúde pública (DE QUEIROZ, 2001). Essas substâncias são utilizadas desde a antiguidade para combater pragas em lavouras, com o objetivo de aumentar a produtividade e a falta de monitoramento tem levado ao agravamento de problemas associados ao meio ambiente. O carbendazim (metil benzimidazol-2-il carbamato) pertencente ao grupo dos carbamatos benzimidazol, é um fungicida com atividade sistêmica e de eliminação rápida pelo metabolismo, registrado no país para as culturas de citros, feijão, trigo e soja, pois possui um importante papel no controle de doenças de final de ciclo por meio de aplicação foliar (DE LA HUEBRA, et al, 2000). Embora os métodos mais utilizados para determinação deste pesticida são técnicas cromatográficas, estudos voltamétricos também se mostram viáveis à determinação deste pesticida(DE LA HUEBRA, et al, 2000). Sendo assim, este trabalho tem como objetivo estudar a oxidação eletroquímica do carbendazim, utilizando voltametria cíclica e eletrodo de pasta de carbono como eletrodo de trabalho.
MATERIAL E MÉTODOS: As medidas foram realizadas em um Potenciostato/Galvanostato AUTOLAB PGSTAT30 (Eco Chemie), utilizando voltametria cíclica (CV), a temperatura ambiente, interfaciado a um microcomputador que dispõe de um programa AUTOLAB SOFTWARE ECOCHEMIE, para obtenção e tratamento de dados. A célula utilizada nas medidas voltamétricas é composta de três eletrodos: eletrodo auxiliar de folha de platina (Metrohm AG 9101 Herisau 8.109.1046), eletrodo de referência Ag/AgCl (Metrohm AG 9101 Herisau 8.109.1156) e o eletrodo de pasta de carbono como eletrodo de trabalho de área superficial de 34,21 mm2. A pasta de carbono foi preparada pela mistura de grafite sintético em pó, de granulometria < 20µm, (Aldrich), com o líquido aglutinante Nujol na proporção em massa de 75%:25%. As soluções estoque de carbendazim foram preparadas a partir de um carbendazim na forma comercial (Derosal 500 SC / Bayer) na concentração 3,125ppm. A solução tampão utilizada foi acetato de sódio/ácido acético 0.04 M; as análises foram realizadas em pH 4.2. Os voltamogramas foram obtidos nas seguintes velocidades: 50, 75, 100, 150, 200 e 250 mV/s.
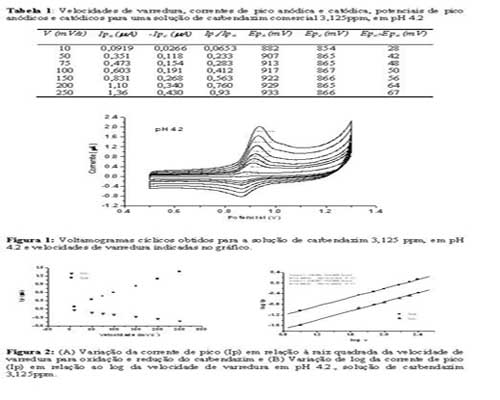
RESULTADOS E DISCUSSÃO: Os voltamogramas cíclicos obtidos, Fig. 1, sugerem um processo reversível, já que apresenta tanto o pico de oxidação (corrente anódica) quanto o de redução (corrente catódica). A Fig. 2A mostra a variação das correntes dos picos (Ip) em relação ao aumento da raiz quadrada da velocidade de varredura, que não é proporcional, indicando um processo quase-reversível (GREEF, R, et al, 1985). Para um processo totalmente reversível, Ipc/Ipa = 1 e a diferença entre os potenciais de pico (Epc−Epa) deve ser igual a 59/n mV. A Tabela 1 mostra que a razão entre Ipc/Ipa é menor que 1 e, assim como ΔEp, aumenta com a variação da velocidade de varredura, indicando que o processo eletródico não é totalmente reversível e que pode ter uma reação química acoplada (GREEF, R, et al, 1985). É possível observar o deslocamento de Epa e Epc para valores mais positivos, o que sugere um processo de transferência de elétrons posterior à reação química (NICHOLSON,R.S.; et al, 1964). Outra observação importante é a relação de log Ip vs log v que se mostra linear na Fig. 2B, com R próximo a 0,999, sugerindo a adsorção do carbendazim ao eletrodo (GREEF, R, et al, 1985).
CONCLUSÕES: Os resultados obtidos mostraram que o processo de oxidação do carbendazim não é totalmente reversível, e indica a existência de uma reação química acoplada ao processo de transferência de carga. Além disso, os resultados mostraram que o processo não é puramente difusional, podendo ocorrer adsorção do carbendazim na superfície do eletrodo.
AGRADECIMENTOS:Fundação de Apoio ao Desenvolvimento do Ensino, Ciência e Tecnologia do Estado de Mato Grosso do Sul FUNDECT/MS, PIBIC/CNPQ.
REFERÊNCIAS BIBLIOGRÁFICA:DE LA HUEBRA MJ, BALLESTEROS PHY, HERNANDEZ L. 2000. Rapid identification of Carbendazim and linuron by a adsorptive stripping on a carbon fiber ultra microelectrode, Fresenius J. Anal. Chem. 368(8): 853-856.
DE QUEIROZ, S. C. N. 2001. Determinação multiresíduos de pesticidas em água por cromatografia liquida de alta eficiência com ênfase em detecção por espectrometria de massas e novos sorventes para extração em fase sólida: Unicamp, p. 3.
GREEF, R.; PEAT, R.; PETER, L.M.; PLETCHER, D.; ROBINSON, J. 1985. Instrumental methods in Electrochemistry. Ellis Horwood Limited.
NICHOLSON, R.S.; SHAIN, I.1964.Theory of Stationary Electrode Polarography. Single Scan and Cyclic Methods Applied to Reversible, Irreversible, and Kinetic Systems. Anal. Chem..v.36, p.706.
